Окислительно–восстановительные и кислотно–основные свойства
Восстановительные свойства р- элементов в группе сверху вниз растут, а окислительные ослабевают. Примером тому может служить изменение значений Еo для галогенов (Г2):
| Г2/2Г ¯ | F2 | Cl2 | Br2 | I2 |
| Е0, В | 2,87 | 1,36 | 1,07 | 0,53 |
и реакции типа
1/2F2 + 1/2Cl2 + H2O ® HF + HClO
7/2F2 + 1/2I2 ® IF7
Окислителями и восстановителями являются соединения, в которых элементы находятся в неустойчивых степенях окисления и в ходе реакции переходят в более устойчивые. Например, для элементов IVА подгруппы стабильность степени окисления 2+ увеличивается с ростом порядкового номера. Если Gе2+ – сильный восстановитель, то Pb4+ – энергичный окислитель, поэтому не существует PbI4 , PbBr4 , PbS2 , a PbCl4 – очень неустойчивое соединение
PbCl4 = PbCl2 + Cl2.
Окислительная активность Pb4+ проявляется в разрядной реакции свинцового аккумулятора:
PbO2 + Pb + 2H2SO4 = 2PbSO4 + 2H2O.
Наиболее типичные гидроксиды р- элементов с характеристикой их кислотно-основных свойств приведены в табл.10.3. О кислотно-основных свойствах соединений, содержащих группировку Э-О-Н, было сказано в теме «Строение атома». Напомним, что они определяются относительной прочностью связей Э-О и О-Н. Если связь Э-О прочнее связи О-Н, то гидроксид диссоциирует по кислотному типу Э-О — Н = Э-О– + Н+. Если прочнее связь О-Н, то соединение диссоциирует как основание Э — О-Н = Э+ + ОН–. Связь Э-О тем прочнее, чем больше заряд и меньше радиус иона элемента. Увеличение заряда и уменьшение радиуса Э усиливает связь Э-О, делает ее более прочной, следовательно, менее прочной – связь О-Н.
При одинаковой степени окисления кислотные свойства гидроксидов в группе сверху вниз уменьшаются вследствие роста эффективного радиуса иона Эn+.
Так, в IIIA подгруппе происходит усиление основных свойств:
Н3ВО3 – кислота, Al(OH)3 и Gа(ОН)3 – амфотерные соединения,
In(OH)3 – амфотерный гидроксид с преобладанием основной ионизации,
Tl(OH)3 – основание.
В IVA подгруппе Ge(OH)2 , Sn(OH)2 , Pb(OH)2 – амфотерные соединения, их основность растет от Ge к Pb; у Gе(ОН)2 преобладает кислотная ионизация, у Pb(OH)2 – основная:
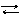
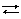
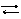 Pb(OH)+ + OH – Pb(OH)2 H2PbO2 H+ + HPbO2–
Pb(OH)+ + OH – Pb(OH)2 H2PbO2 H+ + HPbO2–
K2 = 3.10–8 K1 = 9,6 .10–4 K1 = 4.10–10
В VA подгруппе также наблюдается общая закономерность:
НNO2 и Н3РО3 – слабые кислоты, Вi(OH)3 – основание,
Н3АsO3 – амфотерная кислота, Sb(OH)3 – амфотерное основание.
Большинство гидроксидов р- элементов VIA и VIIA подгрупп являются кислотами. Сила кислот уменьшается сверху вниз в каждой группе. Так, Н2SO4 и Н2SeO4 – cильные кислоты, теллуровая Н2ТеО4 – слабая кислота. В ряду слабых кислот Н2SО3 – Н2SеО3 – Н2ТеО3 у теллуристой кислоты проявляется амфотерность. Кислотные свойства также ослабевают от СI к I, например, HCIO и HBrO – слабые кислоты, а НIO – амфотерное соединение.
Кислотные свойства гидроксидов в периоде возрастают с увеличением заряда ядра Z. Это объясняется тем, что в результате увеличения Z растет ковалентность связи Э-О, а следовательно, повышается ионность связи О-Н.
С увеличением положительной степени окисления элемента уменьшается эффективный радиус, поэтому кислотные свойства гидроксидов усиливаются. Так, Н2SО3 и НNО2 – cлабые, а Н2SО4 и НNО3 – сильные кислоты; ТlOH – сильное, а Tl(OH)3 – слабое основание; Pb(OH)2 – гидроксид с преимущественно основными, а Н2[Pb(OH)6] – с преобладающе кислотными свойствами.
