Определение энтальпии реакции нейтрализации сильной кислоты сильным основанием
Экспериментально энтальпии химических реакций определяют по изменению в ходе реакции температуры реакционной смеси при соблюдении определённых условий, ограничивающих энергетический обмен с окружающей средой. Обычно для этой цели используют специальные приборы – калориметры.
Вариант 1.
Калориметр представляет собой сосуд, снабженный теплоизолирующей оболочкой для уменьшения теплообмена с окружающей средой.
В экзотермической реакции нейтрализации сильной кислоты сильным основанием энтальпия (выделившееся тепло) равна
ΔН = n∙ΔН0,кДж, (1)
где n – количество вещества (протонов), участвующих в реакции, кДж/моль
Это тепло расходуется на нагревание реакционной смеси и сосуда:
Q = К∙Dt. (2)
∆t = tкон.– tнач. – повышение температуры системы, оС.
Коэффициент пропорциональности Кв (2) равен суммарной теплоемкости сосуда и раствора и носит название тепловой постоянной калориметра. Ее можно определить, например, по химической реакции с известным значением DHили, измеряя повышение температуры раствора, вызванное пропусканием тока (J) в течение определенного времени Dt через нагреватель с известным сопротивлением R, который опущен в калориметр с раствором.
J2·R·Dt = K·Dt.
Объединив формулы (1) и (2) nDH0 = – K Dt, можно рассчитать стандартную энтальпию реакции DH0
Чтобы устранить искажение истинной величины Dtв результате частичных потерь тепла в окружающую среду, используют графический метод ее определения. С этой целью записывают изменение температуры в зависимости от времени до начала химического процесса (предварительный период), во время его течения (главный период) и после его окончания (заключительный период). Характерная кривая приведена на рис. 3.3.
Момент окончания химического процесса tс определяют по установлению плавного монотонного хода кривой t(t). Находят середину главного периода tЕ, восстанавливают из точки tЕ перпендикуляр и экстраполируют кривые АВ и СD до пересечения с этим перпендикуляром в точках М и N. Истинное изменение температуры равно отрезку МN.
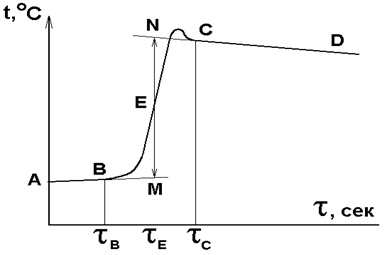
Рис. 3.3. Изменение температуры в зависимости от времени для экзотермического процесса.
Опыты следует проводить вдвоем: один ведет отсчет времени и запись температуры, второй следит за температурой и заливает кислоту.
а) Отмерьте в один цилиндр 110 мл 1н раствора КОН, во второй – 100 мл 1 н раствора сильной кислоты (НCl или Н2SO4).
Опустите в калориметр магнит, залейте в него 110 мл щелочи, закройте крышку и поставьте его на магнитную мешалку. Внимательно следите за процессом перемешивания!
Включив мешалку, (внимательно следите за процессом перемешивания!), в течение 2 – 3 мин. через каждые 10 секунд (время записывать не нужно) записывайте температуру раствора в предварительном периоде) с точностью 0,05oC.
Через 2 – 3 мин. в момент очередного отсчета начните аккуратно и медленно по стеклянной палочке вливать в калориметр через воронку кислоту. С начала и до конца вливания (главный период), показания термометра записывайте уже через 5 сек. Для построения графика таких замеров д. б. ≈ 10.
В заключительном периоде продолжайте вести запись температурного хода через каждые 20 сек., в течение 3 – 5 мин.
б) На миллиметровой бумаге постройте график t (t ), определите Dtграфически и рассчитайте теплоту нейтрализа ции по формуле:
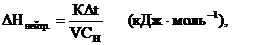 |
гдеCH–нормальность кислоты, моль·л–1 (определяется числом молей протонов Н+ в 1 л раствора);
V – ее объем в л;
K–постоянная калориметра.
Значение постоянной калориметра для объема раствора 210 мл приведено на нем.
в) По указанию преподавателя проведите опыт с другой кислотой – сильной или слабой. Перед проведением второго опыта промойте калориметр, залейте в него воду комнатной температуры и дайте постоять, включив мешалку не менее чем на 10 минут для уравнивания температуры калориметра и воды.
Убедитесь, что теплота нейтрализации разбавленных растворов сильной кислоты сильным основанием мало зависит от вида кислоты, так как при этом всегда осуществляется реакция:
Н+ + ОН– = Н2О, ΔΗ0 = – 55,9 кДж·моль–1
тогда как тепловой эффект нейтрализации слабой кислоты сильным основанием будет меньше, поскольку часть выделившейся энергии образования воды из ионов тратится на диссоциацию кислоты:
СН3СООН + ОН– = СН3СОО– + Н2О.
г) Рассчитайте ΔΗ0 и ΔG0 реакции нейтрализации сильной кислоты сильным основанием, пользуясь значениями термодинамических функций.
Н+(р) + ОН–(р) = Н2О (ж)
S0, Дж·моль–1·К–1 0 –10,8 70
ΔΗ0, кДж·моль–1 0 –230,2 –286,0
Значение ΔΗ0 сравните с экспериментальным.
д) Из уравнения ΔG0 = –RT ln KP , принимая [Н2О] = 1, рассчитайте [Н+]·[ОН–] = Кв (ионное произведение воды).
Вариант 2.
Выделившееся в результате реакции тепло
ΔН = n ΔН0,кДж (1)
расходуется на нагревание реакционной смеси и сосуда и может быть вычислено по формуле:
Q = (cp(р-ра )· mр-ра + cp(ст) mст..) ∆t, Дж, (2)
где n – количество вещества (протонов), участвующих в реакции нейтрализации, кДж/моль
cp – удельные теплоёмкости раствора и сосуда, Дж/г·град.,
m –массы раствора и сосуда, г,
∆t = tкон.– tнач. – повышение температуры системы, оС
Объединив формулы (1) и (2), можно рассчитать стандартную энтальпию реакции:
ΔН0 = – 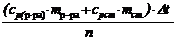 , Дж/моль (3)
, Дж/моль (3)
При определении стандартной энтальпии реакции нейтрализации в качестве калориметра используется полипропиленовый стакан с относительно малой массой.
Низкая теплопроводность материала стакана препятствует прогреванию всего стакана за весьма короткое время эксперимента, задерживая тепло во внутреннем очень тонком слое. Поэтому в формулах (1) и (2) слагаемым(cp(ст.)∙mcт.) можно пренебречь. Ошибка не превысит 1%.
ΔН0 = - 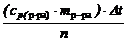 , Дж/моль
, Дж/моль
Процессу нейтрализации в общем случае могут сопутствовать процессы диссоциации (эндотермический, слабые кислоты) и гидратации (экзотермический, сильные кислоты), искажающие результат эксперимента. Их необходимо учитывать, внося поправки в эксперимент.
Для получения удовлетворительных результатов большое значение имеет также достоверность вставляемой в формулу величины удельной теплоёмкости раствора. Она зависит от природы и концентрации веществ, составляющих раствор. Обычно рекомендуется принимать удельную теплоёмкость раствора приближенно равной теплоёмкости воды, т.е. 4.183 Дж/г·град.
Для серной кислоты и гидроксида калия, например, это допущение приводит к завышению результатов примерно на 15−20 %. В этом случае следует пользоваться табличными данными зависимости ср(W), (табл.3.3 и 3.3) или определять удельную теплоёмкость раствора экспериментально.
Таблица 3.2
Теплоёмкость cp, [Дж/г∙град.] водных растворов
NaCl и КCl при 20 оС
| W р-ра, % | Ср | W р-ра, % | Ср |
| 4,18 | 3,90 | ||
| 4,14 | 3,87 | ||
| 4,10 | 3,84 | ||
| 4,07 | 3,79 | ||
| 4,03 | 3,75 | ||
| 3,99 | 3,70 | ||
| 3,96 | 3,52 | ||
| 3,93 |
Таблица 3.3
Теплоёмкость сp, [Дж/г∙град.] водных растворов
Na2SO4 и К2SO4 при 20 оС
| W р-ра, % | Ср | W р-ра, % | Ср |
| 4,18 | 3,63 | ||
| 1,5 | 3,81 | 7,0 | 3,60 |
| 3,71 | 7,5 | 3,58 | |
| 3,5 | 3,69 | 8,0 | 3,56 |
| 4,0 | 3,67 | 8,5 | 3,55 |
| 4,5 | 3,66 | 9.0 | 3,54 |
| 5,0 | 3,65 | 10,0 | 3,52 |
| 5,5 | 3,64 | 10,5 | 3,50 |
Оборудование: штатив химический, мерный цилиндр на 100 мл, мерный полипропиленовый стакан на 100 мл, бюретка на 25 мл, магнитная мешалка, термометр (0 − 100 оС).
Реактивы:
Вода дистиллированная; 4 н кислота (серная или соляная)[3]; 1 н щёлочь (КОН, NaOH)
Ход работы
1. Бюретку заполните раствором 4 н сильной кислоты. Установите мениск на нулевом делении.
2. В мерный стакан опустите магнитик и налейте цилиндром 80 мл щёлочи.
3. Стакан поставьте на магнитную мешалку. Носик бюретки подведите к стакану.
4. Термометр опустите в стакан. Включите перемешивание. Запишите начальную температуру раствора.
5. Прилейте из бюретки 15 мл кислоты. После перемешивания запишите температуру раствора.
6. Определите повышение температуры раствора, ∆t.
7. Проведите холостой опыт. Для этого повторите эксперимент (пункты 1, 3−6), налив в мерный стакан 80 мл дистиллированной воды(вместо щёлочи, п. 2).
8. Определите повышение температуры раствора за счёт процесса гидратации при разбавлении кислоты, ∆tгидр.
9. Определите повышение температуры раствора за счёт процесса нейтрализации, ∆tнейтр. = ∆t - ∆tгидр.
10. Рассчитайте стандартную энтальпию реакции.
Исходные данные и формулы:
Объем КОН 80 мл
Объём кислоты, Vк-ты 15 мл
Концентрация кислоты, СН+ (точно) 4,…моль/л
Плотность исследуемого раствора, ρ 1,03 г/мл
Удельная теплоёмкость, ср, Дж/г∙град
(находится по таблицам (2) и (3) в зависимости от природы и концентрации реагентов.[4])
ΔН0 = - 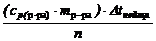 ; ∆tнейтр. = ∆t - ∆tгидр; Vp-pa = 80 + Vк-ты; mp-pa= ρ·Vp-pa; nH+ = СН+∙Vк-ты
; ∆tнейтр. = ∆t - ∆tгидр; Vp-pa = 80 + Vк-ты; mp-pa= ρ·Vp-pa; nH+ = СН+∙Vк-ты
11. Сравните полученный экспериментальный результат стандартной энтальпии реакции нейтрализации сильной кислоты сильным основанием с табличным
Контрольные вопросы
1. Почему в данной работе необходимо проведение холостого опыта?
2. Какую термодинамическую функцию можно рассчитать, исходя из ∆tгидр.?
3. Чем обусловлены отклонения полученного значения энтальпии реакции нейтрализации от истинного?
4. Какие изменения нужно внести в методику проведения эксперимента, чтобы повысить точность полученных результатов?
5. Рассчитайте ΔΗ0 реакции нейтрализации сильной кислоты сильным основанием, пользуясь значениями термо-динамических функций.
