Тема «Спирты (алканолы), тиолы, простые эфиры, сульфиды».
I.Вопросы для проверки исходного (базового) уровня знаний:
1. Какую функциональную группу содержат спирты?
2. Какой тип связи называется водородной? Как наличие этой связи отражается на свойствах спиртов?
3. Написать уравнения реакций взаимодействия этанола с: а)мет Na; б) уксусной кислотой; в) HBr.
4. Привести схемы реакций внутримолекулярной и межмолекулярной дегидратации этанола с указанием условий реакций.
5. Привести структурные формулы бутиловых спиртов.
6. Назвать следующие вещества:
СН3 – О- СН3; СН3- О-С2Н5; СН3-СН – О – СН3
|
CH3
II. Целевые задачи.
| Студент должен знать: | Литература |
| 1.Функциональную группу спиртов. 2.Гомологический ряд спиртов; 3.Изомерию и номенклатуру их. 4.Физические свойства спиртов, их спектральную идентификацию 5.Химические свойства спиртов: - реакции нуклеофильного замещения - реакции отщепления; - кислотно-основные свойства; - реакции окисления и восстановления; 6.Способы получения спиртов, тиолов - гидролиз галогеналканов;- гидратация алкенов; - восстановление карбонильных соединений; - брожение сахаристых веществ; - присоединение сероводорда к алкенам; 7.Многоатомные спирты: - качественная реакция; - дегидратация гликолей: образование диоксана из этиленгликоля; ТГФ из тетраметиленгликоля. 8.Важнейшие представители и их физиологическое действие. 9.Простые эфиры: - формулы простых эфиров и их названия; - простые эфиры-это инертные вещества, но в жестких условиях они подвергаются ацидолизу – расщепляются под действием HI. - взаимодействие со щелочными металлами; - с кислотами образуются оксониевые соли; - радикальные реакции по α- углеродному атому: хлорирование, окисление с образованием гидроперекисей. | ОСНОВНАЯ 1. Э.Т.Оганесян Органичекая химия «Академия», 2011. с 144,168. 2. В.Л.Белобородов, С.Э.Зурабян и др. Органическая химия, основной курс – учебник для вузов. М.: Издательский центр «Дрофа»,2002г стр.340 3. О.Я.Нейланд Органическая химия, Учеб.для хим. спец. вузов.-М. Высш. шк.,1990. с. 280.) ДОПОЛНИТЕЛЬНАЯ: 1. К. Ингольд Теоретические основы органической химии, перевод с англ.М. Мир, 1973 2.Щеголев Органическая химия, учеб. Пособие для студ. мед. и фарм. обр-ю, Архангельск, 2008г., с. 113. |
| Студент должен уметь: | |
| 1. писать структурные формулы изомерных спиртов и тиолов, называть их; 2. записывать уравнения реакций получения спиртов и тиолов: гидролизом галогеналканов, гидратацией алкенов, гидрированием каорбонильных соединений, оксосинтезом через альдегиды и кетоны, сбраживанием сахаристых веществ; присоединением сероводорода к алкенам. 3. в общей формуле спиртов распознавать активные центры и записывать уравнениями реакций химические свойства спиртов: кислотно-основные (взаимодействие с мет.Na, NaOH, 4. влияние заместителей на кислотность спиртов; 5. реакции с участием нуклеофильного центра: О-алкилирования – синтез Вильямсона (образование простых эфиров); О-ацилирование (образование сложных эфиров); 6. реакции с участием электрофильного центра: замещение ОН группы спиртов на галоген; 7. реакции с участием СН-кислотного центра (элиминирования); 8. реакции окисления спиртов, условия дегидрирования первичных, вторичных и третичных спиртов; 9. называть отдельные представители спиртов, тиолов, особенности их химического поведения. 10. называть формулы простых эфиров, сульфидов и по названиям писать формулы их; |
III. Задания для самостоятельной работы по изучаемой теме :
1. Спирты имеют функциональную группу…………, а тиолы……………
2. В зависимости от количества –ОН групп спирты и тиолы делятся на
…………………………………………………………………………….
3. В зависимости от положения – ОН и SH- групп одноатомные
спирты и тиолы делятся на……………………………………………….
4. Первичные спирты окисляются до………………, а вторичные-до………….
Префикс тио- означает замену атома кислорода на атом…………..
5. Схема процесса брожения глюкозы.
6. Назвать по заместительной номенклатуре:

7. Написать структурные формулы следующих соединений:
3-бромгексанол-2; 2-метил-3-этилпентанол-1; пара-меркаптотолуол;
2,7-дихлороктандиол-4,5; 5-метил-4-гексен-1-инол-3.
8.Осуществить превращения:


 С2H4 X Y C2H5 – O – C2H5
С2H4 X Y C2H5 – O – C2H5
9. Составить уравнения реакций взаимодействия пропанола-2
(изопропилового спирта) с металлическим натрием и
бромоводородом, назвать продукты реакций и условия их получения.
10. Составить уравнения реакций гидрирования, гидратации,
галогенирования и гидрогалогенирования 2-пропенола-1.
Назвать продукты реакций.
11.Сколько спиртов имеют молекулярную формулу С5Н12О.
Составить структурные формулы этих веществ и назвать их.
Только ли спиртам соответствует эта формула?
12.Дописать уравнения реакций:
 R-OH + HBr
R-OH + HBr
 CH2=CH-CH3 +H2O
CH2=CH-CH3 +H2O
дрожжи
 C6H12O6
C6H12O6
 СН3СН2Br +NaOH
СН3СН2Br +NaOH
 С2Н5СI + NaSH
С2Н5СI + NaSH
13.Предложить способы получения этанола из: а) метаналя, б) этаналя, в) этена, г) этоксиэтана, д) этилпропионата, е) этилхлорида.
14. Решить задачу: Какую массу карбида кальция надо добавить к 150 мл этанола плотностью 0,8 г/мл для получения абсолютного (безводного) спирта, если массовая доля этанола в спирте составляет 96%? Какая масса абсолютного спирта будет получена при этом? ( Ответ: 8,53гСаС2; 115,2г абсолютного спирта).
15.Какие характеристические полосы поглощения будут присутствовать в ИК-спектре этанола, метантиола?
Тест для самоконтроля
1. Назовите по систематической номенклатуре спирт строения
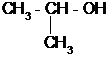
а) 1-метилэтанол-1 б) 2-метилэтанол-1
в) изопропиловый спирт г) пропанол-2
2. Алкоголятами называются продукты взаимодействия:
а) фенолятов с активными металлами
б) спиртов с галогеноводородами
в) спиртов с карбоновыми кислотами
г) спиртов с активными металлами
3. Укажите названия первичных спиртов:
a) этанол б) изопропиловый спирт
в) пропиловый спирт г) изобутиловый спирт
4. Какие виды изомерии возможны для предельного одноатомного спирта с тремя атомами углерода в структуре:
a) углеродного скелета б) положения гидроксильной группы
в) межклассовая г) геометрическая
5. Изомерами диэтилового эфира являются:
a) изопропиловый спирт б) бутанол-1
в) 2-метилпропанол-2 г) бутанол-2
6. Отметьте названия гомологов диметилового эфира:
a) метилэтиловый эфир б) орто-крезол
в) диэтиловый эфир г) этандиол-1,2
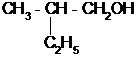 7. Охарактеризуйте спирт строения
7. Охарактеризуйте спирт строения
a) вторичный спирт б) называется: 2-этилпропанол-1
в) гомолог бутанола-1 г) называется: 2-метилбутанол-1
8. Этиленгликоль можно получить:
a) взаимодействием ацетилена с водой
б) взаимодействием этилена с холодным слабощелочным водным раствором KMnO4
в) взаимодействием 1,2-дихлорэтана с водным раствором щёлочи
г) взаимодействием этилена с водой
9. При окислении первичного спирта можно получить:
a) карбоновую кислоту б) альдегид
в) углекислый газ г) простой эфир
10. Между молекулами каких веществ в растворах устанавливаются достаточно прочные водородные связи?
a) вода б) метанол
в) диэтиловый эфир г) этиленгликоль
11. Сколько изомерных тиоспиртов отвечает формуле С4Н9SН?
a) 2 б) 4 в) 3 г) 5
12. Укажите промышленные способы получения этанола:
a) гидратация этилена
б) гидратация ацетилена
в) гидролиз клетчатки и сбраживание полученной глюкозы
г) взаимодействие хлорэтана с водным раствором Са(ОН)2
13. Как можно выразить состав предельных одноатомных спиртов и тиолов?
a) CnH2n+1OH б) CnH2nO
в)CnH2n+2O г) СnH2n+1SH
14. Укажите название вещества, при внутримолекулярной дегидратации которого может образоваться пентен-2:
а) пентанол-1 б) пентанол-2
в) гексанол-2 г) 2-метилбутанол-1
15. В реакциях с каким веществом от спиртов отщепляется группа ОН?
a) натрий б) бромоводород
в) уксусная кислота г) калий
16. Какое вещество можно распознать с помощью свежеприготовленного гидроксида меди(II)?
a) метанол б) бензол
в) глицерин г) этилен
17. Пропанол-1 и пропанол-2 по отношению друг к другу являются:
a) гомологами б) изомерами
в) ни гомологами, ни изомерами
18. Какие вещества являются изомерами диэтилового эфира?
а) фенол б)бензиловый эфир в) бутанол-1 г) метилпропиловый эфир
 19. Выберите название спирта, который преимущественно получается при гидратации алкена строения
19. Выберите название спирта, который преимущественно получается при гидратации алкена строения
a) 2-метилбутанол-4 б) 3-метилбутанол-2
в) 2-метилбутанол-3 г) 2-метилбутанол-2
Ответы: 1 a; 2 г;3 a,в; 4б;5 б,d;6a,в;7г;8 в;9 а,в; 10 a,б,г;11 в;12 а,б,г;13 а, г;14б;15б;16в;17б;18г;19б.
Задания для самостоятельной работы студентов 2 курса фарм. факультета по курсу органической химии.
Тема «Фенолы»
I.Вопросы для проверки исходного (базового) уровня знаний:
1. Привести структурные формулы всех изомерных фенолов состава С7Н8О.
2. Написать структурные формулы следующих веществ: фенола, о-крезола (о –метилфенола), гидрохинона ( п-гидроксифенола), пирокатехина (1,2-дигидроксибензола), резорцина (1,3- дигидроксибензола), бензилового спирта, пирогаллола (1,2,3 – тригидроксибензола).
3. Способ получения фенола из бензола в две стадии.
4. Почему фенол «кислее» воды и спиртов?
5. Как влияют электронодонорные и электроноакцепторные заместители на кислотные свойства фенола?
6. Как влияет наличие гидроксогруппы на ароматичность кольца?
7. Записать уравнение реакции бромирования фенола.
II.Целевые задачи:
| Студент должен знать: | Литература |
| 1. Фенолы и ароматические спирты –это не одно и то же; формулы и названия двухатомных фенолов и продуктов их окисления; 2. Почему фенол «кислее» воды и спиртов, от чего это зависит; 3. Как разные по электроотрицательности заместители в фенолах сказываются на их кислотных свойствах; 4. Химические свойства фенолов: их взаимодействие с о щелочами, ацилирование, нуклеофильное замещение гидроксогруппы на хлор в присутствии электроноакцепторных заместителей, на аминогруппу; электрофильное замещение (-ОН группа – это орто-, пара- ориентант): бромирование, нитрование, сульфирование, алкилирование и ацилирование по Фриделю-Крафтсу; образование фенолформальдегидной смолы 5. Способы получения фенолов: сплавлением аренсульфоновых кислот со щелочами, гидролизом галогенаренов, гидролизом арендиазониевых солей | ОСНОВНАЯ 1.Э.Т.Оганесян Органичекая химия «Академия», 2011. с 156. 2. В.Л.Белобородов, С.Э.Зурабян и др. Органическая химия, основной курс – учебник для вузов. М.: Издательский центр «Дрофа»,2002г стр.363…, 390… 3. О.Я.Нейланд Органическая химия, Учеб.для хим. спец. вузов.-М. Высш. шк.,1990. с. 312.) ДОПОЛНИТЕЛЬНАЯ: 1. К. Ингольд Теоретические основы органической химии, перевод с англ.М. Мир, 1973 2.Щеголев Органическая химия, учеб. Пособие для студ. мед. и фарм. обр-ю, Архангельск, 2008г., с. 450. |
| Студент должен уметь: | |
| 1. писать формулы одно- , двух и трехатомных фенолов, называть их; 2. отличать фенолы от ароматических спиртов; 3. сравнивать кислотные свойства фенола и его замещенных; 4. писать уравнения реакций, отражающие химические свойства фенола: нуклеофильные свойства: алкилирование (образование простых эфиров), ацилирование ( образование сложных эфиров); электрофильное замещение: галогенирование, нитрование, алкилирование и ацилирование в кольцо по Фриделю-Крафтсу, сульфирование, взаимодействие с формальдегидом. нуклеофильное замещение ОН группы на СI в присутствии электроноакцепторных заместителей; реакции окисления и восстановления; цветные реакции на фенолы; 5. подтверждать уравнениями реакций взаимное влияние гидроксогруппы и бензольного кольца; 6. писать уравнения реакций получения фенола и двухатомных фенолов; 7. называть важнейшие представители и их физиологическое действие. |
III. Задания для самостоятельной работы по изучаемой теме:
1. Привести структурные формулы всех изомерных: а) фенолов состава С7Н8О;
б) ароматических спиртов состава С8Н10О; в) двухатомных фенолов состава
С6Н6О2. Назвать все соединения.
2. Какие из соединений:
a) фенол;
b) бензиловый спирт;
c) о-крезол;
d) β-фенилэтиловый спирт;
e) анизол (метоксибензол)
f) салициловая кислота
будут давать цветную реакцию при действии водного раствора FeCl3?
3. Сравнить отношение к действию окислителей следующих соединений:
а) бензола; б) толуола в) бензилового спирта; г) фенола; д) гидрохинона.
4. Качественные реакции на этанол (образование этилацетата; образование иодоформа), на глицерин ( обраование хелатного комплекса, акролеиновая проба), на фенол ( с водным раствором FeCI3, образование трибромфенола).
5.Написать реакции, лежащие в основе технических методов получения фенола:
a) из бензолсульфокислоты;
б) из хлорбензола;
в) из кумола (изопропилбензола). Указать условия. В чём преимущество кумольного метода перед другими?
6.Осуществить превращения:



 Карбид кальция ацетилен бензол Х фенол
Карбид кальция ацетилен бензол Х фенол
6.сравнить реакционную способность бензола и фенола в реакциях электрофильного замещения. Привести реакции нитрования, бромирования , сульфирования. Действием каких реагентов и в каких условиях осуществляются эти реакции?
7. Привести структурные формулы соединений: фенола, о-крезола
(о-метилфенола), гидрохинона, пирокатехина, резорцина, бензилового спирта,
анизола (метилфенилового эфира), фенетола (этилфенилового эфира), дифенилового эфира, аллилфенилового эфира, фенилацетата, фенилбензоата, фенолята натрия.
8.В каждой группе расположить соединения в порядке уменьшения кислотности: а) серная кислота, угольная кислота, фенол, вода;
б) фенол, бензиловый спирт, бензойная кислота;
в) фенол, п-нитрофенол, м-нитрофенол, 2,4-динитрофенол, 2,4,6-тринитрофенол.
9.Кумольный способ получения фенола
10.При лечении катаров дыхательных путей используют гваякол (2-метоксифенол). Предложить способ его получения из хлорбензола с помощью последовательных реакций.
11.Сравнить кислотные свойства фенола, этанола и пикриновой кислоты.
12.Сравнить нуклеофильные свойства этанола и фенола.
13.Как с помощью ИК-спектроскопии доказать наличие гидроксогрупп в этаноле и феноле?
14.Решить задачи:
а) Определить массу 10%-го раствора гидроксида натрия, необходимого для реакции с 42,3 г фенола.
б) Какая масса 96% -ной азотной кислоты потребуется для реакции с 470г фенола, если выход продукта составил 90%.
Тесты для самоконтроля:
1. Кислотные свойства наиболее выражены у
a) фенола b) метанола
c) этанола d) глицерина
2. Укажите название вещества с наиболее сильными кислотными свойствами:
a) метанол б)вода
в) диметиловый эфир г) фенол
3. С какими веществами реагируют как фенол, так и бензол?
a) бром б) натрий
в) нитрующая смесь г) водный раствор гидроксида натрия
4. Укажите число σ-связей в молекуле фенола:
a) 11 б) 12 в) 13 г) 15
5. Для обнаружения фенола используются:
a) хлороводород
b) свежеприготовленный гидроксид меди (II)
c) хлорид железа (III)
d) бромная вода
6. Какое вещество используется как антисептик?
a) бензол
b) толуол
c) диметиловый эфир
d) фенол
7. В каких парах оба вещества являются изомерами по отношению друг к другу?
a) этанол и диметиловый эфир
b) пропанол-1 и изопропиловый спирт
c) фенолят натрия и этилат натрия
d) 2-метилпропанол-1 и 2-метилпропанол-
8. При взаимодействии фенола с какими веществами замещению подвергается
атомы водорода в бензольном кольце?
a) азотная кислота
b) бромная воды
c) гидроксид натрия
d) калий
9. Фенол от спирта можно отличить реакцией с
a) Na b) NaOH в) NaHSO4 c) NaNO3
10. Какие реакции подтверждают взаимное влияние гидроксогруппы и бензольного кольца ?
a) взаимодействие с NaOH b) образование простого эфира
с) замещение водорода в бензольном кольце на галогены
d) реакция присоединения.
Ответы: 1. a; 2. d; 3. a,в; 4. c; 5. c; 6. d; 7. a,b,d; 8. a,b; 9.b; 10. a,c
Задания для самостоятельной работы студентов 2 курса фарм. факультета по курсу органической химии.
Тема «Альдегиды и кетоны».
I.Вопросы для проверки исходного (базового) уровня знаний
1. Какие классы органических соединений вам уже известны?
2. Какую функциональную группу содержат альдегиды и кетоны.
3. Какие химические свойства объясняются наличием этой группы? Особенности химического поведения изученных классов веществ.
4. Важнейшие способы получения альдегидов и кетонов.
5. Составить структурные формулы бутаналя и диметилкетона, а также продуктов их гидрирования.
6. Написать структурные формулы всех изомерных альдегидов и кетонов состава С4Н8О и назвать их.
7. Привести структурные формулы соединений: а) пентаналя; 2-метилбутаналя;β- метилпентаналя; пропеналя (акролеина); бензальдегида; 2-метилпентанона-3;
II. Целевые задачи:
| Студент должен знать | Литература |
| 1. Функциональную группу альдегидов и кетонов: карбонильную группу и ее строение. 2. Изомерию и номенклатуру альдегидов и кетонов. 3. Физические свойства. 4. Химические свойства: -реакции нуклеофильного присоединения; - реакции замещения в радикале; - реакции окисления-восстановления. 5. Способы получения: - гидролиз геминальных дигалогеналканов; - окисление одноатомных спиртов; - секстетные перегруппировки α- гликолей; - гидратация ацетиленовых углеводородов; - озонолиз этиленовых углеводородов; - гидроформилирование алкенов; - пиролиз бариевых или кальциевых солей карбоновых кислот. 6. Важнейшие представители и их физиологическая роль: наркотические свойства, дезинфицирующее действие, токсичность. 7. II. Непредельные 8. Кетен: строение, химическое поведение, способы получения. 9. Непредельные карбонильные соединения с сопряженными π- связями: акролеин, кротоновый альдегид. Названия, физические свойства, физиологическое действие. 10. III. Дикарбонильные соединения: глиоксаль, диацетил, малоновый альдегид, ацетилацетон, янтарный альдегид, ацетонилацетон. 11. Классификация: α, β, γ-дикарбонильные соединения, различия в их химических свойствах. | ОСНОВНАЯ 1.Э.Т.Оганесян Органичекая химия «Академия», 2011. с 180. 2. В.Л.Белобородов, С.Э.Зурабян и др. Органическая химия, основной курс – учебник для вузов. М.: Издательский центр «Дрофа»,2002г стр.420 3.О.Я.Нейланд Органическая химия, Учеб.для хим. спец. вузов.-М. Высш. шк.,1990. с. 435.) ДОПОЛНИТЕЛЬНАЯ: 1. К. Ингольд Теоретические основы органической химии, перевод с англ.М. Мир, 1973 2. Щеголев Органическая химия, учеб. Пособие для студ. мед. и фарм. обр-ю, Архангельск, 2008г., с. 213. |
| Студент должен уметь: | |
| 1. записывать структурные формулы альдегидов и кетонов по их названиям; 2. называть формулы их; 3. способы получения их; 4. выделять реакционные центры в формуле; 5. называть основные химические свойства и записывать уравнения реакций, характерные для альдегидов и кетонов, а именно: 6. реакции нуклеофильного присоединения: образование бисульфитного производного, циангидрина, полуацеталей и ацеталей со спиртами, альдиминов с аммиаком, гидразонов и азинов с гидразином и его производными, оксимов с гидроксиламином, альдольной и кротоновой конденсации; 7. реакции замещения в радикале, 8. образование фенол-формальдегидной смолы, 9. реакции Канниццаро, 10. реакции идентификации альдегидов и кетонов: восстановление аммиачного раствора оксида серебра (реактива Толленса), восстановления меди. |
III. Задания для самостоятельной работы по изучаемой теме.
1. Альдегиды и кетоны содержат……………………………….группу.
2. Написать структурные формулы следующих альдегидов:
2-метилпентаналь; 2,3-диметилпентаналь;
3. Назвать по заместительной номенклатуре ИЮПАК:
СН3-СН2-СН2-СОН; СН3 – СН – СН –СН-СОН
| | |
СН3- СН2- СО –СН3 CH3 CH3 CH3
4.Осуществить следующие превращения:



 Этаналь этанол этилен ацетилен
Этаналь этанол этилен ацетилен
 уксусный альдегид
уксусный альдегид
5.Какой объем формальдегида надо растворить в воде массой
300г для получения формалина с массовой долей
формальдегида 40%? Какая масса формалина будет получена?
(149,3л; 500г)
6.Осуществить превращения:


 карбид алюминия метан ацетилен этаналь
карбид алюминия метан ацетилен этаналь
7. Какое количество вещества формальдегида содержится в
растворе объемом 3л и плотностью 1,06 г/мл, массовая доля
СН2О в котором равна 20%? (21,2моля)
8. Назвать приведенные ниже соединения по международной
номенклатуре: а) пропионовый альдегид; б) ацетон;
в)метилизопропилкетон. г) изовалериановый альдегид.
8. Какие реакционные центры присутствуют в молекулах альдегидов?
9. Какие вещества дают иодоформную реакцию? Привести пример.
10. Записать реакции «медного» ( проба Троммера) и «серебряного»
(проба Толленса) зеркала.
11.Записать уравнения реакций получения ацетона из ацетата натрия.
12. Реакции нуклеофильного присоединения к карбонильным
соединениям:
а) получить бисульфитное производное ацетона;
б) присоединение синильной кислоты к этаналю –
циангидринный синтез;
в) присоединение магнийорганических соединений к
карбонильным соединениям и последующий гидролиз.
13. Записать уравнение реакции получения оксима ацетона.
14.Получить ацетон кумольным способом.
Тест для самоконтроля по альдегидам и кетонам
1.Альдегиды и кетоны содержат
а) гидроксогруппу; б) карбоксильную группу; в) карбонильную группу.
2.Карбонильная группа предполагает реакции:
а) электрофильного замещения; в) электрофильного присоединения;
б) нуклеофильного замещения; г) нуклеофильного присоединения
3.Реакции нуклеофильного присоединения – это взаимодействие с :
а) бисульфитом натрия; б) спиртом; в) тиолами;
г) гидразинами; д) гидроксиламином; е) синильной кислотой;
4.Уксусный альдегид реагирует с каждым из двух веществ:
а) аммиачным раствором оксида серебра и кислородом;
б) гидроксидом меди (II) и оксидом кальция;
в) соляной кислотой и серебром;
г) гидроксидом натрия и водородом.
5. Взаимодействуют между собой:
А) этанол и хлорид натрия;
Б) уксусная кислота и хлор;
В) этаналь и бисульфит натрия;
Г) метан и гидроксид меди
6. При окислении альдегидов образуется:
а) спирты б) кетоны в) кислоты г) эфиры
7. Что образуется при окислении метаналя?
а) метановая кислота б) метанол в) ацетон г) уксусная кислота
8. Реакцию «серебряного зеркала дают:
а) метаналь б) метановая кислота в) метанол г) глицерин
9.При окислении вторичных спиртов образуются:
а) альдегиды; б) кислоты в) кетоны г) спирты
10. Галоформная реакция является качественной на:
А) многоатомные спирты; Б) карбоновые кислоты;
В) карбонильные соединения, содержащие метильную группу;
Ответы:1-в; 2-г; 3- со всеми; 4-а; 5 – б,в; 6-в; 7- а; 8 –а,б; 9-в; 10-в
Задания для самостоятельной работы студентов 2 курса фарм. факультета по курсу органической химии.
Тема «Карбоновые кислоты».
I.Вопросы для проверки исходного (базового) уровня знаний
- Какую функциональную группу содержат карбоновые кислоты?
- Записать структурные формулы следующих веществ: метановая кислота, 2-метилбутановая кислота, 2,3-диметилпентановая кислота, 2,3,4-трихлорпропановая кислота.
- Как различить растворы этанола, муравьиной и уксусной кислот?
- Осуществить превращения:


 метан Х У этановая кислота
метан Х У этановая кислота
- Сколько изомерных одноосновных карбоновых кислот может соответствовать формуле С5Н10О2?
II. Целевые задачи:
| Студент должен знать: | Литература: |
| 1. Предельные монокабоновые кислоты. 2. Функциональную группу карбоновых кислот: карбоксильную группу и ее строение. 3. Номенклатуру и изомерию моно-карбоновых кислот. 4. Физические свойства их. 5. Химические свойства: (реакционные центры карбоновых кислот) - кислотно-основные свойства; - реакции нуклеофильного замещения; - реакции с участием α-водородных атомов; - реакции декарбоксилирования кислот и их солей; - дегидратацию амидов кислот (образование нитрилов кислот) -нуклеофильное присоединение к нитрилам. 6. Функциональные производные карбоновых кислот: -ацилгалогениды; - ангидриды; - сложные эфиры; - лактоны; - амиды; 7. Способы получения карбоновых кислот: - окисление одноатомных спиртов; - окисление альдегидов и кетонов; - окисление непредельных углеводородов; - гидролиз геминальных тригалогеналканов; - гидролиз своих ацильных производных (галогенангидридов, ангидридов, сложных эфиров, амидов) - металлорганический синтез; - реакция карбонилирования 8. Важнейшие представители карбоновых кислот и их физиологическое действие. 9. II. Непредельные монокарбоновые кислоты(2, с. 550;3, с.262) 10. Номенклатура и изомерия. 11. Строение (сопряженные, несопряженные) 12. Химические свойства: - кислотность; - реакции присоединения; - реакции радикального замещения. 11. Способы получения: 12. Важнейшие представители и их физиологическая роль. 13. III. Дикарбоновые кислоты: ( 2, с. 556; 3, с.270) 14. особенности химического поведения; | ОСНОВНАЯ 1. Э.Т.Оганесян Органичекая химия «Академия», 2011. с 200. 2.В.Л.Белобородов, С.Э.Зурабян и др. Органическая химия, основной курс – учебник для вузов. М.: Издательский центр «Дрофа»,2002г стр.453. 3.О.Я.Нейланд Органическая химия, Учеб.для хим. спец. вузов.-М. Высш. шк.,1990. с. 536.) ДОПОЛНИТЕЛЬНАЯ: 1. К. Ингольд Теоретические основы органической химии, перевод с англ.М. Мир, 1973 2. Щеголев Органическая химия, учеб. Пособие для студ. мед. и фарм. обр-ю, Архангельск, 2008г., с. 239. |
| Студент должен уметь: | |
| 1. записывать общую формулу насыщенных карбоновых кислот; 2. составлять структурные формулы изомерных карбоновых кислот и называть их; 3. давать названия карбоновым кислотам тривиальные, а также по заместительной номенклатуре; 4. записывать уравнения реакций способов получения карбоновых кислот: а) реакцией гидрофрормилирования; б) окислением первичных спиртов, альдегидов и кетонов; в) иодоформной реакцией; г) из металлорганических соединений; 5. сравнивать силу кислоты в зависимости от характера радикала ее, длины и разветвленности радикала; 6. записывать уравнения реакций нуклеофильного замещения: со спиртами, галогенидами фосфора, (образование галогенангидридов кислот); образования амидов кислот, их ангидридов, декарбоксилирование кислот, галогенирование, дегидратацию, восстановления; 7. записывать уравнения реакций получения производных карбоновых кислот из их хлорангидридов |
III. Задания для самостоятельной работы по изучаемой теме
1. Дописать пропущенные слова: карбоновые кислоты содержат
…………………. группу, их систематические названия имеют окончание…….. .
2. Температуры кипения монокарбоновых кислот выше
температур кипения спиртов соответствующих спиртов и
альдегидов, т.к……………………………………………….. .
3. Расположить следующие кислоты в порядке усиления их
кислотных свойств: уксусную, пропионовую, хлоруксусную,
дихлоруксусную, трихлоруксусную.
4. Составить структурные формулы веществ, имеющих состав:
С3Н6О2. К каким классам веществ их можно отнести?
5. Назвать следующие вещества:
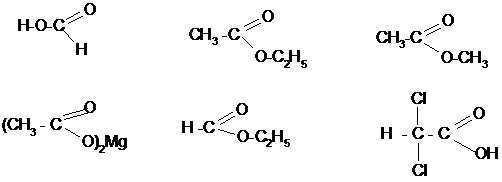
6.Осуществить превращения:


 этилацетат ацетат натрия метан ацетилен
этилацетат ацетат натрия метан ацетилен


 этаналь этановая кислота этилацетат
этаналь этановая кислота этилацетат
7.Написать структурные формулы всех изомерных кислот
состава С5Н10О2. Назвать их. Для кислоты, имеющей
хиральный центр, привести формулы D и L энантиомеров.
8.Какая кислота в паре более сильная и почему: муравьиная и
уксусная; уксусная и триметилуксусная; α- хлормасляная и β-
хлормасляная; муравьиная и щавелевая.
9.В какой области ИК- спектра находятся полосы поглощения, вызванные
колебаниями атомов карбоксильной группы?
Можно ли по ИК-спектру различить валентные колебания ОН-группы спирта и кислоты? Карбонильной группы кетона и кислоты?
10.На примере уксусной кислоты и уксусного альдегида показать
различия их химических свойств.
11. Дописать уравнения реакций;
 а) СН3СООН + С2Н5ОН
а) СН3СООН + С2Н5ОН
 б) СН3СООН + CI2
б) СН3СООН + CI2
 в) СН3СООН + РОCI3
в) СН3СООН + РОCI3
 г) НСООН + Ag2O
г) НСООН + Ag2O
 д) СН3СОСI + NH3
д) СН3СОСI + NH3
 е)СН3СООNa + NaOH
е)СН3СООNa + NaOH
12. Осуществить превращения;
KBr Mg CO2 H2O C2H5OH




 этанол A B C D
этанол A B C D
13. Написать схемы получения из пропионовой кислоты ее
производных: натриевой соли; кальциевой соли;
хлорангидрида; амида; нитрила; ангидрида; этилового эфира.
14. Из уксусной кислоты, получить а) бромуксусную;
б)оксиуксусную; в) аминоуксусную. Привести схемы реакций , условия.
15.Какое химическое свойство роднит сложные эфиры и амиды кислот?
16. Записать уравнения реакций получения муравьиной, пропановой бензойной
кислот окислением соответствующих альдегидов, Гидролизом каких
тригалогенпроизводных эти кислоты могут быть получены?
17.Из предложенных веществ обнаружить ацетат калия.
18. Используемые в качестве жаропонижающих и болеутоляющих средств
парацетамол и фенацетин являются замещенными амидами уксусной
кислоты. Как определить, что среди предложенных соединений эти
препараты присутствуют?
19. Из серии предложенных веществ выбрать муравьиную, уксусную и
щавелевую кислоты.
20. Решить задачу: Окислением пропанола-1 массой 7,2 получили
пропионовую кислоту, на нейтрализацию которой затраили раствор
объемом 16,4 мл с массовой долей гидроксида натрия 20% и плотностью
1,22 г/мл. Определить выход кислоты. ( Ответ: 83,3
Тест для самоконтроля
1.Уксусная кислота может реагировать с:
а) этанолом б) этаналем в) ацетоном г) метановой кислотой
2.Что образуется при окислении метаналя?
а) метановая кислота б) метанол в) ацетон г) уксусная кислота
3.Реакция этерификации – это взаимодействие карбоновой кислоты с:
а) альдегидом б) спиртом в) кислотой
4. При взаимодействии уксусного ангидрида с метиламином образуется:
А) метиламид уксусной кислоты и метанол;
Б) метиламид уксусной кислоты и уксусная кислота;
В) метиламид муравьиной кислоты и уксусная кислота.
5. При взаимодействии пропионовой кислоты с этанолом образуется
А) ангидрид пропионовой кислоты;
Б) этилпропионат;
В) пропилацетат
6. При окислении альдегидов образуется:
а) спирты б) кетоны в) кислоты г) эфиры
7. Взаимодействуют между собой:
А) этанол и хлорид натрия;
Б) уксусная кислота и хлор;
В) этаналь и бисульфит натрия;
Г) метан и гидроксид меди
8. При окислении третичных спиртов образуются:
а) кислоты б) спирты в) кетоны г) альдегиды
9. Реакцию «серебряного зеркала» дают:
а) метаналь б) метановая кислота в) метанол г) глицерин
10.Конечным продуктом, образующимся при окислении этилбензола
перманганатом калия в кислой среде является:
А) бензойная кислота;
Б) бензиловый спирт;
В) фенилуксусная кислота;
Г) бензальдегид
11.Расположить следующие кислоты в порядке увеличения их кислотности:
а) пропеновая
б) пропановая
в) пропиновая
12. Оптическая изомерия характерна для:
а) пропановой кислоты
б) гексена
в) 2-аминопропановой кислоты
г) толуола
Ответы: 1- а; 2- а; 3- в; 4-б; 5 -б; 6 - в; 7 -б,в; 8- а,в; 9 - а,б; 10-в; 11-в,а,б; 12-в.
Задания для самостоятельной работы студентов 2 курса фарм. факультета по курсу органической химии.
