Международная система единиц (СИ) (в сокращении)
| Величина | Единица измерения | Сокращенное обозначение | Переводной коэффициент |
| Длина | Метр | м | 1 см = 10-2 м |
| Площадь | Квадратный метр | м2 | 1 см2 = 10-4 м2 |
| Объем | Кубический метр | м3 | 1 л = 10-3м3 |
| Время | Секунда | сек | - |
| Скорость | Метр в секунду | 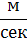 | 1 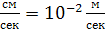 |
| Масса | Килограмм | кг | 1 г = 10-3 кг |
| Химическая масса | Киломоль Килограмм-эквивалент | кмоль кг-экв | 1 моль = 10-3 кмоль 1 кг-экв = 10-3 г-экв |
| Плотность | Килограмм на куб. метр | 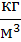 | 1 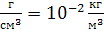 |
| Работа, энергия | Джоуль | дж | 1л атм = 1,013·103 дж 1 эрг = 10-7 дж 1кгм = 9,81дж |
| Давление | Ньютон на кв. метр | 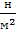 = Па = Па | 1 кГ = 9,8 н 1атм = 1,013⋅105 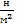 =1013гПа 1мм.рт.ст.= 1,333⋅102 =1013гПа 1мм.рт.ст.= 1,333⋅102 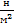 1ат = 9,8⋅104 1ат = 9,8⋅104 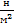 |
| Сила | Ньютон | н | 1 дина = 10-3 н |
| Теплота, внутренняя энергия | Джоуль | дж | 1 кал = 4,19 дж 1ккал = 4,19·103дж |
| Молярная теплота (сгорания, образования) | Джоуль на киломоль | 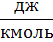 | 1 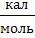 = 4,19 = 4,19 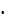 103 103 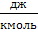 1 1 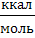 = 4,19 ×106 = 4,19 ×106 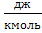 |
| Молярная теплоемкость | Джоуль на киломоль -градус | 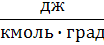 | 1 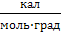 = 4,19×103 = 4,19×103 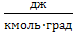 |
| Электрическое напряжение | Вольт | в | 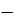 |
| Электрическое сопротивление | Ом | ом | 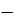 |
| Количество элекричества | Кулон | к | 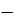 |
| Удельная электропроводность | Ом-1м-1 | 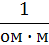 | 1 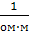 = 102 = 102 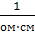 |
| Эквивалентная электропроводность | Сименс на метр | 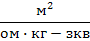 | 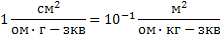 |
| Подвижность ионов | 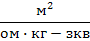 | 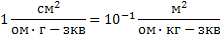 | |
| Молярность | 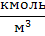 | 1 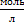 = = 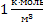 | |
| Нормальность | 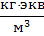 | 1 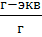 = = 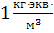 | |
| Разбавление | 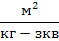 | 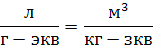 | |
| Поверхностное натяжение | Ньютон на метр | 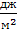 = =  | 1 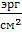 = = 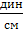 = 10-3 = 10-3  |
| Вязкость | 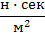 | 1 пуаз = 0,1 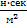 |
Некоторые физические постоянные
| Величина | Сокращенное обозначение единицы измерения |  Переводной коэффициент Переводной коэффициент |
| Универсальная газовая постоянная | 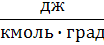 | 0,082 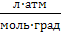 1,98 1,98 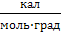 8,3⋅107 8,3⋅107 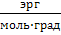 8,3⋅103 8,3⋅103 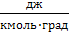 8,3 8,3 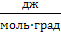 |
| ЧислоАвогадро | 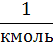 | 6,02·1023 моль-1 = 6,02·1026кмоль-1 |
| ЧислоФарадея | 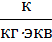 | 9,65⋅104 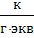 = 9,65⋅107 = 9,65⋅107 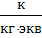 |
| Объем одного кмоль идеального газа | 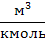 | 22,3 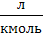 = 22,4 = 22,4 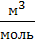 |
Библиографический список
& Основная литература
Хмельницкий Р.А. Физическая и коллоидная химия.- М.: Высш. шк., 1988.
Болдырев А.И. Физическая и коллоидная химия. - М.: Высш. шк., 1983.
Кругляков П.М. Физическая и коллоидная химия: учеб пособие / П.М.Кругляков, Т.Н.Носкова: 2-е изд., испр. М., 2007
Сумм Б.Д. Основы коллоидной химии: учеб пособие / Б.Д.Сумм: 2-е изд., стер. М., 2007
¨ Дополнительная литература
1. Галинкер И.С. и др. Физическая и коллоидная химия. - М.: Высш. шк., 1972.
2. Денисов В.В. и др. Химия. - М.: ИКЦ «Март» Ростов н/Д:, 2003.
3. Ершов Ю.А. Общая химия. - М.: Высш. шк., 2000.
4. Практикум по физической и коллоидной химии /М.С.Чемерис.-Новосибирск, 1999.
Примерные затраты учебного времени при самостоятельной работе по темам и на выполнение контрольной работы в часах:
Введение 1
Часть 1. Физическая химия
1. Агрегативные состояния вещества 2
2. Химическая термодинамика и термохимия 6
3. Химическая кинетика и катализ 5
4. Химическое равновесие 4
5. Растворы неэлектролитов 3
6. Растворы электролитов 6
7. Электропроводность растворов 6
8. Электрохимия 7
9. Поверхностные явления 5
Часть 2. Коллоидная химия
1. Коллоидные системы и их получение 3
2. Молекулярно-кинетические свойства коллоидных систем. Очистка коллоидов 2
3. Оптические свойства коллоидных систем 2
4. Электрические свойства коллоидных систем 3
5. Устойчивость и коагуляция коллоидных систем 4
6. Микрогетерогенные системы. Полуколлоиды. 2
7. Растворы высокомолекулярных соединений 4
8. Гели и студни 3
Чемерис Марина Сергеевна
ФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ
Методическое пособие и задания для контрольных работ
Редактор Н.К. Крупина
Компьютерная верстка М.С. Чемерис
