Молекулярно-абсорбционная спектроскопия (фотометрический анализ)
Принцип метода: в зависимости от того, в какой области спектра измеряют аналитический сигнал, методы молекулярно-абсорбционной спектроскопии разделяют на две группы: 1) фотометрический анализ в УФ- и видимой области (спектрофотометрия); 2) ИК-спектроскопия. Соответствующие методы сильно различаются по своим возможностям, но основаны они на одних и тех же теоретических закономерностях.
Общие закономерности поглощения света: при пропускании монохроматического светового потока через кювету с раствором, содержащим молекулы или ионы Х, интенсивность светового потока уменьшается. Это связано с рядом причин: часть света поглощается молекулами или ионами Х, другая часть – растворителем и примесями, третья - рассеивается и отражается стенками кюветы. Чтобы учесть потери света, связанные с растворителем и кюветой, измерения проводят относительно раствора сравнения, не содержащего Х. Обычно в качестве раствора сравнения используют чистый растворитель. Если поместить и фотометрируемый раствор, и раствор сравнения в одинаковые кюветы, а затем через эти кюветы пропускать свет с одной и той же длиной волны и одинаковой начальной интенсивностью, то потери света на отражение и рассеяние для обеих кювет окажутся одинаковы. Тогда различие в интенсивности получаемых световых потоков (I и I0) будет определяться лишь природой и концентрацией Х.
В качестве аналитического сигнала в молекулярно-абсорбционной спектроскопии используют оптическую плотность (А). Это десятичный логарифм отношения интенсивности монохроматического света, прошедшего через раствор сравнения, к интенсивности света, прошедшего через исследуемый раствор:
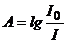
Оптическая плотность – безразмерная величина. Она не зависит от Iнач, а определяется природой и концентрацией частиц, поглощающих свет на данной длине волны, а также толщиной поглощающего слоя в кювете. Связь этих величин описывает основной закон светопоглощения, который принято называть законом Бугера – Ламберта - Бера: в соответствии с этим законом, оптическая плотность раствора, измеренная на некоторой длине волны, прямо пропорциональна концентрации растворенного вещества, поглощающего свет на этой длине волны, и толщине слоя раствора.
А = εl С
Концентрацию поглощающих частиц (С) выражают в моль/л, толщину слоя (l) - в сантиметрах. В таком случае коэффициент пропорциональности ε называют молярным коэффициентом поглощения. Его величина зависит от природы Х и длины волны, на которой измеряют оптическую плотность.
Аппаратура: для измерения оптической плотности растворов и регистрации спектров поглощения используют спектрофотометры. Важнейшая их часть - монохроматор. Другие узлы - источник света, приемник излучения и регистрирующее устройство.
Источники света. В зависимости от оптической области, в которой работает прибор, источниками света служат: в УФ-области – водородная или дейтериевая газоразрядные лампы, дающие сплошной спектр излучения; в видимой области – обычная лампа накаливания с вольфрамовой нитью, в ИК-области – глобар (керамический стержень, нагреваемый до температур порядка 1600 0С).
Монохроматоры. В спектрофотометрах применяют призменные монохроматоры или дифракционные решетки. Материал, из которого изготавливают оптическую систему прибора, должен хорошо пропускать свет в рабочем диапазоне длин волн. В УФ-области используют кварц, в видимой области – стекло, в ИК-области – кристаллические соли, галогениды щелочных и щелочноземельных металлов (NaCl, KBr, CaF2).
Прибор настраивают на нулевую оптическую плотность по кювете с раствором сравнения, а затем вместо нее вводят в световой поток кювету с исследуемым раствором. В результате меняется интенсивность светового потока, падающего на приемник излучения (фотоэлемент), меняется и величина фототока.
Фотометрический анализ: чтобы выбрать оптимальные условия анализа, после проведения фотометрической реакции исследуют спектр поглощения полученного соединения. Вид конкретного спектра и значения вышеперечисленных характеристик определяются природой поглощающих частиц. Спектр поглощения отдельного раствора строят в координатах А - лямбда (длина волны). При изменении концентрации раствора спектральная кривая будет сдвигаться по вертикали (рис.4, слева), но число максимумов на этой кривой и их положение в шкале длин волн не изменятся. Длину волны, при которой наблюдается максимальное поглощение, обозначают как лямбдаmax, а молярный коэффициент на этой длине волны – как εmax. Зависимость ε от лямбды (или lg ε от лямбды) характеризует все растворы данного состава. Она не меняется при изменении концентрации растворенного вещества или толщины поглощающего слоя. Именно такие «обобщенные» спектры поглощения индивидуальных веществ приводят в спектральных атласах (рис.4, справа).Чем больше εmax, тем меньшие концентрации Х можно определять по данной методике.
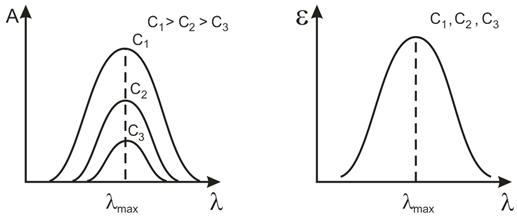
Рис.4.. Спектры поглощения растворов с разной концентрацией Х и их обобщение
Выбор аналитической длины волны. Если проба содержит только один компонент, поглощающий свет, то в качестве аналитической длины волны выбирают лямбдаmax, что обеспечивает максимальную чувствительность. Если же в растворе надо определять два и более компонента по отдельности, аналитические длины волн выбирают так, чтобы на каждой поглощал бы лишь один компонент. Это не всегда удается: в молекулярных спектрах полосы поглощения достаточно широки и часто накладываются друг на друга. В таких случаях селективность фотометрического анализа обеспечивают, проводя соответствующую пробоподготовку. Например, маскируют или заранее отделяют один из компонентов.
Аналитические возможности. Простота оборудования и самих фотометрических измерений сделали спектрофотометрию одним из самых распространенных методов анализа. Этот метод, в отличие от АЭС, не требует применения высоких температур, высокой квалификации исполнителей, его область применения не ограничена задачами элементного анализа. Сегодня фотометрическим методом аналитики решают задачи и элементного, и молекулярного, и вещественного, и структурно-группового анализа. Для идентификации веществ этот метод применяют редко; спектрофотометрия – это, прежде всего, способ количественного анализа. Нижняя граница определяемых концентраций обычно характеризуется значениями порядка 0,1 – 1,0 мкг/мл, что в большинстве случаев полностью удовлетворяет требованиям практики. Относительная погрешность результата анализа (при традиционном способе фотометрических измерений) составляет 2-5%, а в некоторых случаях может быть снижена до 1%.
Весьма важно, что определяемый компонент пробы можно заранее связать с подходящим реагентом в новое, интенсивно окрашенное соединение. Такой прием повышает селективность анализа, позволяет определять почти все элементы и множество их соединений. К недостаткам фотометрического анализа можно отнести лишь невысокую селективность и необходимость предварительного перевода пробы в раствор.
Фотометрический анализ широко применяют в контрольно-аналитических лабораториях на предприятиях химической, пищевой, нефтеперерабатывающей промышленности, в криминалистике, в сельском хозяйстве, в клиническом анализе и научных исследованиях. Данный метод важен для контроля за выбросами токсичных веществ и для мониторинга состояния окружающей среды.
По теории Эйнштейна, монохроматическая электромагнитная волна представляет собой поток частиц - квантов или фотонов. Каждый фотон всегда движется со скоростью света и несет квант энергии. При взаимодействии с веществом фотон передает свою энергию одному или нескольким электронам, после чего фотона больше не существует.
Фотон- это удивительная частица, которая обладает энергией, импульсом, но не обладает массой! Фотон "обречен" всегда летать со скоростью света.Свойства фотона:1) Не имеет состояния покоя.2) Безмассовая частица (m=0).3) Электрически нейтрален (q=0).4) Скорость его движения равна скорости света во всех инерциальных системах отсчета.5) Энергия фотона пропорциональна частоте соответствующего электромагнитного излучения (формула Планка).
6) Энергия фотона может быть выражена через длину волны: (единица измеренияэнергии фотона [Дж])
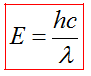

7) Модуль импульса фотона равен отношению его энергии к скорости:
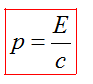
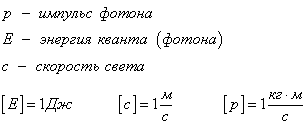
Длина волны — расстояние между двумя ближайшими друг к другу точками в пространстве, в которых колебания происходят в одинаковой фазе.
Длину волны можно также определить:как расстояние, измеренное в направлении распространения волны, между двумя точками в пространстве, в которых фаза колебательного процесса отличается на 2π;как путь, который проходит фронт волны за интервал времени, равный периоду колебательного процесса;как пространственный период волнового процесса: λ = с/ν[м]
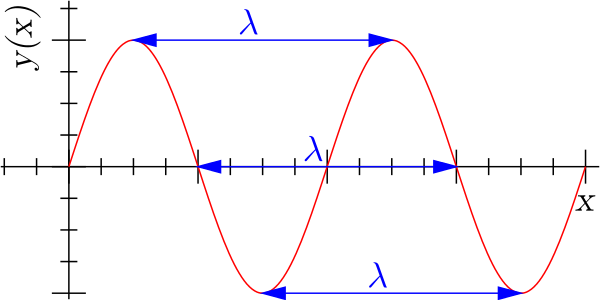
Представим себе волны, возникающие в воде от равномерно колеблющегося поплавка, и мысленно остановим время. Тогда длина волны — это расстояние между двумя соседними гребнями волны, измеренное в радиальном направлении. Размерность длины волны — метр.
Частота:электромагнитная волна характеризуется одним главным параметром — числом гребней, кот. за секунду проходят мимо нас (или поступают в детектор). Эту величину называют частотой излучения ν. Поскольку для всех электромагнитных волн скорость в вакууме одинакова, по частоте легко определить длину волны λ: λ = с/ν.
Мы просто делим путь, пройденный светом за секунду, на число колебаний за то же время и получаем длину одного колебания.
Единица измерения частоты: герц — производная единица, имеющая специальные наименование и обозначение. Через основные единицы СИ герц выражается следующим образом(1 Гц означает одно исполнение такого процесса за одну секунду, другими словами — одно колебание в секунду):1 Гц = 1 с−1
Волновое число — это величина, обратная длине волны, т. е. это число волн на отрезке 2π. Единица измерения — обратная длина, точнее рад*м-1. Обозначение - k, формула:
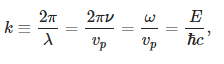
где: λ - длина волны,- ν (греч. буква «ню») - частота,- vp = vф - фазовая скорость волны,- ω - угловая частота,- E - энергия,- ħ – редуцированная постоянная Планка, (постоянная Дирака)- c – скорость света в вакууме (300 000 000 м/с (или 300 000 км/с)).
В спектроскопии волновое число измеряют в обратных сантиметрах (см-1).
43) Спектроскопические методы анализа. Основные типы взаимодействия в-ва с излучением: эмиссия (тепловая, люминесценция), поглощение, рассеяние. Классификация спектроскопических методов по природе частиц, взаимодействующих с излучением (атомные, молекулярные); по характеру процесса.
В атомной спектроскопии встречается либо эмиссия (свечение), либо абсорбция (поглощение), либо комбинация обоих эффектов (атомная флуоресценция).
Испускание света атомами и молекулами может быть спонтанным (самопроизвольным или вынужденным) Спонтанное испускание света (эмиссия) используется в методах эмиссионной спектроскопии. Эмиссия возникает за счёт перехода термически возбуждённых частиц в основное состояние с выделением кванта света: Спонтанное испускание света атомами - атомная эмиссия, лежит в основе методов атомно-эмиссионной спектроскопии, в частности, фотометрии пламени.
Вынужденное испускание света (люминесценция) используется в методах люминесцентной спектроскопии. Люминесценция возникает за счёт перехода частиц, возбуждённых от внешнего источника энергии (не термически!), в основное состояние с выделением кванта света (вынужденное испускание света молекулами). Явления, обусловленные волновой природой света, лежат в основе оптических методов анализа.
