Диффузия лекарственных препаратов в растворе
Диффузия – процесс, снижения разницы концентраций в растворе за счет спонтанного движения вещества по градиент химического потенциала (привычней градиента их концентрации).Представим простейший случай, когда раствор содержит только одно растворенное вещество. При растворении оно будет самопроизвольно двигаться из зоны с высокой концентрацией в зону с низкой.
Представьте раствор, разделенный на несколько объемов. Несмотря на это нет индивидуальной растворенной части в конкретном объеме показывающий предпочтения движений в любом конкретном направлении, определенная фракция молекул в этой части может считаться двигающейся в, скажем, Х направлении. Если концентрация в первой объемной части больше той что в второй части. Общий эффект в том, что большая часть частиц покидает первую часть переходя ко второй и, следовательно, есть поток растворенного вещества в Х направлении, убавляющую концентрацию. Экспрессия, которая относится к течению материла на концентрацию градиента (dc/dx) упоминается как первый закон Фикса
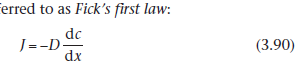
J - поток компонента через действующую плоскость и D - коэффициент диффузии. Отрицательный знак показывает поток убавляющий концентрацию. J в моль m-2 s-1, c в моль на м3 и Х в метрах, следовательно D единица м2 s-1
Отношения между радиусом диффундирующих молекул и их коэффициент диффузии полученный с помощью уравнения Энштейна-стокса
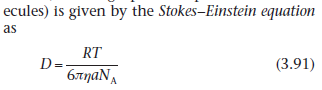
На коэффициент диффузии влияют:размера молекул (чем больше размер, тем ниже д),разветвление молекул,форма(большинство ассиметричных молекул имеет большее сопротивление текучести).
Диффузия через биологические мембраны.
Диффузионные свойства лекарств актуальны в фармацевтических системах в рассмотрении таких процессов как растворение лекарства и транспорт его через искусственную или биологическую мембрану.Диффузия в тканях, таких как кожа или опухоли, представляет собой процесс, который опирается на те же критерии, хотя диффузия происходит в сложных средах.
12. Стабильность лекарственных веществ. Химический распад лекарственных препаратов. Гидролиз. Окисление (приведите примеры данных реакций).
Химический распад лекарств приводит к потере их активности эффективности и безопасности, а также изменению внешних признаков ,уменьшению срока годности
используя повышения температур ускоряют распад ЛВ. Это используют в клинических испытаниях для экономии времени. (использованием уравнения Аррениуса.)
Химический распад лекарств
Распад лекарст приводит к потере активности . основные группы подвергающиеся этому: сложноэфирные
Гидролиз
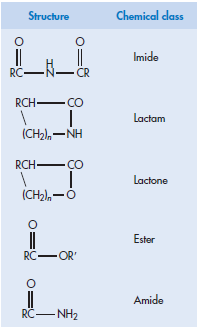
Если лекарство является производным карбоновой кислоты или содержит функциональную группуна основе этой молекулы, напримерсложный эфир, амид, лактон, лактам, имид или карбамат, когда мы имеем дело с лекарством, которое склонно подвергаться гидролитическому разложению. Пример: содержат сложноэфирные связи включая ацетилсалициловую кислоту(аспирин),физостигмин,метилдопа, тетракаин и прокаин.
Гидролиз сложного эфира обычно бимолекулярная реакция, включающая расщепление: остаток карбоновой кислоты- кислород. Например, гидролиз прокаина показан на схеме
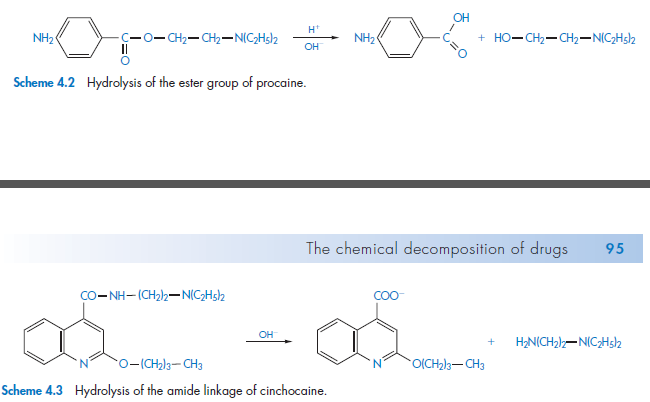
Гидролиз амидов включает расщепление амидного соединения как ,например, при распаде местного анестетика цинхокаина (схема 4.3).
Этот тип связи также находится в таких лекарствах,как хлорамфеникол, эргометрин и бензилпенициллиновые соли.
И наконец, как пример гидролиза лактамного кольца мы можем рассматривать разложение нитразепама и хлордиазепоксид. Другие лекарства, кроме бензодиазепинов, которые подвергаются гидролизу включают пенициллины и цефалоспорины.
