Различные способы выражения концентрации растворов и их взаимные пересчеты.
· Молярная концентрация
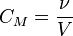 , где ν — количество растворённого вещества, моль;
, где ν — количество растворённого вещества, моль;
V — общий объём раствора, л.
· Моляльная концентрация
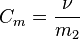 , где ν — количество растворённого вещества, моль;
, где ν — количество растворённого вещества, моль;
m2 — масса растворителя, кг.
· Нормальная концентрация
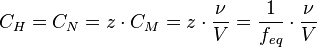
где ν — количество растворённого вещества, моль;
V — общий объём раствора, литров;
z — число эквивалентности (фактор эквивалентности f_{eq}=1/z).
· Титр
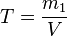 , гдеm1 — масса растворённого вещества, г;
, гдеm1 — масса растворённого вещества, г;
V — общий объём раствора, мл;
Растворы неэлектролитов.
Неэлектролиты-вещества, которые в растворенном или расплавленном состоянии не проводят электрический ток.
Осмос. Осмотическое давление. Закон Вант-Гоффа. Явление осмоса в природе. Давление насыщенного пара над раствором. Повышение температуры кипения растворов и понижение температуры кристаллизации. Законы Рауля.
Осмос–самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану при условии разности концентраций раствора по обе стороны мембраны.
Осмотическое давление–давление, которое нужно приложить к раствору во избежание проникновения растворителя в раствор.
Осмотическое давление p достаточно разбавленных коллоидных растворов может быть найдено по уравнению:
П=сRT=(Cm/Na)RT=CmkT илиП=СRT уравнение Вант-Гоффа
где V – объем частицы; М – масса одного моля растворенного вещества; с – массовая концентрация.
Если концентрацию растворённого вещества выразить как молярную
С = n/V (число молей растворённого вещества в единице объёма), тогда
Росм ∙V = n∙R∙T или
Pосм = m∙R∙T/M∙V,
R=8,314 Дж/моль∙К (универсальная газовая постоянная).
Это уравнение совпадает с уравнением идеального газа, уравнением Менделеева-Клайперона. Поэтому Вант - Гофф пришёл к выводу, что осмотическое давление равно тому давлению, которое оказывало бы растворённое вещество, если бы оно, находясь в газообразном состоянии при той же температуре, занимало тот же объём, что и раствор.
Законы Рауля. 1 закон: Давление насыщенных паров над раствором меньше, чем давление насыщенных паров над растворителем. Относительное понижение давления насыщенных паров растворителя нвд раствором прямо пропорционально мольной доли раствора при t=const.
(P0А-pА)/p0А=XBкомпонент А-растворитель
Парциальное давление насыщенного пара i-го компонента над раствором (pi) равно произведению давления насыщенного пара над чистым компонентом (p0i) на мольную долю (xi) этого компонента в растворе:
Pi=P0i*xi
Температура кипения жидкости – температура, при которой давление насыщенных паров жидкости становится равным атмосферному давлению.
2 закон: изменение температуры кипения и замерзания растворов прямо пропорционально моляльной концентрации раствора.
∆Tкип=ECmE-эбуллиоскопическая константа(Е(H2O)=0,52) ∆Tкип-разность между Tкип раствора и растворителя.
∆Tзам=KCmK-криоскопическая константа (K(H2O)=1,86)∆Tзам-разность между Tзам раствора и растворителя.
Роль осмоса в природе. У растений клетки используют осмос для увеличения объёма вакуоли. Благодаря этому растение становится более упругим.
Следует отметить роль осмоса в переносе питательных веществ в высоких стволах деревьев. Дело в том, что капиллярный перенос у высокорослых деревьев не способен выполнить функцию снабжения питанием.
Роль осмоса также важна для целых биологических систем. Иногда осмос имеет негативное влияние. Например, если в водоёме концентрация соли или других веществ в воде существенно изменится, то все обитатели такой экосистемы могут погибнуть из-за губительного фатального воздействия осмоса.
Растворыэлектролитов.
Электролиты-вещества, которые в растворенном или расплавленном состоянии проводят электрический ток.
Исходя из степени диссоциации все электролиты делятся на две группы:
Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как HCl, HBr, HI, HNO3, H2SO4 ).
Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты, такие как HF), основания p-, d- и f-элементов.
Электролитическая диссоциация. Особенности воды как растворителя. Зависимость диссоциации от характера химических связей в молекулах электролитов. Механизм процесса электролитической диссоциации. Характеристика поведения электролитов. Сила электролитов. Степень диссоциации. Константа диссоциации. Закон разбавления Оствальда. Кажущаяся степень диссоциации сильных электролитов. Понятие об активности и ионной силе растворов.
Электролитическая диссоциация – процесс распада на ионы.
Вода хорошо растворяет ионные и многие полярные соединения. Такое свойство воды связано в значительной мере с ее высокой диэлектрической проницаемостью (78,5).
Теория электролитической диссоциации. Зависимость направления диссоциации от характера химических связей в молекуле. Способность электролитов в растворах проводить электрический ток и их отклонения от законов Рауля и Вант-Гоффа объясняет теория электролитической диссоциации Аррениуса.
1. В растворах молекулы электролитов диссоциируют на положительно и отрицательно заряженные ионы. Раствор в целом электронейтрален. Благодаря наличию электрически заряженных частиц, через раствор электролитов проходит электрический ток.
2. Свойства ионов отличаются от свойств нейтральных атомов
3. Ионы движутся беспорядочно, но при пропускании электрического тока приходят в направленное движение. Положительно заряженные ионы движутся к катоду и называются катионами (металлы и водород); отрицательно заряженные ионы движутся к аноду и называются анионами (кислотные остатки и гидроксид ионы).
4. Объясняет отклонения растворов электролитов от законов Рауля и Вант-Гоффа. Это связано со способностью молекул элекиролитадиссоциировать на ионы. Понижение температуры кристаллизации и повышении температуры кипения зависит исклюсительно от числа растворённых частиц.
Однако теория Аррениуса не учитывала всей сложности явлений в растворах. В частности, она рассматривала ионы как свободные, независимые от молекул растворителя частицы. Этой теории противостояла химическая теория растворов Менделеева, в основе которой лежало представление о взаимодействии растворённого вещества с растворителем. В преодалении кажущегося противоречия обеих теорий большая заслуга принадлежит русскому учёному Каблукому, впервые высказавшему предположение о гидратации ионов. Развитие это идеи привело в дальнейшем к объединению этих теорий.
В зависимости от структуры растворяющегося вещества в безводном состоянии его диссоциация протекает по-разному. Наиболее типичны при этом два случая. Один из них это диссоциация растворяющихся солей, т.е. кристаллов с ионной связью в молекуле, второй - диссоциация при растворении кислот, т.е. веществ, состоящих из полярных молекул с ковалентной связью.
Когда кристалл соли попадает в воду происходит постепенное его растворение. Слой за слоем полярные молекулы воды, находящиеся в движении в результате соударений отделяют ионы от кристалл и переводят их в раствор. Иначе протекает диссоциация полярных молекул. Молекулы воды вызывают расхождение полюсов притянутой молекулы - поляризуют её. Такая поляризация в комбинации с колебательным тепловым движением атомов, а также с непрерывным тепловым движением окружающихеё молекул приводит к распаду полярной молекулы на ионы и они гидратируются. При этом ион водорода Н+ прочно связывается с молекулой воды и образует ион гидроксония Н3О+.
Диссоциации веществ как ионного, так и молекулярного строения способствует полярность молекул растворителя. Поэтому кроме воды, многие жидкости, состоящие из полярных молекул, являются ионизирующими растворителями.
Если теперь записать выражение для константы диссоциации HCN, то можно выразить Кд через Сα:
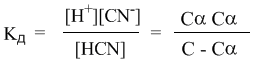
Концентрация недиссоциированных молекул [HCN] в равновесии должна быть меньше исходной концентрации С как раз на величину Сα – отсюда выражение (С – Сα) в знаменателе дроби. Если вынести концентрацию С за скобки и сократить, то получим следующее выражение:
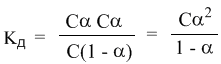
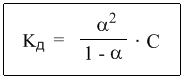 -закон разбавления Оствальда.
-закон разбавления Оствальда.
