Затвердевание бинарных жидких смесей. Диаграмма состояния системы с неограниченной растворимостью компонентов в жидком и твердом состоянии.
Простейший вид диаграмма состояния имеет в том случае, когда вещества обладают неограниченной растворимостью как в жидкой, так и в твердой фазе. Таким свойством обладают системы Cu-Ni ; Ag-Au; Вi-Sb и др. Диаграмма состояния таких сплавов (типа сигары) приведена на рис. 1, где по оси ординат нанесены температуры, а по оси абсцисс - концентрации. Линия аNKb называется линией ликвидуса, линия аМLb - линией солидуса. Выше линии ликвидуса имеется однородная жидкость. Ниже линии солидуса - однородный твердый раствор. Заштрихованная область является областью расслоенияна жидкую и твердую фазы. При построении кривой охлаждения сплава концентрации С видно, что она имеет две критические точки К и М (рис. 2), соответствующие началу и концу затвердевания соответственно.
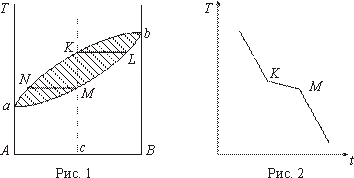
Изменение наклона кривых указывает на наличие температурного интервала, в котором происходит выделение теплоты кристаллизации, в отличие от чистого компонента, у которого выделение теплоты кристаллизации происходит при одной строго определенной температуре Такие диаграммы состояния служат для установления условий равновесия между твердыми и жидкими фазами. Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью) Диаграмма состояния и кривые охлаждения сплавов системы представлены на рис. 5.1.
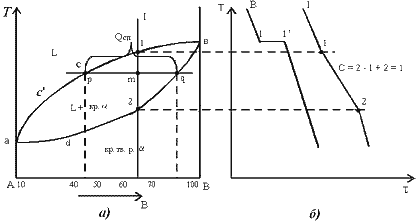 Рис.5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (а); кривые охлаждения типичных сплавов (б) Сначала получают термические кривые. Полученные точки переносят на диаграмму, соединив точки начала кристаллизации сплавов и точки конца кристаллизации, получают диаграмму состояния.Проведем анализ полученной диаграммы.1. Количество компонентов: К = 2 (компоненты А и В).2. Число фаз: f = 2 (жидкая фаза L, кристаллы твердого раствора
Рис.5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (а); кривые охлаждения типичных сплавов (б) Сначала получают термические кривые. Полученные точки переносят на диаграмму, соединив точки начала кристаллизации сплавов и точки конца кристаллизации, получают диаграмму состояния.Проведем анализ полученной диаграммы.1. Количество компонентов: К = 2 (компоненты А и В).2. Число фаз: f = 2 (жидкая фаза L, кристаллы твердого раствора 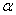 )3. Основные линии диаграммы:
)3. Основные линии диаграммы:
· acb – линия ликвидус, выше этой линии сплавы находятся в жидком состоянии;
· adb – линия солидус, ниже этой линии сплавы находятся в твердом состоянии.
4. Характерные сплавы системы: Чистые компоненты А и В кристаллизуются при постоянной температуре, кривая охлаждения компонента В представлена на рис. 5.1,б. Остальные сплавы кристаллизуются аналогично сплаву I, кривая охлаждения которого представлена на рис. 5.1, б. Процесс кристаллизации сплава I: до точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры кристаллизации твердого раствора 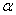 . На кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации. На участке 1–2 идет процесс кристаллизации, протекающий при понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз (жидкой и кристаллов твердого раствора
. На кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации. На участке 1–2 идет процесс кристаллизации, протекающий при понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз (жидкой и кристаллов твердого раствора 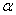 ) число степеней свободы будет равно единице
) число степеней свободы будет равно единице 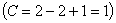 . При достижении температуры соответствующей точке 2, сплав затвердевает, при дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора
. При достижении температуры соответствующей точке 2, сплав затвердевает, при дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора 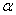 .
.
5. Количественный структурно-фазовый анализ сплава.
Пользуясь диаграммой состояния можно для любого сплава при любой температуре определить не только число фаз, но и их состав и количественное соотношение. Для этого используется правило отрезков. Для проведения количественного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы (ликвидус, солидус или оси компонентов).
а). Определение состава фаз в точке m:
Для его определения через точку m проводят горизонталь до пересечения с ближайшими линиями диаграммы: ликвидус и солидус.
Состав жидкой фазы определяется проекцией точки пересечения горизонтали с линией ликвидус p на ось концентрации.
Состав твердой фазы определяется проекцией точки пересечения горизонтали с линией солидус q (или осью компонента) на ось концентрации.
Состав жидкой фазы изменяется по линии ликвидуса, а состав твердой фазы – по линии солидуса.
С понижением температуры состав фаз изменяется в сторону уменьшения содержания компонента В.
б). Определение количественного соотношения жидкой и твердой фазы при заданной температуре (в точке m):
Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды.Рассмотрим проведенную через точку m коноду и ее отрезки.
Количество всего сплава (Qсп) определяется отрезком pq.
Отрезок, прилегающий к линии ликвидус pm, определяет количество твердой фазы. 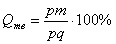
Отрезок, прилегающий к линии солидус (или к оси компонента) mq, определяет количество жидкой фазы. 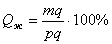
Компоненты этих сплавов неограниченно растворимы в жидком и твердом состояниях, не образуют химических соединений. В данном случае при затвердевании образуются однородные по структуре сплавы, состоящие из зерен - твердого раствора компонента В в А (или А в В). По этому типу диаграммы кристаллизуются сплавы Sb-Bi, Cu-Ni, Au-Ag, Fe-Ni и некоторые другие. Общий вид типовой диаграммы показан на рис.3.
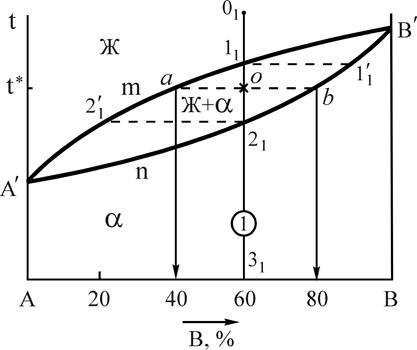 Рис.3. Диаграмма состояния системы А-В, с неограниченной растворимостью в твердом состоянии Рис.3. Диаграмма состояния системы А-В, с неограниченной растворимостью в твердом состоянии | Компоненты: А и В (К=2); фазы: Ж, a (твердый раствор) (Ф=2); линия А'nB' - линия солидус - геометрическое место точек критических температур конца процесса кристаллизации всех сплавов данной системы при охлаждении и начала плавления при нагреве; линия А'mB' - линия ликвидус, геометрическое место точек критических температур начала процесса кристаллизации всех сплавов данной системы при охлаждении и конца плавления при нагреве. |
По диаграмме этого типа кристаллизация всех сплавов протекает аналогично сплаву 1.
При кристаллизации сплава 1 (рис.4) от температуры 01 в нем происходят следующие превращения. До температуры точки 11, жидкий сплав охлаждается. При температуре точки 11, начинается процесс кристаллизации (зарождение центров кристаллизации). В интервале температур 11-21кристаллизуется из жидкого сплава a-твердый раствор, состав которого изменяется по линии солидус на участке 1¢1-21, состав жидкой фазы изменяется по линии 11-2¢1 (см.рис.4). В соответствии с диаграммой состояния во всем интервале температур 11-21 образуются кристаллы a-твердого раствора, более богатые тугоплавким элементом В, чем исходный сплав 1. Это приводит к неоднородности химического состава в пределах одного зерна (дендрита), так называемой дендритной ликвации, которая при реальных условиях охлаждения сохраняется в твердых растворах.
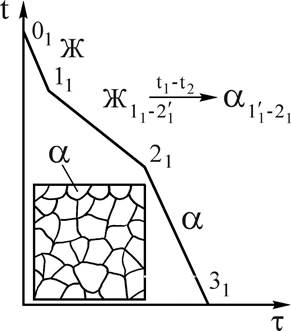 Рис.4. Кривая охлаждения и схема структуры сплава 1 при нормальной температуре. Рис.4. Кривая охлаждения и схема структуры сплава 1 при нормальной температуре. | Однако при очень медленном (равновесном) охлаждении состав сплава успевает выравниваться за счет диффузии и структура твердого раствора получается однородной (см. рис.4). В двухфазных областях и на линиях нонвариантных равновесий диаграмм двойных систем с помощью правила отрезков можно определить состав (концентрацию компонентов в фазах) и количественное соотношение фаз. Для того, чтобы определить концентрацию компонентов в фазах (их состав), через заданную точку, характеризующую состояние сплава, проводят горизонталь (коноду) до пересечения с линиями, ограничивающими данную область; проекции точек пересечения на ось концентраций показывают составы фаз. |
Определим составы фаз для сплава 1 при температуре t* (см. рис.3). Для этого, проводя при температуре t* горизонталь до пересечения с линиями, ограничивающими область А¢В¢А¢, получим точки пересечения "a" и "b". Проекция точки "а" на ось концентрации определяет состав жидкой фазы - 40%В и 60%А. Проекция точки "b" показывает состав твердой фазы - 80%В и 20%А.
Для того чтобы определить количественное соотношение фаз по правилу отрезков, необходимо через заданную точку провести горизонталь до пересечения с ближайшими линиями диаграммы состояния. Отрезки этой линии между заданной точкой и точками пересечения, определяющими составы фаз, обратно пропорциональны количествам этих фаз.
Рассмотрим их основные типы. Простейший вариант соответствует случаю, когда компоненты А и В образуют одну жидкую фазу (расплав или раствор), при охлаждении которой только выделяются (кристаллизуются) индивидуальные вещества (не образуются ни твердые растворы, ни химические соединения).
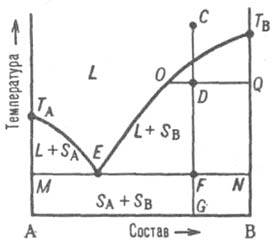 Рис. 2. Диаграмма плавкости двойной системы, компоненты которой А и В не образуют твердых растворов. L - область существования жидкости (расплава), (L + SA) и (L + SB) области сосуществования жидкой фазы и твердых А и В соответственно; (SA + SB) область существования механической смеси твердых А и В. ТАETВ и MEN - линии ликвидуса и солидуса соответственно, E - эвтектическая точка. С, D, F, G, О и Q - фигуративные точки (пояснения в тексте).
Рис. 2. Диаграмма плавкости двойной системы, компоненты которой А и В не образуют твердых растворов. L - область существования жидкости (расплава), (L + SA) и (L + SB) области сосуществования жидкой фазы и твердых А и В соответственно; (SA + SB) область существования механической смеси твердых А и В. ТАETВ и MEN - линии ликвидуса и солидуса соответственно, E - эвтектическая точка. С, D, F, G, О и Q - фигуративные точки (пояснения в тексте).
На диаграмме состояния (рис. 2) линия, изображающая зависимость от состава температуры начала выделения из жидкой фазы твердого компонента (начала равновесной кристаллизации), называется линией ликвидуса. Она состоит из двух ветвей ТАЕ и ТВЕ, отграничивающих фазовое поле жидкости L от полей сосуществования жидкой фазы с твердыми А и В соответственно (поля L + SA и L + SB). Линия, изображающая зависимость от состава температуры окончания равновесной кристаллизации при охлаждении (или начала плавления при нагревании), называется линией солидуса. Ниже нее расположено фазовое поле SA + SB твердого состояния системы, отвечающее условиям сосуществования двух твердых фаз.
Происходящие в системе фазовые изменения описываются следующим образом. При охлаждении жидкой фазы, например, из начального состоянияС, фигуративная точка системы в целом движется вниз вдоль прямой CG. В точке ее пересечения с линией ликвидуса начинается кристаллизация компонента В, система становится двухфазной и дивариантной или, поскольку давление фиксировано, условно моновариантной. По мерекристаллизации В жидкость обогащается компонентом А, ее состав изменяется по ветви ликвидуса и по достижении системой состояния, изображаемого, например, фигуративной точкой D, жидкой и твердой фазам соответствуют фигуративные точки О и Q. Прямые, соединяющие фигуративные точки двух находящихся в равновесии фаз, называются нодами (или коннодами); горизонтальные ноды, подобные OQ, можно провести через любые точки фазовых полей, отвечающих гетерогенным состояниям системы. При выражении состава в массовых (молярных) долях отношение отрезков OD и DQ пропорционально отношению масс (чисел молей) твердой и жидкой фаз (так называемое правило рычага). Оно позволяет рассчитать по диаграмме состояния относительные количества фаз при любой температуре, чтобы, например, определить полнотукристаллизации или степень извлечения данного компонента из жидкой фазы в твердую. В точке F пересечения прямой CG с линией солидуса начинается кристаллизация компонента А. Система становится трехфазной (жидкость и две твердые фазы А и В) и моновариантной (условно нонвариантной), т.е. при постоянном давлении совместная кристаллизация двух твердых фаз (так называемая эвтектическая кристаллизация) протекает при постоянных температуре и составе жидкой фазы, отвечающих координатам эвтектической точки Е.
После завершения эвтектической кристаллизации система состоит из двух твердых фаз и является дивариантной (условно моновариантной). В обсуждаемом случае система после затвердевания состоит из относительно крупных кристаллов В и мелкодисперсной смеси совместно возникших при эвтектической кристаллизации кристаллов А и В; такую смесь называют эвтектикой. Если исходная жидкость имела эвтектический состав, продукт ее затвердевания - мелкодисперсная эвтектика без примеси крупных кристаллов какого-либо из компонентов. При нагревании смеси твердых А и В описанные явления протекают в обратной последовательности: изотермическое образование жидкости эвтектического состава вплоть до исчерпания какого-либо из твердых компонентов и растворение в жидкости оставшегося твердого компонента при дальнейшем повышении температуры, которое завершается по достижении фигуративной точкой системы линии ликвидуса
