Строительные материалы. коррозия бетона
В строительстве широко используются вяжущие материалы, стекло, керамика, пластмассы.
Вяжущими материаламиназывают тонкодисперсные порошкообразные вещества или композиции веществ, образующие при взаимодействии с жидкостями полимерные твердые материалы. По химической природе вяжущие материалы могут быть органическими и неорганическими веществами. В качестве жидкости для неорганических вяжущих материалов обычно используют воду. К неорганическим вяжущим материалам относят алебастр, известь, цемент.
Алебастр, или жженый гипс, получают при частичном обезвоживании природного гипса CaSO4∙2H2O, при этом гипс переходит в алебастр CaSO4∙0,5H2O.
При замешивании с водой алебастр образует жидкое тесто, которое быстро затвердевает, снова превращаясь в CaSO4∙2H2O. Алебастр применяется для штукатурки стен и потолков, для производства гипсокартона.
Смесь гашеной извести Са(ОН)2 с песком и водой называется известковым раствором и используется для скрепления кирпичей при кладке стен. Затвердевание известкового раствора происходит сначала из-за испарения воды, а затем в результате поглощения диоксида углерода из воздуха и образования СаСО3:
Са(ОН)2+СО2 → СаСО3+Н2О
Гашеную известь применяют также в качестве штукатурки.
При производстве строительных работ в огромных количествах используется цемент. Химический состав цементов обычно выражают в процентах содержащихся в них оксидов, главными из которых являются СаО, Al2O3, SiO2 и Fe2O3.
Обычный цемент (силикатцемент, или портландцемент) получают путём обжига цементной смеси, в состав которой входят глина и известняк. При обжиге этой цементной смеси карбонат кальция разлагается на диоксид углерода и оксид кальция; СаО вступает во взаимодействие с глиной, в результате чего образуются силикаты и алюминаты кальция. Цементная смесь обычно приготавливается искусственно, но возможно использование и природных материалов – известково-глинистых пород (мергелей), которые по составу соответствуют цементной смеси. При обжиге до спекания мергеля или специально подготовленной сырьевой смеси, состоящей из 75-78 % известняка и 22-25 % глины, получают клинкер. Химический состав клинкера следующий: 60 - 64 % СаО, 19 - 24 % SiO2, 4 - 8 % Al2O3, 2 - 6 % Fe2O3. Продуктом тонкого помола клинкера является портландцемент.
При замешивании цемента с водой образуется тестообразная масса, которая через непродолжительное время затвердевает. Данный переход из тестообразного состояния в твёрдое называется «схватывание». При затвердении цемента образуется цементный камень, состоящий в основном из силиката кальция, который уплотнён длинными игольчатыми кристаллами гидроксида кальция.
При употреблении цемента в качестве вяжущего материала его обычно смешивают с песком и водой; полученную смесь называют цементным раствором.
При смешивании цементного раствора с гравием или щебнем получают важнейший строительный материал – бетон; сооружения из бетона с основой из стальных балок или стержней называются железобетонными.
Из портландцемента и тонковолокнистого минерала – асбеста – изготавливают асбестоцементные изделия, в т.ч. асбестоцементные трубы, применяемые в водопроводных и мелиоративных системах.
Кроме силикатцемента выпускаются и другие виды цементов, в частности глиноземистый , кислотоупорный и магнезиальный.
Глиноземистый цемент получают сплавлением тонко размолотой смеси боксита (природного оксида алюминия) с известняком. Этот цемент содержит больше Al2O3 по сравнению с силикатцементом (~ 30 %), тогда как содержание SiO2 и СаО в глиноземистом цементе ниже – 5 - 16 % SiO2 и 35 - 40 % СаО. Основными соединениями глиноземистого цемента являются алюминаты кальция. Этот цемент затвердевает гораздо быстрее, чем силикатный, и лучше противостоит действию морской воды, но стоит гораздо дороже силикатцемента, поэтому применяется в строительстве лишь в специальных случаях.
Кислотоупорный цемент представляет собой смесь тонко размолотого кварцевого песка с кремнеземистым веществом, обладающим высокоразвитой поверхностью. После смешивания этой смеси с раствором силиката натрия получается пластичное тесто, превращающееся в прочную массу, противостоящую всем кислотам, кроме фтороводорода HF. Кислотоупорный цемент применяется в качестве вяжущего вещества при футеровке химической аппаратуры кислотоупорными плитками.
Магнезиальный цемент (цемент Сореля) получается при замешивании прокаленного оксида магния с 30 %- водным раствором хлорида магния. Такая смесь при затвердевании превращается в плотную белую, легко полирующуюся массу. Магнезиальный цемент в качестве вяжущего материала применяется при изготовлении мельничных жерновов, точильных камней и т. п.
Широкое применение получили вяжущие материалы на основе различных материалов (цинка, магния, алюминия, хрома) и ортофосфорной кислоты, отличающиеся жаропрочностью и жаростойкостью. На основе этих материалов разработаны антикоррозионные, огнезащитные покрытия и краски, жаростойкие бетоны, керамические огнеупорные, теплоизоляционные и конструкционные материалы.
Органические вяжущие вещества представляют собой природные или искусственные твёрдые, вязкопластичные и жидкие материалы, являющиеся высокомолекулярными соединениями и обладающие вяжущими свойствами. К ним относятся битумы, дегти, полимеры и их модификации.
Битумы – органические вещества чёрного или тёмно коричневого цвета, состоящие из смеси углеводородов с молекулярной массой 400-500 а.е.м. и их неметаллических производных с серой, азотом или кислородом. Битумы могут быть природными и искусственными. Природные битумы образовались из нефти в верхних слоях земной коры или в виде поверхностных озёр, и встречаются в виде отдельных скоплений, а чаще они пропитывают осадочные горные породы. Искусственные битумы получают путём переработки отдельных фракций нефти (мазута, гудрона). В состав битума входят масла (35-60 %), смолы (20-40 %), асфальтены (10-40 %).
Полимерами называют высокомолекулярные соединения, макромолекулы которых построены из многократно повторяющихся структурных звеньев, соединенных ковалентными связями. Широкое распространение получили искусственные полимеры, синтезируемые из простых низкомолекулярных соединений – мономеров.
По составу основной цепи макромолекул органические полимеры подразделяются на три класса:
1. Карбоцепные полимеры, основные цепи которых построены только из атомов углерода (полиэтилен, полипропилен, полиизобутилен, полибутадиен и т.п.).
2. Гетероцепные полимеры, в основных цепях которых кроме атомов углерода содержатся атомы кислорода, азота, серы и других элементов (полиэфиры, полиамиды, полиуретаны, полиэпоксидные соединения).
3. Элементоорганические полимеры, содержащие в основных цепях атомы Si, Al, Ti и других элементов (кремнийорганические соединения с кремний - кислородными связями, называемыми силоксановыми).
Исходными веществами для синтеза полимеров являются низкомолекулярные соединения, получаемые из нефти, угля, газа – мономеры. Полимеры получают методами полимеризации и поликонденсации. Полимеризацией называют процесс соединения молекул мономера за счет разрыва ненасыщенных (двойных) связей. Процесс полимеризации не сопровождается образованием побочных продуктов реакции. Если в полимеризации участвуют два или более вида мономера, то такую реакцию называют сополимеризацией, а продукт реакции – сополимером.
При помощи реакции полимеризации получают полимеры, называемые полимеризационными смолами – полиэтилен ( – СН2 – СН2 – )n, полипропилен ( – СН2 – СНСН3 – )n, полиизобутилен ( – СН2 – С(СН3)2 – )n, поливинилхлорид ( – СН2 – СНCl – )n, полистирол ( – СН2 – СН – С6Н5 – )n, поливинилацетат ( – СН2 – СНCООСН3 – )n, полиметилметакрилат ( – СН2 – ССН3CООСН3 – )n, синтетические каучуки.
Поликонденсацией называют процесс образования полимера из мономеров, содержащих две или несколько функциональных групп, сопровождающийся образованием наряду с макромолекулой полимера побочных низкомолекулярных продуктов – воды, HCl, NH3 и др. В результате поликонденсации образуется полимер, элементарное звено которого отличается от состава исходного мономера. К важнейшим поликонденсационным полимерам, используемым в строительстве, относятся фенолформальдегидные, карбамидные, полиэфирные, полиамидные, эпоксидные, полиуретановые, фурановые, кремнийорганические и другие полимеры.
В качестве вяжущих веществ при производстве полимербетонов и стеклопластиков используются следующие полимеры: бутадиен- стирольный каучук, полиэфиракрилатные, эпоксидные и фурановые полимеры, а фенолформальдегидные, полиэфирные, полиамидные и полиуретановые полимеры используют для изготовления лаков, эмалей, пленок и клеев.
Стекломназывают прозрачные аморфные сплавы, полученные путём переохлаждения расплава смеси многих силикатов с другими силикатами или с диоксидом кремния.
По структуре стекла представляют собой переохлажденные системы, обладающие механическими свойствами твёрдых тел. Для получения стекол с определёнными свойствами используют различные исходные материалы и разные технологические процессы. Кроме SiO2 в состав стекол могут входить многие оксиды: Li2O, K2O, Na2O, BeO, MgO, CaO, SrO, CdO, PbO, Al2O3, Fe2O3, B2O3.
Обычное оконное стекло, а также стекло, из которого изготавливается большая часть стеклянной посуды, состоит из силикатов натрия и кальция, сплавленных с SiO2.Состав такого стекла выражается формулой Na2O∙CaO∙6SiO2, а исходными материалами для его получения служат белый песок SiO2, сода Na2СO3 и известняк или мел CaСO3. Если соду заменить поташем К2СO3, то получается тугоплавкое стекло, а если кроме поташа добавить оксид свинца, то получится тяжёлое стекло (хрусталь); а при добавлении борного ангидрида B2O3 увеличивается твердость стекла и стойкость к химическим воздействиям.
Существует также кварцевое стекло, приготавливаемое непосредственно из расплавленного кварца.
В строительстве применяется препарат, называемый жидким стеклом. Этот препарат представляет собой водный раствор так называемого растворимого стекла- силикатов натрия и калия Na2SiO3 и К2SiO3, которые благодаря внешнему сходству со стеклом и растворимости в воде и получили такое название. Таким образом, жидкое стекло на самом деле не относится к стеклу. Жидкое стекло применяется для изготовления кислотоупорного цемента и бетона, для химического укрепления слабых грунтов и др.
При вытягивании расплавленного стекла через мелкие отверстия (фильеры) получают стеклянное волокно – нити диаметром 2-10 мкм. Стеклянное волокно очень прочное, нехрупкое, негорючее, обладает тепло-, электро-, звукоизолирующими свойствами и химической стойкостью, что вместе с доступностью и дешевизной основного сырья и сравнительной простотой производства волокна позволяет его широко использовать.
При сочетании в одном материале стеклянного волокна и синтетических смол получают новые конструкционные материалы - стеклопластики. Они в 3-4 раза легче стали, но не уступают ей по прочности; или можно заменять и металл, и дерево.
Керамикойназывают материалы и изделия, изготавливаемые из огнеупорных веществ (глины, карбидов, оксидов некоторых металлов). Керамика – это поликристаллические материалы, получаемые спеканием неметаллических порошков природного или искусственного происхождения.
В зависимости от применения различают строительную, огнеупорную, химически стойкую, бытовую и техническую керамику.
К строительной (конструкционной) керамике относятся материалы, которые служат для создания механически прочных конструкций и сооружений (кирпич, черепица, трубы, облицовочная плитка). Остальные виды керамики относятся к функциональной керамике, изделия из которой обладают особыми электрическими, магнитными, оптическими, термическими и т. п. свойствами.
Процесс изготовления керамических изделий включает приготовление керамической массы, формование, сушку и обжиг. При обжиге происходит спекание, обусловленное химическими реакциями в твёрдой фазе, в результате чего получается материал с заданными свойствами. В зависимости от природы исходных материалов и требований, предъявляемых к конечному продукту, все операции проводятся в соответствии с технологией по строго определённому режиму.
Некоторые керамические изделия покрывают глазурью – тонким слоем стекловидного материала, в результате чего керамика становится водонепроницаемой и приобретает некоторые новые свойства.
Пластмассы(пластические массы, полимерные композиты) – композиционные материалы на основе высокомолекулярных соединений, способные под влиянием нагревания и давления приобретать нужную форму (формироваться), а затем устойчиво сохранять приданную им форму.
Кроме высокомолекулярных соединений пластмассы содержат и другие вещества: наполнители, пластификаторы, стабилизаторы, отвердители, красители и другие добавки. Наибольшая доля в составе пластмасс приходится на наполнители. Наполнители предназначены для придания необходимых эксплутационных свойств материалу и для понижения его себестоимости. В качестве наполнителей используются порошкообразные вещества ( сажа, древесная мука, кварцевая мука и др.), волокнистые материалы (хлопковые очесы, асбестовое волокно и др.), листовые материалы (бумага, хлопчатобумажная ткань, стеклоткань и др.).
Пластификаторы – низкомолекулярные малолетучие жидкие, смолообразные или твердые вещества, хорошо растворимые в полимере. При пластификации полимеров происходит снижение температуры стеклования полимера (повышение морозостойкости), повышение эластичности, пластичности и т. д. Для каждой пары полимер – пластификатор существует определённое оптимальное соотношение, позволяющее получить материал с требуемыми характеристиками. Обычно дозировка пластификатора не превышает 30 %. В качестве пластификаторов используют фталаты, фосфаты, камфору и др.
Стабилизаторы – вещества, вводимые в полимер для предотвращения деструкции или структурирования в процессе эксплуатации материала. Количество стабилизатора – 2-3 % от массы полимера. Стабилизаторами являются различные ароматические амины и фенолы, фосфаты, фосфиты, сульфиды, меркаптаны и др.
Отвердители – химические вещества, с помощью которых происходит отверждение мономеров и олигомеров при производстве полимеров. В зависимости от химической природы олигомеров используют различные вещества для их отверждения.
Модификаторы – вещества, которые направленно изменяют свойства полимеров, в результате чего образуются полимеры другого свойства, с новыми свойствами. Модификаторы бывают как неорганическими (хлор, кислоты), так и органическими веществами (битумы, растительные масла, канифоль, полиэфиры, полиамиды и др.)
По химической стойкости пластмассы превосходят металлы – они устойчивы к действию воды, растворов кислот и щелочей.
Пластмассы в основном называют по типу наполнителя.
В настоящее время широко применяются армированные пластики, в которых в качестве наполнителя используются различные волокна, несущие основную механическую нагрузку. В органопластиках связующим являются синтетические смолы, а наполнителем – органические полимерные волокна.
В стеклопластиках армирующим компонентом является стекловолокно, придающие стеклопластикам особую прочность и легкость. Из стеклопластиков изготавливают трубы, выдерживающие большое гидравлическое давление и не подвергающееся коррозии.
К числу недостатков полимерных материалов относится их горючесть – они легко возгораются, при горении выделяют много ядовитых веществ. Поэтому в пластмассы в качестве наполнителей вводят специальные добавки, препятствующие их горению – либо инертные наполнители, либо наполнители, разлагающиеся с поглощением тепла (например, гидроксид алюминия), либо ингибиторы процесса горения – антипирены (фосфаты, бура, борная кислота и др.).
В результате воздействия внешней среды на бетон происходит его разрушение – коррозия. Существует три вида разрушения бетона: 1) растворение и выщелачивание составных частей бетона за счёт обменных реакций, сопровождающихся образованием растворимых соединений; 2) образование в бетоне в результате реакций обмена рыхлых осадков, не обладающих вяжущими свойствами и способных вымываться во внешнюю среду; 3) образование труднорастворимых соединений, объём которых значительно превышает объём составных частей бетона, в результате чего бетон растрескивается и разрушается. Скорость процесса коррозии и его интенсивность зависят как от состава и качества бетона, так и от особенностей внешней среды (химического состава, солесодержания воды, условий фильтрации воды и т. д.)
Химическое разрушение бетона может быть вызвано несколькими причинами – агрессивным действием сильных кислот и щелочей, СО2, газов, аммиачных и фосфорных удобрений, сульфатов, а также воздействием пресной воды и наличием биологической коррозии.
Кислотная коррозия наблюдается при действии на бетон растворов кислот. Свободные кислоты присутствуют в сточных водах некоторых промышленных предприятий. Реагируя с Са(ОН)2, являющимся основой цементного камня, кислоты приводят к образованию гипса либо растворимых солей:
H2SO4+ Ca(OH)2 → CaSO4+2H2O
2HCl+ Ca(OH)2 → CaCl2+2H2O
Сильные кислоты взаимодействуют также с труднорастворимыми соединениями, входящими в состав бетона (гидросиликатами, карбонатом кальция). В зависимости от растворимости образующихся в результате реакции солей в одних случаях будет наблюдаться быстрое разрушение бетона, в других- медленное. Возможно и уплотнение бетона за счёт образования труднорастворимых осадков – фосфатов и оксалатов кальция (солей фосфорной и щавелевой кислот). Если величина рН воды, контактирующей с бетоном, ниже 5-6, то применяют кислотостойкие бетоны или защитные покрытия.
Углекислотная коррозия проявляется при нарушении карбонатного равновесия
СаСО3+СО2+Н2О = Са(НСО3)2
в присутствии агрессивной угольной кислоты.
Равновесная угольная кислота не является агрессивной по отношению к бетону, и наряду с ионами НСО3- способствует образованию защитной пленки на поверхности бетона. Избыточная (агрессивная) углекислота разрушает этот защитный слой, превращая СаСО3 в гидрокарбонат Са(НСО3)2, хорошо растворимый в воде. Предельно допустимые концентрации агрессивной угольной кислоты СО2 в воде, контактирующей с бетоном, составляют с учетом различных факторов 3-8,3 мг/л. Более устойчивы к углекислотной коррозии бетоны, имеющие высокую плотность.
Выщелачивающая коррозия наблюдается при воздействии на бетон пресной воды, растворяющей Са(ОН)2. Гидроксид кальция сравнительно хорошо растворим в воде – его растворимость составляет 1,3 г/л. При воздействии на бетон безнапорной воды происходит её просачивание в тело бетона и его разрушение на небольшие глубины, но если бетонные сооружения подвергаются воздействию напорной воды (плотины, перемычки, шлюзы), то вода начинает фильтроваться через бетон и в большом количестве вымывает из цементного камня Са(ОН)2, а затем и другие соединения. В таких случаях целесообразно использовать портландцемент с активными гидравлическими добавками, которые при твердении цемента химическим путём связывают Са(ОН)2 в нерастворимые в воде соединения (например, в гидросиликаты кальция), либо применять модифицирующие добавки, понижающие фильтрационную проницаемость бетона. Процесс выщелачивания можно замедлить карбонизацией (выдерживанием бетонных изделий на воздухе), при которой в поверхностных слоях бетона в результате взаимодействия Са(ОН)2 с СО2,содержащимся в воздухе, образуется СаСО3.
Магнезиальная коррозия наблюдается при воздействии на бетон минерализованных вод, содержащих соли магния. При этом происходит замещение ионов Са2+ в бетоне ионами Mg2+ из воды:
Са(ОН)2+MgCl2→CaCl2+Mg(OH)2
В результате реакции в цементном камне образуется CaCl2, хорошо растворимый в воде, и Mg(OH)2, образующий рыхлый осадок, не обладающий вяжущими свойствами и вымываемый из бетона.
Сульфатная коррозия бетона происходит при значительном содержании в воде ионов SO42-. Эта разновидность коррозии проявляется в образовании новых соединений, обладающих значительным объёмом и способствующих образованию трещин. К числу таких соединений относится гидросульфоалюминат кальция (эттрингит), называемый также бетонной или цементной бациллой - 3CaO∙Al2O3∙3СаSO4∙31Н2О.
Процесс образования гидросульфоалюмината кальция из содержащегося в бетоне трёхкальциевого алюмината описывается уравнением:
3CaO∙Al2O3∙6Н2О+3СаSO4+6Н2О → 3CaO∙Al2O3∙3СаSO4∙31Н2О
Реакция сопровождается увеличением объёма в 2,5 раза, что приводит к растрескиванию бетона. Гидросульфоалюминат кальция представляет собой кристаллы в виде тонких игл, иногда собранных вместе наподобие звёздочек. Под действием NaCl, содержащегося в морской или грунтовой воде, игольчатые кристаллы постепенно разрушаются, превращаясь в слизистую массу, в результате чего бетон полностью разрушается.
При повышенном содержании в воде магния сульфатная коррозия бетона усиливается. Сульфат магния взаимодействует с известью с образованием рыхлого осадка Mg(OH)2 и гипса:
Са(ОН)2+MgSO4+2Н2О→ Mg(OH)2 +СаSO4∙2Н2О
Гипс приводит к растрескиванию бетона из-за увеличения объёма. Этот комбинированный вид коррозии бетона проявляется в морской воде.
Для уменьшения сульфатной коррозии бетона при его изготовлении применяют сульфатостойкий портландцемент, либо применяют бетоны с повышенной плотностью.
Коррозия бетона сильными щелочами (NaОН, КОН). Щелочи разрушают бетон в меньшей степени, чем кислоты и минерализованные воды. Вода с высоким содержанием щелочи оказывает разрушающее воздействие на все цементы, т.к. некоторые составляющие на основе глинозёма подвергаться сольватации. Щёлочи, содержащиеся в воде, взаимодействуют с СО2, содержащимся в воздухе:
2NaОН+ СО2→Na2СО3+ Н2О
Образующийся карбонат натрия Na2СО3∙ 10Н2О кристаллизуется в порах бетона, давит на его стенки и расшатывает структуру. Поэтому не рекомендуется допускать контакт воды с обычными цементами при рН>12, или с глиноземистыми цементами при рН>8,5 при отсутствии защитных покрытий.
Коррозия железобетона в газовой среде зависит от ряда факторов: состава и концентрации газов, температуры, влажности и т.д. Углекислый газ и фтороводород образует с Са(ОН)2 малорастворимые соли и практически не снижают прочность бетона, но вызывают коррозию стальной арматуры; серный и сернистый ангидрид и Н2S вызывают сульфатную коррозию бетона, а хлор и хлороводород агрессивны к стальной арматуре. Для предотвращения коррозии от газов необходимо применять бетоны низкой проницаемости, вводить защитные покрытия.
Разрушение бетона под действием минеральных удобрений. Аммиачные удобрения – аммиачная селитра и сульфат аммония – реагируют с Са(ОН)2:
Са(ОН)2+2NH4NO3 +2Н2О→Ca (NO3)2∙4 Н2О+2 NH3
Гидронитрат кальция Ca (NO3)2∙4 Н2О хорошо растворяется в воде. Коррозию бетона также вызывает суперфосфат, состоящий из Са(Н2РО4)2, гипса и фосфорной кислоты.
Биологическая коррозия возникает при взаимодействии цементного камня с кислыми продуктами метаболизма живых организмов – различными кислотами.
Наиболее часто встречается бактериальная коррозия бетона, обусловленное образованием Н2S и Н2SО4 в канализационных коллекторах в анаэробных условиях (при недостатке кислорода).
Для повышения стойкости бетонов к коррозии обычно рекомендуется правильно выбирать цемент в зависимости от условий эксплуатации бетонных и железобетонных конструкций. Изготовление бетонов повышенной плотности (с добавлением поверхностно- активных веществ) делает их менее проницаемыми для агрессивной среды, а использование пластифицирующих и гидрофобизирующих добавок в бетонных смесях способствует замедлению процессов коррозии.
Пример.
Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 140 мг/л гидрокарбонат-иона НСО3ˉ и 28 мг/л свободной углекислоты.
Решение. Гидрокарбонаты, содержащиеся в данной воде, состоят наполовину из связанной и полусвязанной угольной кислоты, так как при разложении гидрокарбонаты дают карбонаты (связанную) и свободную угольную кислоту (полусвязанную):
2НСО3‾ 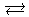 СО2 + СО32‾ + Н2О
СО2 + СО32‾ + Н2О
В воде, содержащей свободную углекислоту и гидрокарбонаты, количество связанной угольной кислоты равно содержанию полусвязанной. Следовательно, в данной воде содержание полусвязанной угольной кислоты составит:
140 : 2 – 70 мг/л.
Сумма свободной и полусвязанной угольной кислоты (s) будет равна:
28 + 70 = 98 мг/л.
По табл. 5 Приложения находим, что этому значению s соответствует значение g (сумма полусвязанной и агрессивной углекислоты), равное 83,3 мг/л. Вычитая содержание полусвязанной кислоты, получим содержание агрессивной угольной кислоты: 83,3 – 70 = 13,3 мг/л.
Поскольку максимальное значение агрессивной углекислоты в зависимости от разных факторов не должно превышать 3-8,3 мг/л, а данная вода содержит 13,3 мг/л, то можно сделать вывод, что эта вода будет разрушать бетон.
Вопросы и задачи
276. Перечислите основные виды вяжущих материалов и приведите примеры. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 210 мг/л НСО3ˉ и 24 мг/л свободной углекислоты.
277. Перечислите основные виды цементов. Чем они различаются? Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 126 мг/л НСО3ˉ и 20 мг/л свободной углекислоты.
278. Что такое стекло? Приведите примеры разных видов стекла и укажите, чем они различаются. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 184 мг/л НСО3ˉ и 17 мг/л свободной углекислоты.
279. Что такое жидкое стекло? Где оно применяется? Напишите уравнение получения жидкого стекла. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 108 мг/л НСО3ˉ и 22 мг/л свободной углекислоты.
280. Что такое керамика? Перечислите основные виды керамики и приведите примеры. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 98 мг/л НСО3ˉ и 18 мг/л свободной углекислоты.
281. Что такое пластмассы? Из чего они состоят? Приведите примеры пластмасс. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 200 мг/л НСО3ˉ и 21 мг/л свободной углекислоты.
282. Что такое термопластичные полимеры? Перечислите их свойства и приведите примеры. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 220 мг/л НСО3ˉ и 25 мг/л свободной углекислоты.
283. Что такое термореактивные полимеры? Перечислите их свойства и приведите примеры. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 116 мг/л НСО3ˉ и 20 мг/л свободной углекислоты.
284. Что такое армированные пластики? Перечислите их свойства и приведите примеры. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 56 мг/л НСО3ˉ и 16 мг/л свободной углекислоты.
285. Перечислите основные виды коррозии бетона. В чем причина разрушения бетона при этих видах коррозии? Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 116 мг/л НСО3ˉ и 6 мг/л свободной углекислоты.
286. Какой вид коррозии протекает в морской воде? Напишите уравнения протекающих при этом реакций. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 158 мг/л НСО3ˉ и 28 мг/л свободной углекислоты.
287. Как можно предотвратить коррозию бетона? Ответ подтвердите соответствующими примерами. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 162 мг/л НСО3ˉ и 14 мг/л свободной углекислоты.
288. Какие виды коррозии протекают при воздействии на бетон минерализованных вод? Ответ подтвердите уравнениями соответствующих реакций. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 108 мг/л НСО3ˉ и 27 мг/л свободной углекислоты.
289. Какие виды коррозии бетона могут проявляться при использовании воды в сельском хозяйстве? Ответ мотивируйте. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 138 мг/л НСО3ˉ и 8 мг/л свободной углекислоты.
290. Какие виды коррозии бетона сопровождаются образованием рыхлых осадков, не обладающих вяжущими свойствами? Ответ подтвердите уравнениями соответствующих реакций. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 112 мг/л НСО3ˉ и 35 мг/л свободной углекислоты.
291. Какие виды коррозии бетона вызваны образованием соединений, вызывающих растрескивание бетона? Приведите химические формулы этих веществ и уравнения их образования. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 174 мг/л НСО3ˉ и 11 мг/л свободной углекислоты.
292. Какие виды коррозии бетона обусловлены образованием растворимых соединений? Ответ подтвердите примерами этих соединений и уравнениями их образования. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 110 мг/л НСО3ˉ и 23 мг/л свободной углекислоты.
293. Какие вещества препятствуют коррозии бетона? Ответ подтвердите примерами. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 145 мг/л НСО3ˉ и 27 мг/л свободной углекислоты.
294. Какие виды коррозии бетона могут наблюдаться при действии на бетон сточных вод промышленных предприятий? Ответ подтвердите уравнениями соответствующих реакций. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 224 мг/л НСО3ˉ и 31 мг/л свободной углекислоты.
295. Перечислите основные виды поликонденсационных полимеров. Какое применение эти полимеры находят в строительстве? Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 146 мг/л НСО3ˉ и 33 мг/л свободной углекислоты.
296. Перечислите основные виды полимеризационных смол. Какое применение эти полимеры находят в строительстве? Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 188 мг/л НСО3ˉ и 12 мг/л свободной углекислоты.
297. Напишите уравнения получения основных поликонденсационных полимеров. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 128 мг/л НСО3ˉ и 18 мг/л свободной углекислоты.
298. Напишите уравнения получения основных полимеризационных смол. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 95 мг/л НСО3ˉ и 20 мг/л свободной углекислоты.
299. Приведите химические формулы основных видов синтетического каучука. Какое применение каучуки находят в строительстве? Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 68 мг/л НСО3ˉ и 23 мг/л свободной углекислоты.
300. Перечислите неорганические вяжущие материалы и напишите уравнения их получения. Определите, будет ли вода проявлять агрессивность по отношению к бетону, если в воде содержится 166 мг/л НСО3ˉ и 15 мг/л свободной углекислоты.
Варианты индивидуальных заданий
для студентов специальностей 280401 и 280402
| № вариан-та | Номера заданий | |||||||||||
| Номера тем | ||||||||||||
Наши рекомендации
|
