ОСНОВЫ ИДЕНТИФИКАЦИИ НЕОРГАНИЧЕСКИХ Соединений
Идентификация – это отождествление, установление совпадения чего-либо с чем либо. В применении к химии идентификация - установление химического состава неорганических веществ.
Вопросами идентификации соединений занимается аналитическая химия - область химии, изучающая качественный и количественный состав веществ.
При помощи качественного анализа находят, из каких химических элементов, ионов, групп атомов и молекул состоит анализируемое вещество. Количественный анализ позволяет установить количественные соотношения составных частей данного соединения или смеси веществ. При исследовании состава неизвестного вещества (идентификации) качественный анализ всегда предшествует количественному анализу.
Методы анализа условно делят на 3 группы:
1) Химические – основаны на использовании химических реакций, протекающих в растворах. В результате химических превращений образуются новые соединения, обладающие специфическими свойствами: определенным физическим состоянием (осадок, жидкость, газ); известной растворимостью в воде, кислотах, щелочах и других растворителях; характерным цветом, запахом и т.д. Такие реакции называют качественными на соответствующие ионы, молекулы или группы атомов.
2) Физические – методы, основанные на изучении физических (оптических, электрических, магнитных, тепловых и других) свойств веществ или их растворов без применения химических реакций.
3) Физико-химические – основаны на измерении физических свойств, проявляющихся или изменяющихся в результате химических реакций.
Качественный анализ. Реакции, применяемые в качественном химическом анализе, чаще всего проводят в растворах. Анализируемое вещество сначала растворяют, а затем действуют на полученный раствор соответствующими реактивами. В некоторых случаях вещества анализируют сухим путем, без перевода их в раствор.
Проведение качественного анализа неизвестного вещества начинают с анализа сухого вещества.
Анализ сухого вещества включает следующие операции:
а) определение окраски бесцветного пламени горелки при внесении в пламя анализируемого вещества. Некоторые вещества способны окрашивать бесцветное пламя горелки в характерные цвета, например: соединения натрия окрашивают пламя в желтый цвет, соединения калия – в фиолетовый, соединения кальция – в кирпично-красный, бария – желто-зеленый, меди – в зеленый;
б) термическое разложение вещества. В результате нагревания веществ возможна возгонка этого вещества либо разложение с выделением газообразных продуктов. Образование капель воды при нагревании указывает на присутствие солей, содержащих кристаллизационную воду, органических соединений, гидроксидов, основных и кислых солей. Выделение кислорода свидетельствует о присутствии перекисных соединений, нитратов, хлоратов, перманганатов и других богатых кислородом соединений. Например, при термическом разложении нитрата калия происходит следующая реакция:
2KNO3 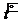 2KNO2 + O2↑
2KNO2 + O2↑
Выделение диоксида углерода СО2 свидетельствует о присутствии карбонатов и органических соединений; оксидов азота – о присутствии нитратов и нитритов; выделение хлора, брома и иода – о присутствии хлоридов, бромидов и иодидов, гипохлоритов, хлоратов и др. подобных соединений; выделение аммиака свидетельствует о присутствии солей аммония, цианидов и т.п.;
в) растворение вещества в воде, кислотах, щелочах и других растворителях. Для растворения вещества применяют дистиллированную воду, уксусную, серную, азотную и другие кислоты, царскую водку, водный раствор аммиака, органические растворители.
Полученные растворы анализируют при помощи качественных реактивов или реагентов – веществ, вызывающих характерные превращения исследуемых веществ.
В результате реакции может:
а) образоваться нерастворимое соединение (осадок) определенного цвета. Например, ион серебра образует нерастворимые осадки разного цвета: АgС1 – белый, АgI – бледно-желтый, Аg2S – черный;
б) образоваться характерное окрашивание исследуемого раствора. Например, рН-индикаторы указывают на присутствие избытка иона Н+ или ОН- в зависимости от окраски этого индикатора в данном растворе;
в) образоваться газообразное вещество, например, аммиак в растворе соединений аммония, диоксид углерода – при анализе растворов карбонатов.
Аналитические реакции проводят с реактивами, образующими характерные продукты реакции, которые легко установить, не прибегая к специальным методам исследования. Зная состав образовавшегося продукта реакции, делают вывод о наличии в составе анализируемого вещества того или иного искомого элемента или иона.
Качественные реакции на ионы. Некоторые ионы легко распознать при помощи следующих качественных реакций:
а) Ионы Н+ и ОН- – по окраске индикаторов – фенолфталеина (бесцветная в нейтральной и кислой среде, малиновая – в щелочной), лакмуса (красная в кислой среде, фиолетовая – в нейтральной, синяя – в щелочной) и метилоранжа (красная в кислой, оранжевая – в нейтральной, желтая – в щелочной среде).
б) Ион Ва2+ - при помощи раствора H2SO4:
Ва2+ + SO42- → ВаSO4↓
Образовавшийся осадок ВаSO4 имеет белый цвет и не растворяется в кислотах.
в) Ион NH4+ - при нагревании анализируемого раствора с NaOH:
NH4+ + OH- 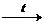 NH3↑ + H2O
NH3↑ + H2O
В результате реакции выделяется аммиак NН3, обладающий резким характерным запахом.
г) Ион Fе3+ - при взаимодействии с роданидом аммония NH4CNS и гексацианоферратом (II) калия:
Fe3+ + 3CNS ˉ → Fe(CNS)3
4Fe3+ + 3[Fe(CN)6]4- → Fe4[Fe(CN)6]3
В результате этих реакций образуются окрашенное слабо диссоциирующее соединение – кроваво-красный роданид железа (III) – Fe(CNS)3 и синий гексацианоферрат (II) железа (III), называемый берлинской лазурью.
д) Ион Fе2+ - при реакции с гексацианоферратом (III) калия:
3Fe2+ + 2[Fe(CN)6]3- → Fe3[Fe(CN)6]2
Образовавшийся гексацианоферрат (III) железа (II) представляет собой нерастворимую соль синего цвета, называемую турнбулевой синью.
е) Ионы Clˉ, Brˉ, Iˉ, S2ˉ, PO43ˉ - по реакции с AgNO3. В результате образуются нерастворимые осадки: АgС1 – белого, AgBr – желтоватого, AgI – бледно-желтого, Ag2S – черного, Ag3PO4 – ярко-желтого цвета.
ж) Ион SO42ˉ - при взаимодействии с ВаCl2 образуется белый осадок ВаSO4.
з) Ион СО32ˉ - разложение карбонатов при реакции с НС1:
СО32ˉ + 2Н+ → СО2↑ + Н2О
Образовавшийся углекислый газ пропускают через раствор гидроксида кальция Са(ОН)2 и по помутнению этого раствора судят о присутствии определяемого иона:
СО2 + Са(ОН)2 → СаСО3↓ + Н2О
Одним из основных методов химического анализа является окисление-восстановление, которое широко используется в аналитической химии.
Окислителями в химических реакциях являются элементы, находящиеся в максимальной для данного элемента степени окисленности, восстановителями – находящиеся в минимально возможной степени окисленности. Если же элемент имеет промежуточную степень окисленности, то в зависимости от условий он может выполнять как функцию окислителя, так и восстановителя.
К числу сильных окислителей относятся следующие ионы и молекулы: МnО4ˉ, Сr2О72ˉ, Сl2, Вr2, NO3ˉ, Fe3+, I2, SО42ˉ, Sn4+. Окислители вступают в реакцию восстановления, заключающуюся в присоединении электронов:
Mn+7 + 5ē → Mn+2
Cr+6 + 3ē → Cr+3
I2 + 2ē → 2I‾
К наиболее сильным восстановителям относятся активные металлы, а также ионы S2ˉ, I‾, Fe2+, Cl‾. Восстановители в ходе окислительно-восстановительной реакции отдают электроны, а сами при этом окисляются:
S2ˉ – 2ē → S↓
2I‾ – 2ē → I2
2Cl‾ – 2ē → Cl2
Fe2+ – ē → Fe3+
Наиболее полно окислительно-восстановительные реакции протекают в кислой среде, поэтому в растворы предварительно добавляют какую-либо кислоту, чаще всего – серную H2SO4.
Пример 1.
Написать химические формулы веществ, находящихся в трех колбах, если: 1) раствор из первой колбы окрашивает пламя в желтый, а из второй – в фиолетовый цвет; 2) при нагревании образца из третьей колбы с NaOH появился запах аммиака; 3) при приливании раствора AgNO3 во всех образцах выпали осадки белого цвета, причем в образце из третьей колбы осадок растворился при добавлении воды; 4) добавление раствора ВаС12 способствовало выпадению белых осадков в образцах из второй и третьей колб; 5) приливание раствора НС1 привело к бурному выделению газа в образце из второй колбы, причем этот газ вызвал помутнение раствора Са(ОН)2. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
Решение. По изменению окраски пламени можно сделать вывод о том, что в первой колбе находится соединение натрия (желтая окраска пламени), во второй – калия (фиолетовая окраска пламени).
Нагревание раствора с NaOH является качественной реакцией на присутствие в растворе иона NH4+ поскольку при этом появился запах аммиака, значит в третьей колбе находится соединение аммония.
Приливание раствора AgNO3 к образцам из всех колб вызвало образование осадков белого цвета. Согласно таблице растворимости солей и оснований в воде (Приложение), такие осадки могут быть получены, если в состав соединений входят следующие ионы: Cl‾, SO32‾, SO42‾ и СО32‾, а при их взаимодействии с ионом Ag+ получаются AgCl, Ag2SO3, Ag2SO4 и Ag2CO3. Растворение осадка, полученного в образце из третьей колбы, при добавлении воды, говорит о том, что получившийся осадок является малорастворимым веществом. Это возможно в том случае, если формула этого вещества – Ag2SO4. Следовательно, в третьей колбе находится сульфат.
Этот вывод подтверждается и результатами следующего эксперимента – добавления раствора ВаСl2. При этом могут образоваться нерастворимые осадки ВаSО3, ВаSО4, ВаСО3. Поскольку установлено, что в образце из первой колбы осадка не образовалось, следовательно, там находится ион Сl‾, который не образует осадка с ионом Ва2+.
Во второй колбе может содержаться либо ион SO32‾, либо ион СО32‾. Присутствие во второй колбе иона СО32‾ подтверждается качественной реакцией с НС1, в результате чего выделился газ, вызвавший помутнение раствора Са(ОН)2.
Таким образом, в состав вещества в первой колбе входят ионы Na+ и Сl‾, во второй колбе – К+ и СО32‾; в третьей колбе – NH4+ и SO42‾. Получаем химические формулы этих веществ: первая колба – NaCl, 2-я колба – К2СО3, 3-я колба – (NH4)2SO4.
Запишем уравнения реакций, протекающих в образцах из этих колб, при добавлении реактивов:
с NaOH: (NH4)2SO4 + 2NaOH 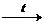 Na2SO4 +2NH3 ↑ + 2H2O
Na2SO4 +2NH3 ↑ + 2H2O
2NH4+ + SO42‾ + 2Na+ + 2OH‾ 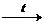 2Na+ + SO42‾ + 2NH3 ↑ + 2H2O
2Na+ + SO42‾ + 2NH3 ↑ + 2H2O
NH4+ + OH‾  NH3 ↑ + H2O
NH3 ↑ + H2O
с AgNO3: 1. NaCl + AgNO3 → AgCl↓ + NaNO3
Na+ + Cl‾ + Ag+ + NO3‾ → AgCl↓ + Na+ + NO3‾;
Cl‾ + Ag+ → AgCl↓
2. K2CO3 + 2AgNO3 → Ag2CO3↓ + 2KNO3
2K+ + CO32‾ + 2Ag+ + 2NO3‾ → Ag2CO3↓ + 2K+ + 2NO3‾;
CO32‾ + 2Ag+ → Ag2CO3↓
3. (NH4)2SO4 + 2AgNO3 → Ag2SO4↓ + 2NH4NO3
2NH4+ + SO42‾ + 2Ag+ + 2NO3‾ → Ag2SO4↓ + 2NH4+ + 2NO3‾;
SO42‾ + 2Ag+ → Ag2SO4↓
c BaCl2: 2. K2CO3 + BaCl2 → BaCO3↓ + 2KCl
2K+ + CO32‾ + Ba2+ + 2Cl‾ → BaCO3↓ + 2K+ + 2Cl‾;
CO32‾ + Ba2+ → BaCO3↓
3. (NH4)2SO4 +BaCl2 → BaSO4↓ + 2NH4Cl
2NH4+ + SO42‾ + Ba2+ + 2Cl‾ → BaSO4↓ + 2NH4+ + 2Cl‾
SO42‾ + Ba2+ → BaSO4↓
c HCl: K2CO3 + 2HCl → 2KC1 + CO2↑ +H2O
2K+ + CO32‾ + 2H+ + 2Cl‾ → 2K+ + 2Cl‾ + CO2↑ +H2O
CO32‾ + 2H+ → CO2↑ +H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Пример 2.
В четырех колбах без этикеток содержатся растворы следующих веществ: соляной кислоты, хлорида бария, сульфата калия, фосфата калия. Используя дополнительно раствор AgNO3, определить, в какой именно колбе содержится каждое из указанных веществ. Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
Решение. Прильем в образцы из всех колб раствор AgNO3. При этом должны произойти следующие реакции:
1. HCI + AgNO3 → AgCl↓+ HNO3
Н+ + Cl‾ + Ag+ + NO3‾ → AgCl↓ + H+ + NO3‾;
Cl‾ + Ag+ → AgCl↓
2. BaCl2 + 2AgNO3 → 2AgCl↓+ Ba(NO3)2
Ba2+ + 2Cl‾ + 2Ag+ + 2NO3‾ → 2AgCl↓ + Ba2+ + 2NO3‾;
Cl‾ + Ag+ → AgCl↓
3. K2SO4 + 2AgNO3 → Ag2SO4↓ + 2KNO3
2K+ + SO42‾ + 2Ag+ + 2NO3‾ → Ag2SO4↓ + 2K+ + 2NO3‾;
SO42‾ + 2Ag+ → Ag2SO4↓
4. K3PO4 + 3AgNO3 → Ag3PO4↓ + 3KNO3
3K+ + PO43‾ + 3Ag+ + 3NO3‾ → Ag3PO4↓ + 3K+ + 3NO3‾;
PO43‾ + 3Ag+ → Ag3PO4↓
Осадки AgCl и Ag2SO4 имеют белый цвет, a Ag3PO4 – ярко-желтый, следовательно, в том образце, где выпадет осадок ярко-желтого цвета, находится К3РО4.
Добавим к оставшимся растворам с белыми осадками воду. Поскольку Ag2SO4 является малорастворимым, осадок в соответствующем образце растворится, следовательно, в этом образце изначально содержался K2SO4. В оставшихся неопознанными образцах будут находиться HCl и ВаСl2. Чтобы их различить, добавим в каждый образец уже определенный нами ранее раствор K2SO4.
1. 2НСl + K2SO4 D H2SO4 + 2КСl
2. ВаСl2 + K2SO4 → BaSO4↓ + 2KCl
Ba2+ + 2Сl‾ + 2K+ + SO42‾ → BaSO4↓ + 2K+ + 2Сl‾
Ba2+ + SO42‾ → BaSO4↓
В образце из той колбы, где находится ВаСl2, выпадет осадок белого цвета, а там, где содержится НСl, изменений не произойдет.
Вопросы и задачи.
126. Написать химические формулы веществ, находящихся в трех колбах, если: 1) раствор из колбы №2 окрашивает пламя горелки в желтый цвет, а из колбы №3 – в фиолетовый; 2) при нагревании образца из первой колбы с NaOH появился запах аммиака; 3) при приливании раствора AgNO3 в образцах из всех колб выпал осадок белого цвета, причем в образце из колбы №3 он растворился при добавлении воды; 4) при добавлении серной кислоты в образце из второй колбы произошло бурное выделение газа, который вызвал помутнение раствора Са(ОН)2; 5) добавление раствора BaCl2 привело к образованию белого осадка в образцах из второй и третьей колб. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
127. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы окрашивают пламя горелки в желтый цвет (образец из второй колбы) и фиолетовый цвет (образец из третьей колбы); 2) при приливании раствора AgNO3 в образцах из первой и второй колб выпал белый осадок, причем в образце из второй колбы он растворился при добавлении Н2О, а в образце из третьей колбы выпал осадок ярко-желтого цвета; 3) раствор BaCl2 вызвал образование осадков белого цвета в образцах из второй и третьей колб; 4) добавление к образцам раствора роданида аммония NH4CHS привело к образованию ярко-красного окрашивания раствора из первой колбы. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
128. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы окрашивают пламя горелки в желтый цвет (образец из второй колбы) и кирпично-красный цвет (образец из третьей колбы) 2) при приливании раствора AgNO3 в образце из второй колбы выпал осадок ярко-желтого цвета, а в образце из третьей колбы – белого цвета; 3) при добавлении к образцу из первой колбы раствора HCl с последующим нагреванием был обнаружен запах уксусной кислоты; 4) нагревание образца из первой колбы с раствором NaOH вызвало появление запаха аммиака. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
129. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы окрашивают пламя горелки в желто-зеленый (образец из первой колбы), фиолетовый (образец из второй колбы) и желтый цвет (образец из третьей колбы); 2) при приливании раствора AgNO3 выпали осадки белого (первая колба) и черного (третья колба) цвета; 3) внесение сухого вещества из второй колбы в пламя горелки вызвало сгорание этого вещества, сопровождающееся вспышками пламени. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
130. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы из первой и второй колб окрашивают пламя горелки в желтый цвет; 2) при нагревании раствора из третьей колбы с КОН ощущается запах аммиака; 3) приливание раствора AgNO3 привело к образованию белых осадков в образцах из первой и третьей колб, причем в образце из первой колбы осадок растворился при добавлении воды; 4) при приливании раствора ВаС12 в образце из первой колбы выпал белый осадок; 5) внесение сухого вещества из второй колбы в пламя горелки вызвало сгорание этого вещества, сопровождающееся вспышкой пламени. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
131. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы из всех колб окрашивают пламя горелки в желтый цвет; 2) приливание раствора AgNO3 привело к выпадению осадка ярко-желтого цвета в образце из первой колбы, 3) нагревание раствора из второй колбы с раствором HCl вызвало появление запаха уксусной кислоты; 4) внесение в пламя горелки сухого вещества из третьей колбы сопровождалось яркими вспышками пламени. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
132. Написать химические формулы веществ, находящихся в трех колбах, если: 1) раствор из первой колбы окрашивает пламя горелки в кирпично-красный цвет, а из третьей колбы – в фиолетовый; 2) при приливании раствора AgNO3 в образце из второй колбы выпал осадок белого цвета, а в образце из третьей колбы – черного цвета; 3) приливание раствора HCl к образцу из второй колбы привело к бурному выделению газа, который вызвал помутнение раствора Са(ОН)2; 4) внесение в пламя горелки сухого вещества из первой колбы сопровождалось яркими вспышками пламени; 5) нагревание образца из второй колбы с NaOH привело к появлению запаха аммиака. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
133. Написать химические формулы веществ, находящихся в трех колбах, если: 1) раствор из первой колбы окрашивает пламя горелки в фиолетовый цвет, из второй – желтый, а из третьей – в желто-зеленый цвет; 2) при приливании раствора AgNO3 в образце из первой колбы выпал творожистый осадок бледно-желтого цвета, а из второй колбы – ярко-желтого цвета; 3) приливание раствора H2SO4 способствовало образованию белого осадка в образце из третьей колбы. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
134. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы окрашивают пламя горелки в фиолетовый цвет; 2) при приливании раствора AgNO3 в образцах из первой и третьей колб выпал осадок белого цвета, а из второй колбы – ярко-желтый осадок; 3) при добавлении серной кислоты в образце из третьей колбы произошло бурное выделение газообразного вещества, которое вызвало помутнение раствора Са(ОН)2. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
135. Написать химические формулы веществ, находящихся в трех колбах, если: 1) растворы окрашивают пламя горелки в фиолетовый цвет (образцы из первой и второй колб) и желтый цвет (образец из третьей колбы); 2) при приливании раствора AgNO3 в образце из второй колбы выпал творожистый осадок белого цвета; 3) при добавлении раствора ВаС12 в образцах из первой и третьей колб выпал белый осадок; 4) при добавлении раствора Н2SО4 изменений не обнаружено. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
136.В пять пробирок, содержащих растворы хлоридов калия, меди (II), бария, алюминия и железа (III), добавили раствор NaOH. Указать, в каких именно пробирках находились данные соли, если в первой пробирке выпал осадок белого цвета, в четвертой – голубого цвета, в пятой – бурого цвета, а во второй и третьей осадка не образовалось. При помощи какого реагента можно определить состав содержимого второй и третьей пробирок? Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
137. В пять пробирок, содержащих растворы нитратов натрия, аммония, магния, железа (II) и кальция, добавили раствор КОН. Указать, в каких именно пробирках находились данные соли, если в первой пробирке выпал осадок зеленого цвета, во второй и четвертой – белого цвета, причем во второй он растворился при разбавлении водой, а в третьей и пятой пробирках осадка не образовалось. Как можно определить состав растворов в третьей и пятой пробирках? Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
138. В пять пробирок, содержащих растворы ацетатов калия, магния, цинка, железа (III) и аммония, добавили раствор КОН. Указать, в какой именно пробирке находилась каждая соль, если в первой и четвертой пробирках выпали осадки белого цвета, причем осадок в первой пробирке растворился при приливании избытка КОН, в третьей пробирке выпал осадок бурого цвета, а во второй и пятой пробирках осадка не образовалось, однако при нагревании пятой пробирки появился запах аммиака. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
139.В пять пробирок, содержащих растворы сульфатов натрия, марганца (II), меди (II), алюминия и хрома (III), добавили раствор NaOH. Указать, в какой именно пробирке находится каждая соль, если в четвертой пробирке выпал осадок голубого цвета, в третьей – синевато-серого цвета, в первой и пятой пробирках – белого цвета, причем осадок в пятой пробирке растворился при добавлении избытка NaOH, а во второй пробирке осадка не образовалось. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
140. В пяти колбах находятся растворы нитратов калия, кальция, натрия, серебра и цинка. Определить, в какой именно колбе находится каждый раствор, если: 1) раствор из второй колбы окрашивает пламя горелки в желтый цвет, из третьей – в фиолетовый, из четвертой – в кирпично-красный цвет; 2) приливание раствора KCl вызывает образование в образце из первой колбы белого творожистого осадка, а приливание КI – бледно-желтого осадка; 3) при добавлении в образцы из четвертой и пятой колб раствора NaOH образуются белые осадки, причем осадок из четвертой колбы растворяется при дальнейшем разбавлении водой, в осадок из пятой колбы – при избытке NaOH. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
141. В пяти колбах находятся растворы ацетатов аммония, бария, железа (II), натрия и свинца (II). Определить, в какой именно колбе находится каждый раствор, если: 1) раствор из первой колбы окрашивает пламя горелки в желтый цвет, из третьей – в желто-зеленый; 2) приливание раствора серной кислоты вызывает образование белых осадков в образцах из третьей и четвертой колб; 3) при добавлении раствора КОН образовался осадок белого цвета в образце из четвертой колбы и зеленого цвета – в образце из пятой колбы; 4) при нагревании образца из второй колбы с гидроксидом калия появился запах аммиака. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
142. В пяти колбах находятся растворы сульфатов алюминия, аммония, железа (III), магния и натрия. Определить, в какой именно колбе находится каждый раствор, если: 1) раствор из четвертой колбы окрашивает пламя горелки в желтый цвет; 2) при приливании раствора КОН выпали белые осадки в образцах из первой и второй колб, причем осадок из первой колбы растворился от избытка КОН, а в образце из пятой колбы выпал осадок бурого цвета; 3) нагревание образца из третьей колбы с КОН вызвало появление запаха аммиака; 4) добавление раствора роданида аммония NH4CNS в образец из пятой колбы способствовало появлению ярко-красного окрашивания раствора. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
143. В пяти колбах находятся растворы солей аммония – ацетат, бромид, карбонат, сульфат и хлорид. Определить, в какой именно колбе находится каждая из солей, если: 1) при приливании раствора AgNO3 в образцах из первой, третьей и четвертой колб выпал осадок белого цвета, причем осадок из третьей колбы растворился при добавлении воды, а в образце из второй колбы выпал желтоватый осадок; 2) добавление раствора ВаС12 вызвало образование осадков в образцах из третьей и четвертой колб; 3) приливание раствора НС1 вызвало бурное выделение газа в образце из четвертой колбы, причем этот газ вызвал помутнение раствора Са(ОН)2; 4) при нагревании образца из пятой колбы с раствором НС1 появился запах уксусной кислоты. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
144. В пяти колбах находятся растворы солей меди (II) – ацетат, бромид, нитрат, сульфат, хлорид. Определить, в какой именно колбе находится каждая из солей, если: 1) при приливании раствора AgNO3 в образцах из первой и пятой колб выпал белый осадок, причем в образце из пятой колбы он растворился при разбавлении водой, а в образце из второй колбы – осадок желтоватого цвета; 2) приливание раствора BaCl2 вызвало образование белого осадка в образце из пятой колбы; 3) нагревание образца из четвертой колбы с раствором HCl способствовало появлению запаха уксусной кислоты. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
145. В пяти колбах находятся растворы солей калия. Определить, что это за соли и в какой именно колбе находится каждая из солей, если: 1) при приливании раствора AgNO3 в образце из первой колбы выпал творожистый осадок белого цвета, а в образце из второй колбы – ярко-желтого, а в четвертой – черного; 2) приливание раствора HCl привело к образованию студенистого осадка в образце из пятой колбы; 3) нагревание образца из третьей колбы с HCl вызвало появление запаха уксусной кислоты, а образца из четвертой колбы – запаха сероводорода; 4) при приливании раствора BaCl2 к образцу из первой колбы никаких изменений не произошло, а при добавлении этого раствора к образцу из второй колбы выпал осадок белого цвета. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
146.В пяти колбах находятся растворы солей натрия – ацетат, карбонат, сульфат, сульфид, сульфит. Определить, в какой именно колбе находится каждая из солей, если: 1) при приливании раствора AgNO3 в образце из первой колбы выпал осадок черного цвета, а в образцах из второй, третьей и пятой колб – осадок белого цвета, причем осадок из третьей колбы растворился при разбавлении водой; 2) приливание к образцу из пятой колбы раствора HCl способствовало бурному выделению газа, вызвавшего помутнение раствора Са(ОН)2. Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
147. В трех пробирках находятся растворы сульфата, сульфита и сульфида натрия в воде. Определить, в какой именно пробирке находится раствор каждой соли, если при добавлении в каждую пробирку нескольких капель раствора йода I2 наблюдалось следующее: в первой пробирке йод обесцветился, но в результате реакции раствор помутнел, а через некоторое время выделился осадок бледно-желтого цвета; во второй пробирке йод также обесцветился, но раствор остался прозрачным; в третьей пробирке никаких изменений не наблюдалось. Ответ подтвердить уравнениями соответствующих реакций.
148. В трех пробирках находятся растворы йодида калия, нитрата калия и пероксида водорода. Определить, в какой именно пробирке находится каждый раствор, если при добавлении в каждую пробирку смеси КМnО4 и Н2SО4 наблюдалось следующее: в первой пробирке раствор перманганата калия обесцветился, при этом наблюдалось выделение пузырьков газа, поддерживающего горение; во второй пробирке в результате реакции образовалось желто-коричневое вещество, которое через некоторое время выпало в осадок; в третьей пробирке изменений не произошло. Ответ подтвердить уравнениями соответствующих реакций.
149. В трех пробирках находятся растворы сульфата, сульфита и хлорида калия. Определить, в какой именно пробирке находится каждый раствор, если при приливании в каждую пробирку смеси растворов КМnО4 и Н2SО4 наблюдалось следующее: в первой пробирке раствор перманганата калия обесцветился, во второй пробирке обесцвечивание раствора сопровождалось выделением пузырьков газа с резким запахом, напоминающим хлор; в третьей пробирке никаких изменений не наблюдалось. Ответ подтвердить уравнениями соответствующих реакций.
150. В трех пробирках находятся растворы сульфата, сульфита и сульфида калия. Определить, в какой именно пробирке находится каждая соль, если при приливании в каждую пробирку смеси растворов К2Сr2О7 и Н2SO4 наблюдалось следующее: в первой пробирке раствор изменил окраску с оранжевой на зеленую; во второй пробирке такое же изменение окраски сопровождалось помутнением раствора, а через некоторое время – образованием бледно-желтого осадка; в третьей пробирке никаких изменений не наблюдалось. Ответ подтвердить уравнениями соответствующих реакций.
151. Как при помощи перманганата калия можно различить: а) сульфаты железа (II) и (III); б) нитрат и нитрит калия? Ответ подтвердить уравнениями возможных окислительно-восстановительных реакций.
152. Как при помощи дихромата калия можно различить: а) сульфаты железа (II) и (III); б) нитрат и нитрит калия? Ответ подтвердить уравнениями возможных окислительно-восстановительных реакций.
153. Как при помощи перманганата калия можно различить: а) нитраты ртути Hg2(NO3)2 и Hg(NO3)2; б) сульфат и сульфит калия? Ответ подтвердить уравнениями возможных окислительно-восстановительных реакций.
154. Как при помощи дихромата калия можно различить а) нитраты ртути Hg2(NO3)2 и Hg(NO3)2; б) сульфат и сульфит калия? Ответ подтвердить уравнениями возможных окислительно-восстановительных реакций.
155. Что такое рН-индикаторы? Присутствие каких ионов в растворе можно обнаружить при помощи этих индикаторов? Привести примеры.
156. Используя таблицу растворимости солей и оснований в воде, указать два химических реагента, каждый из которых позволяет одновременно различать растворы хлоридов магния, кальция и бария. Написать в молекулярной и молекулярно-ионной форме уравнения реакций, протекающих между этими реагентами и каждой из солей.
157. В трех банках без этикеток находятся следующие вещества: сульфат натрия, сульфит натрия и сульфид натрия. Как, имея в своем распоряжении лишь один реактив, узнать, где какая соль находится? Указать этот реактив. Написать в молекулярной и молекулярно-ионной форме уравнения реакций между этим реактивом и каждой из солей.
158. При помощи каких химических реактивов можно различить следующие соединения натрия: карбонат, хлорид, сульфат, фосфат и гидроксид натрия? Ответ подтвердить уравнениями соответствующих реакций в молекулярной и молекулярно-ионной форме.
159. При помощи какого универсального реактива можно определить, в какой из шести пробирок находятся растворы NaCl, NaBr, NaI, Na2S, Na3РО4 и СН3СООNа? Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме с указанием цвета осадков.
160. Как при помощи воды и азотной кислоты распознать четыре порошка – соду, мел, сульфат натрия и гипс? Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
161. Как при помощи воды и соляной кислоты распознать четыре порошка – гашеную известь, мел, кальциевую селитру и фосфат кальция? Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
162. В четырех пакетах содержатся следующие вещества: сульфат алюминия, нитрат бария, хлорид аммония, сульфит натрия. Используя раствор гидроксида калия и открытый им сульфат алюминия, обнаружить все остальные вещества. Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
163. В четырех колбах без этикеток содержатся растворы следующих веществ: азотной кислоты, хлорида бария, фосфата натрия, сульфата натрия. Используя дополнительно раствор AgNO3 определить, в какой именно колбе содержится каждое из указанных веществ. Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
164.В четырех колбах содержатся сульфаты и хлориды железа (II) и (III). При помощи каких реактивов можно определить, в какой именно колбе содержится каждая из четырех солей? Ответ подтвердить уравнениями реакций в молекулярной и молекулярно-ионной форме.
165-168. При помощи каких качественных реакций можно подтвердить состав трех приведенных ниже веществ? Написать уравнения соответствующих реакций в молекулярной и молекулярно-ионной форме.
165. (NH4)2SO4, KCl, Na2S.
166. К2CO3, NH4Cl, Na2SO4.
167. K3PO4, NaNO3, BaCl2.
168. FeSO4, Na2CO3, KI.
169. Имеются следующие удобрения: а) калийная селитра; б) сульфат аммония; в) хлорид аммония; г) суперфосфат; д) аммиачная селитра; е) диаммофос. В каких случаях при внесении удобрений на раскаленный уголек будет наблюдаться вспышка, в каких случаях будет ощущаться запах аммиака? Ответ подтвердить уравнениями соответствующих реакций. В каких случаях при внесении удобрений в пламя горелки окраска пламени изменится? Ответ мотивировать.
170. Как при помощи гидроксида натрия, нитрата серебра и хлорида бария определить, какое из удобрений – сульфат аммония, чилийская селитра, хлорид аммония – представляет собой исследуемый образец удобрения? Ответ подтвердить уравнениями всех возможных реакций в молекулярной и молекулярно-ионной форме.
171. Как при помощи гидроксида натрия, нитрата серебр
