Уравнение состояния идеального газа
2.1. Состояние данной массы идеального газа описывается уравнением Менделеева - Клапейрона:
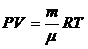 ,
,
где P,T - давление и температура газа; V - объем, занимаемый данной массой газа (объем сосуда); 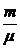 - число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K).
- число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K).
2.2. Исходя из уравнения состояния, можно определить плотность идеального газа:
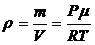 .
.
Между температурой t (по шкале Цельсия) и температурой T (по шкале Кельвина) существует следующая связь:
T=(t + 273,15)К 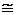 (t+273) К.
(t+273) К.
2.3. Вводя постоянную Больцмана 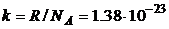 Дж/К уравнение состояния (2.1) примет вид:
Дж/К уравнение состояния (2.1) примет вид:
р = nkT,
где n – концентрация молекул.
2.4. Закон Дальтона для смеси газа.
Если в сосуде V при температуре T содержится смесь газов, то необходимо считать, что каждый из компонентов этой смеси распространяется по всему объему сосуда. Парциальное давление pi, создаваемое отдельным i-м компонентом смеси, определяется из уравнения Менделеева - Клапейрона:
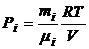 ,
,
где mi- масса данного компонента в смеси; 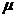 i - масса одного моля этого компонента.
i - масса одного моля этого компонента.
Давление смеси газов равно сумме парциальных давлений, входящих в нее газов:
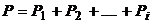
или
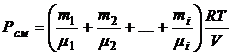 .
.
В равновесном состоянии плотность смеси ρсм равна сумме плотностей компонентов смеси:
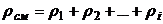 .
.
Пример 1. Смесь азота и гелия при температуре 270С находится под давлением Р = 1,3·102Па. Масса азота составляет 70% от общей массы смеси. Найти концентрацию молекул каждого из газов.
Дано: Р=1,3·102Па; m1=0,7m; m1 =28г/моль=28·10-3кг/моль; 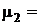 4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
Найти: n1 и n2.
Решение. Давление смеси выразим по закону Дальтона:
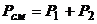 .
.
где Р1 – парциальное давление азота в смеси; Р2 – парциальное давление гелия.
Выразим Р1и Р2 из уравнения Менделеева - Клапейрона:
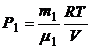 ;
; 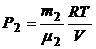 .
.
Найдем соотношение между Р1 и Р2:
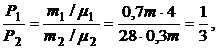 т. е. Р2 = 3Р1.
т. е. Р2 = 3Р1.
Так как
Рсм = Р1 + Р2 = Р1 + 3Р1 = 4Р1,
Следовательно,
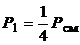 ,
, 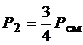 .
.
С другой стороны, давление любого газа можно легко выразить через концентрацию его молекул (n) и температуру:
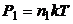 ;
; 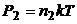 .
.
Отсюда
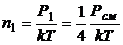 ;
; 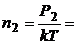
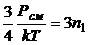 .
.
Проверим размерность:

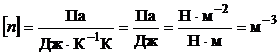 .
.
Произведем вычисления:
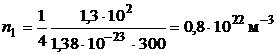 ;
;
n2 = 3n 1 = 2,4 ·1022 м-3.
Ответ: n1 = 0,8·1022 м-3; n2 = 2,4·1022м-3.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ
ИДЕАЛЬНЫХ ГАЗОВ
3.1. Основное уравнение кинетической теории газов для давления:

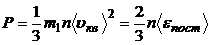 ,
,
где m1 - масса одной молекулы; n – концентрация молекул; 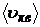 - средняя квадратичная скорость молекул.
- средняя квадратичная скорость молекул.
3.2. Средняя кинетическая энергия поступательного движения молекулы:

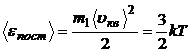 .
.
(Эта формула раскрывает молекулярно – кинетическое толкование температуры: она – мера средней кинетической энергии поступательного движения молекул идеального газа).
3.3 Закон о равномерном распределении энергии по степеням свободы молекул: на каждую степень свободы приходится в среднем одинаковая энергия, равная
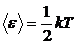 .
.
3.4. Средняя энергия молекулы:
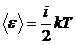 ,
,
где i - число степеней свободы молекулы данного газа: для одноатомных молекул i = 3 (поступательных), для двухатомных i = 5 (3 поступательных + 2 вращательных), для всех многоатомных i = 6 (3 поступательных + 3 вращательных).
3.5. Внутренняя энергия массы m газа:
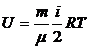 .
.
3.6. Скорости газовых молекул:
· средняя квадратичная
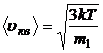 или
или 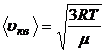 ,
,
· средняя арифметическая
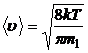 или
или 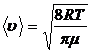 ,
,
· вероятная
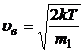 или
или 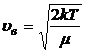 .
.
Пример 2. Найти среднюю квадратичную скорость, среднюю кинетическую энергию поступательного движения и среднюю полную кинетическую энергию молекул гелия и азота при температуре t = 27 оС. Определить полную энергию всех молекул каждого из газов. Массы газов одинаковы ( 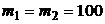 г).
г).
Дано: t = 27оС; T=300 K; =100г = 100ּ10-3кг; μ1 = 4г/моль=4·10-3кг/моль; i1 = 3; μ2 = 28г/моль = 28· 10-3кг/моль; і2 = 5.
Найти: 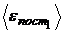 ;
; 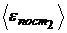 ;
; 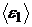 ;
; 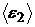 ;
; 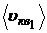 ;
; 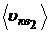 ; U1; U2 .
; U1; U2 .
Решение.1. Средняя кинетическая энергия поступательного движения одной молекулы при данной температуре T одинакова для любых молекул, т.е.
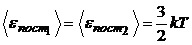 .
.
2. Полная кинетическая энергия молекулы газа определяется по формуле:
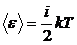 ,
,
тогда для молекул двух разных газов:
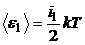 ,
, 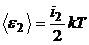 .
.
3. Внутренняя энергия, заключенная в 100 г каждого из газов, определяется по формулам:
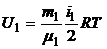 ,
, 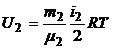 .
.
4. Средняя квадратичная скорость молекул этих газов зависит от их молярной массы газа или от их масс, т.е.
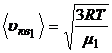 ,
, 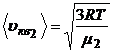 .
.
Проверим размерность:
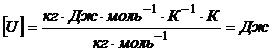 ;
;
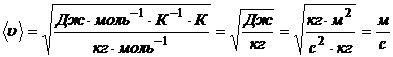 .
.
Произведем вычисления:
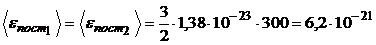 Дж;
Дж;
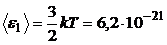 Дж;
Дж;
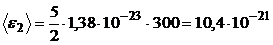 Дж;
Дж;
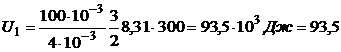
 кДж;
кДж;
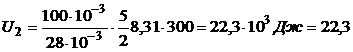 кДж;
кДж;
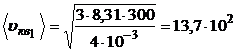 м/с;
м/с;
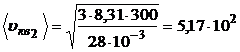 м/с.
м/с.
Ответ: 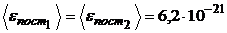 Дж;
Дж; 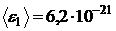 Дж;
Дж; 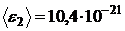 Дж;
Дж; 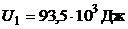 ;
; 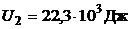 ;
; 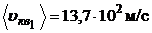 ;
; 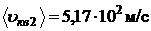 .
.
4. ТЕПЛОЕМКОСТИ ИДЕАЛЬНОГО ГАЗА
4.1. Теплоемкость системы (тела):
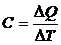 ,
,
где ∆Q – количество теплоты, сообщенное системе (телу); ∆Т – изменение температуры системы (тела), вызванное сообщением этого количества теплоты.
4.2. Молярная и удельная теплоемкости:
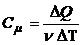 ;
; 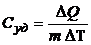 .
.
4.3. Молярные теплоемкости идеального газа при постоянном объеме Сvμ и постоянном давлении Срμ:
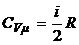 ,
, 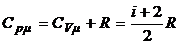 .
.
4.4. Соотношение между молярной и удельной теплоемкостями:
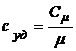 .
.
4.5. Удельные теплоемкости идеального газа при постоянном объеме и постоянном давлении:
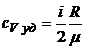 ,
, 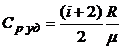 .
.
4.6. Отношение теплоемкостей (показатель адиабаты):
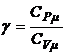 или
или 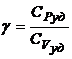 или
или 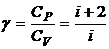 .
.
4.7. Количество теплоты, израсходованное на нагревание данного вещества: 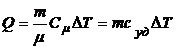 .
.
Пример 3. Вычислить удельные теплоемкости газа, зная, что его молярная масса µ = 4· 10-3кг/моль и отношение теплоемкостей γ = 1,67.
Дано: μ = 4·10-3 кг/моль; γ = 1,67.
Найти: сVуд, 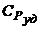 .
.
Решение. Исходя из классической теории теплоемкостей идеального газа, имеем:

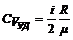 ,
, 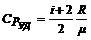 .
.
Определим i из выражения:

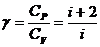 ,
,
отсюда
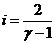 ,
, 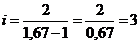 .
.
Следовательно, газ одноатомный.
Проверим размерность:
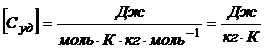 .
.
Производим вычисления:
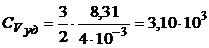 Дж/(кг×К);
Дж/(кг×К); 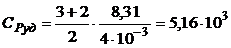 Дж/(кг×К).
Дж/(кг×К).
