Химические свойства полимеров
Химические свойства обусловлены наличием в составе их молекул двойных связей и функциональных групп. Поэтому отдельные макромолекулы могут сшиваться поперечными связями. При этом линейная структура молекул переходит в сетчатую. Такое явление имеет место при вулканизации каучука – взаимодействии с серой с образованием резины (0,5–5% S) или эбонита (≥ 20% S).
Полимеры могут подвергаться деструкции – разрушению под действием кислорода, света, радиации. Процесс ухудшения свойств полимера под действием деструкции называется старением полимера. Для замедления этого процесса в полимеры вводят стабилизаторы – антиоксиданты (фосфиты, фенолы, ароматические амины), т.е. вещества которые замедляют процессы окисления, взаимодействуя со свободными радикалами, образующимися в процессе окисления.
Электрические свойства полимеров
Электропроводность полимеров изменяется в широких пределах, что зависит от состава и структуры макромолекул, наличия, характера и концентрации полярных групп. Большинство полимеров являются диэлектриками, т.е. не проводят электрического тока. Наличие в макромолекулах галогенных, гидроксильных, карбоксильных и др. полярных групп ухудшает диэлектрические свойства. Хорошими диэлектриками являются такие полимеры как фторопласт, полиэтилен, полиизобутилен, полистирол. Диэлектрические свойства выше у полимеров с более высокой молекулярной массой. Повышение электрической проводимости наблюдается при переходе от стеклообразного состояния полимера к вязкотекучему.
Такие полимеры как полиацетилен (–СН=СН–)n, поливинилены (–HC=C<)n, полинитрилы (–HN=C<)n относятся к органическим полупроводникам. Полупроводниковые свойства этих полимеров определяются наличием нелокализованных π-электронов сопряженных двойных связей. В электрическом поле определенного напряжения эти электроны могут перемещаться вдоль цепи, обеспечивая перенос заряда. Их проводимость возрастает с увеличением температуры и при воздействии света. Проводимость их можно повысить при внедрении в состав полимера анионов, например, ClO4–, или катионов Li+ при электрохимическом окислении или восстановлении.
Применение и свойства некоторых полимеров приведены в приложении 13.
Контрольные вопросы
1. Дайте определение реакции полимеризации. Рассмотрите радикальный механизм полимеризации (инициирование, рост цепи, обрыв цепи) на примере получения поливинилхлорида.
2. Объясните механизм ионной полимеризации (катодной и анодной). Какие вещества можно использовать в качестве инициаторов ионной полимеризации?
3. Дайте определение реакции поликонденсации. Какие полимеры получают методом поликонденсации?
4. Дайте определение полимерам, олигомерам и мономерам. Как подразделяются полимеры?
5. Опишите строение, свойства, использование натурального каучука.
6. Опишите строение молекулы крахмала, его химические свойства и использование.
7. Опишите строение, физические и химические свойства молекул целлюлозы, применение целлюлозы для получения взрывчатых веществ и искусственных волокон.
8. Дайте характеристику белкам как высокомолекулярным веществам. Опишите строение и структуру белков, их функции в живом организме.
9. Опишите структуру полимеров: линейную (регулярную, нерегулярную) разветвленную, сетчатую. В чем состоит различие кристаллических и аморфных полимеров?
10. Опишите физические и химические свойства синтетических полимеров. Какое применение находят полимеры благодаря их свойствам?
Примеры выполнения заданий
Пример 1. Рассчитайте коэффициент полимеризации изобутилена при получении полиизобутилена с молярной массой полимера 56 280.
| Дано: Мп = 56 280 | Решение 1) Запишем уравнение получение полиизобутилена: |
| α - ? |
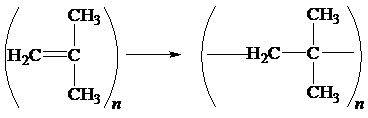
2) Рассчитаем молекулярную массу мономера, из которого состоит полимер:
Mм(C4H6) = 56 г/моль
3) Найдем степень полимеризации изобутилена по формуле:
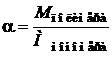
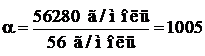
Ответ: α = 1005
Пример 2. Вычислить объем пропилена (при н.у.), затраченный для синтеза одной молекулы полипропилена со средней молекулярной массой 84 000? Какова степень полимеризации?
| Дано: Мср = 84 000 | Решение: 1) Вычислим молекулярную массу мономера: Мм(С3Н6) = 42 г/моль |
| V(–C3H6–) - ? |
2) Рассчитаем степень полимеризации:
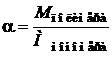 ,
,
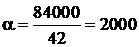
3) Найдем по соотношению объем пропилена:
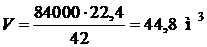 .
.
Ответ: α = 2000, V = 44,8 м3.
Пример 3.28,2 г фенола нагрели с избытком формальдегида в присутствии кислоты. При этом образовалось 5,116 г воды. Определите среднюю молярную массу полученного высокомолекулярного продукта реакции, считая, что поликонденсация протекает только линейно, и фенол полностью вступает в реакцию.
| Дано: m(C6H5OH) = 28,2 г m(H2O) = 5,116 г | Решение 1) Запишем уравнение линейной поликонденсации фенола и формальдегида: |
| Mср - ? |
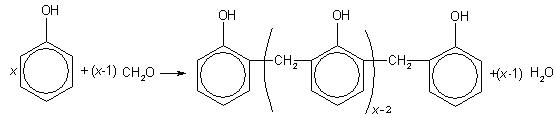
2) Найдем количество вещества фенола и воды:
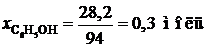
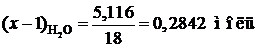
3) Найдем соотношение по уравнению количества воды и фенола:
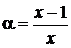 ,
,
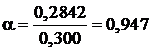 ,
,
откуда х = 19.
4) Молярная масса продукта конденсации равна:
М = М(С6Н4ОН) + (x-2)·M(СН2С6Н3ОН) + M(СН2С6Н4ОН)
М = 93 + 17·106 + 107 = 2002 г/моль.
Ответ: 2002 г/моль.
Задания для самостоятельной работы
Задание 1. Напишите структурные формулы предложенных веществ и составьте схемы полимеризации мономеров (с учетом возможности существования структурных и геометрических изомеров) и приведите названия полученных полимеров:
| № вар. | Названия веществ |
| этилен, хлоропрен | |
| пропилен, ε-аминокапроновая кислота | |
| стирол, 6-аминогексановая кислота | |
| винилхлорид, 1,3-бутадиен | |
| метилметакрилат, винилбензол | |
| тетрафторэтилен, этилакрилат | |
| акрилонитрил, n-метоксистирол | |
| бутен-2, хлоропрен | |
| 4-хлорбутадиен-1,3, винилхлорид | |
| n-метоксистирол, тетрафторэтилен | |
| этилакрилат, 4-хлорбутадиен-1,3, | |
| винилбензол, метилметакрилат | |
| 1,3-бутадиен, стирол | |
| 6-аминогексановая кислота, пропилен | |
| ε-аминокапроновая кислота, этилен |
Задание 2.Составьте структурные цепи полимеров и запишите уравнения реакций их получения с указанием названия исходных веществ:
| Вариант | Полимер | Вариант | Полимер |
| полиамид | полиуретан | ||
| капролактам | акрилонитрил | ||
| фенолформальдегид | капрон | ||
| лавсан | полистирол | ||
| полиметилметакрилат | капролактам | ||
| политетрафторэтилен | полиакрилонитрил | ||
| поливинилхлорид | полистирол | ||
| полиэтилен |
Задание 3. Решите расчетную задачу:
1. Определите массу ε-аминокапроновой кислоты в процессе производства капрона, если при этом выделилось 24 кг воды.
2. Рассчитайте объем бутана и массу стирола, необходимых для производства 50 кг бутанстирольного каучука, в котором соотношение бутандиеновых и стирольных звеньев равно 1 : 1.
3. 28,2 г фенола нагрели с избытком формальдегида в присутствии кислоты. При этом образовалось 5,116 г воды. Определите среднюю молярную массу полученного высокомолекулярного продукта реакции, считая, что поликонденсация протекает только линейно и фенол полностью вступает в реакцию.
4. Рассчитайте среднюю степень полимеризации природного каучука, если средняя молекулярная масса его составляет 200 тыс. г/моль.
5. При катионной полимеризации получен полимер с α = 5000. Как изменится α при уменьшении концентрации катализатора в 2 раза?
6. Рассчитайте степень полимеризации адипиновой кислоты, если получен полимер с молекулярной массой 13600.
7. Полимер массой 2 г поместили в склянку с бензином. Через 20 мин полимер вынули из склянки и взвесили, масса стала 2,5 г. Рассчитайте степень набухания.
8. Вычислите степень полимеризации полиэтилена и полипропилена, если молекулярные массы равны 50 000.
9. При набухании 200 г каучука поглотилось 964 мл хлороформа (плотность 1,9 г/мл). Рассчитайте степень набухания каучука и состав полученного студня (в массовых долях).
10. Найдите степень полимеризации полиметилметакрилата со средней молекулярной массой 60 000.
11. При набухании образца резины массой 50 г поглотилось 15 мл бензола (плотность 0,89 г/мл). Рассчитайте степень набухания резины.
12. Степень набухания полиамидного волокна капрон в воде составляет 10-12%. Как изменится при этом масса образца полимера от первоначального значения 75 г?
13. Степень набухания полиакрилонитрильного волокна в воде составляет 2%. Как изменится при этом масса образца полимера от первоначального значения 425 г?
14. Вычислить объём пропилена (н.у.), затраченный для синтеза одной молекулы полипропилена со средней молекулярной массой 84000? Какова степень полимеризации ?
15. Вычислите степень полимеризации полипропилена, если его молекулярная масса равна 10 000.
Тестовые задания для самоконтроля
1. Натуральный каучук получают из млечного сока:
1) одуванчика;
2) молочая;
3) гевеи.
2. Вулканизация натурального каучука состоит в его взаимодействии с:
1) серной кислотой;
2) оксидом серы (IV);
3) серой.
3. Полимер, продукт фотосинтеза у зеленых растений?
1) каучук;
2) крахмал;
3) ДНК.
4. Молекула крахмала состоит из остатков:
1) нециклической α-глюкозы;
2) циклической α-глюкозы;
3) циклической β-глюкозы.
5. Последовательность образования промежуточных продуктов при гидролизе крахмала:
1) декстрины – мальтоза – глюкоза;
2) мальтоза – декстрины – глюкоза;
3) глюкоза – мальтоза – декстрины.
6. Природный полимер, представляющий собой твердое волокнистое вещество, не растворяющееся в воде и других растворителях, – это:
1) крахмал;
2) целлюлоза;
3) белок.
7. Последовательность чередования различных аминокислотных звеньев в полипептидной цепи это … структура.
1) первичная;
2) вторичная;
3) третичная.
8. Стадия реакции полимеризации, представляющая собой образование активных радикалов из соединений со слабыми связями, - это:
1) инициирование;
2) рост цепи;
3) обрыв цепи.
9. Синтез полимеров из мономеров с двумя или несколькими функциональными группами, сопровождающийся образованием низкомолекулярных продуктов -
1) радикальная полимеризация;
2) ионная полимеризация;
3) поликонденсация.
Ответы к тестовым заданиям
| № вопроса | |||||||||
| № ответа |
Лабораторная работа № 14
Получение синтетических полимеров
Цель работы: получение полимеров.
Реактивы: метиловый эфир метакриловой кислоты, бензоил пероксид, HCl (конц.); C6H5OH (тв.), HCOH (р-р), уротропин, ацетон, вазелин.
Оборудование: пробирки и штатив для них, горелка, держатель, микрошпатель, стеклянная палочка, стеклянные стаканы, стекло или металлическая пластинка, водяная баня, вазелин.
Опыт1. Получение полимера (плексигласа)
Налейте в пробирку 2 мл метилового эфира метакриловой кислоты. В качестве инициатора добавьте 0,05 г перекиси бензоила. Нагрейте пробирку с содержимым на кипящей водяной бане, пока жидкость не примет сиропообразную консистенцию. После этого поместите пробирку в стакан с водой, нагретой до 60-70°С. Когда полимер затвердеет, разбейте пробирку и извлеките стекловидную массу полимера (плексигласа).
Опыт 2. Получение новолачной смолы
В пробирку поместите 2 г фенола (С6Н5ОН), прилейте 3-4 мл формалина (40% водный раствор НСОН) и добавьте 2-3 капли концентрированной соляной кислоты. Пробирку погрузите в кипящую водяную баню и время от времени перемешивайте содержимое пробирки стеклянной палочкой. Когда наступит бурная реакция (через 2-3 мин.) со вспениванием и последующим расслоением, верхний водяной слой сливают и образовавшуюся фенол-формальдегидную смолу «подсушивают», оставляя пробирку на 10 мин. в кипящей водяной бане. Затем смолу выгружают при помощи стеклянной полочки на пластинку и дают затвердеть при остывании на воздухе.
Остатки смолы в пробирке и на палочке растворите в 2-3 мл ацетона («Лак»). Полученным лаком покройте небольшую поверхность металла или дерева.
Запишите в журнале формулу новолачной смолы. Размягчается ли эта смола при нагревании? Как называют такие смолы?
Опыт 3. Получение резольной смолы
В пробирку поместите 2 г фенола и 0,7 г уротропина и слабо нагрейте в пламени горелки в течение 1-1,5 мин. до образования густой жидкости желтого цвета, при более длительном нагревании происходит осмоление с образованием продукта темно-красного цвета. При реакции наблюдается сильное вспучивание в результате выделение аммиака. Желтую жидкость вылейте на стекло, смазанное вазелином, или на металлическую пластинку. Происходит быстрое ее остывание и образуется прозрачная светло-желтая хрупкая термореактивная смола. Полученную смолу испытайте на излом. Какое свойство при этом обнаруживается?
Часть полученной смолы нагрейте. Плавится ли она при нагревании?
