Сульфат тетрааминмеди (II), гексахлороплатинат (IV) калия, тетрахлороамминакваплатина.
Ответ:
а) [Cu(NH3)4]SO4;
б) K2[PtCl6];
в) [PtNH3H2OCl4].
3. Записать выражение константы устойчивости комплексных ионов [Fe(CN)6]4-; [Pt(NH3)2Cl 2]2+.
Ответ:
Fe2+ + 6CN- <=> [Fe(CN)6]4-;
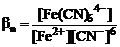 .
.
Pt4+ + 2NH3 + 2Cl- <=> [Pt(NH3)2Cl 2]2+;
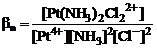 .
.
УРОВЕНЬ В
Определить заряд комплексного иона, степень окисления и координационное число комплексообразователя в каждом из соединений
K4[Mo(CN)8], [PtCl4(NH3)2].
Написать уравнения диссоциации этих соединений в водных растворах.
| Дано: K4[Mo(CN)8], [PtCl4(NH3)2] Заряд комплексного иона – ? | Решение: Диссоциация комплексных соединений протекает с отщеплением ионов внешней сферы по типу диссоциации сильных электролитов: K4[Mo(CN)8] = 4К+ + [Mo(CN)8]4-. |
| Меn+ – ? кч – ? |
Заряд комплексного иона [Mo(CN)8]4- равен суммарному заряду ионов внешней сферы, но противоположен ему по знаку.
Вторичная диссоциация комплексного иона обратима и протекает по типу диссоциации слабого электролита:
[Mo(CN)8]4- <=> Мох + 8 CN-.
Степень окисления комплексообразователя (х) определяется по заряду комплексного иона:
х
[Mo(CN)8] 4-.
х + 8·(–1) = –4, откуда х = + 4, т.е. заряд комплексообразователя Мо4+.
Координационное число комплексообразователя (Мо4+) равно суммарному числу лигандов (CN-), окружающих комплексообразователь, т.е. 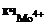 = 8.
= 8.
Так как соединение [PtCl4(NH3)2] не содержит внешней сферы, то его заряд равен нулю (неэлектролит) и для него наблюдается только вторичная диссоциация:
[Pt(NH3)2Cl4]0 <=> Рtx + 2NH 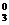 + 4Cl-.
+ 4Cl-.
x + 2 · 0 + 4 · (–1) = 0, x = +4,
т.е. заряд комплексообразователя Рt4+, а 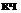 Pt4+ = 6.
Pt4+ = 6.
Ответ: [Mo(CN)8]4-,[PtCl4(NH3)2]0; Мо4+, Pt4+; 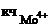 = 8;
= 8; 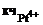 = 6.
= 6.
2. Константы нестойкости комплексных ионов [Fe(CN)6]4- и [Fe(CN)6]3- соответственно равны 1·10-37 и 1·10-44. Написать выражения констант нестойкости этих ионов и рассчитать константы их устойчивости. Какой из комплексных ионов является более прочным?
| Дано: [Fe(CN)6]4- [Fe(CN)6]3- | Решение Диссоциация комплексных ионов – процесс обратимый и количественно характеризуется константами нестойкости. [Fe(CN)6]4- <=> Fe2+ + 6CN-; |
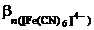 – ? – ?  – ? – ? |
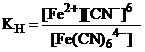 = 1·10-24;
= 1·10-24;
[Fe(CN)6]3- <=> Fe3+ + 6CN-;
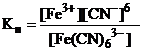 = 1·10-3.
= 1·10-3.
Константы устойчивости – константы равновесия обратных процессов (образования комплексных ионов).
Fe2+ + 6CN- <=> [Fe(CN)6]4-;
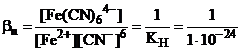 = 1024;
= 1024;
Fe3+ + 6CN- <=> [Fe(CN)6]3-;
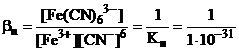 = 1031.
= 1031.
Значение константы устойчивости комплексного иона [Fe(CN)6]3- больше константы устойчивости комплексного иона [Fe(CN)6]4-. Значит, комплексный ион [Fe(CN)6]3- более прочный.
Ответ: комплексный ион [Fe(CN)6]3- более прочный.
3. Составить формулы следующих комплексных соединений с координационным числом платины (IV), равном шести: PtCl4·6NH3; PtCl4·4NH3; PtCl4·2NH3. Написать уравнения диссоциации этих солей в водном растворе и назвать их.
| Дано: PtCl4·6NH3 PtCl4·4NH3 PtCl4·2NH3 | Решение В состав внутренней сферы включается шесть лигандов. В первую очередь – молекулы аммиака и затем до координационного числа шесть – ионы хлора. Остальные ионы хлора образуют внешнюю сферу. |
| Комплексные соединения – ? |
PtCl4·6NH3 → [Pt(NH3)6]Cl4 = [Pt(NH3)6]4+ + 4Cl-;
[Pt(NH3)6]4+ <=> Pt4+ + 6NH3 ;
PtCl4·4NH3 → [Pt(NH3)4Cl2]Cl2 = [Pt(NH3)4Cl2]2+ + 2Cl- ;
[Pt(NH3)4Cl2]2+ <=> Pt4+ + 4NH3 + 2Cl-;
PtCl4 ·2NH3 → [Pt(NH3)2Cl4] <=> Pt4+ + 2NH3 + 4Cl- ;
[Pt(NH3)6]Cl4 – хлорид гексаамминплатины (IV);
[Pt(NH3)4Cl2]Cl2 – хлорид дихлоротетраамминплатины (IV);
[Pt(NH3)2Cl4] – тетрахлородиамминплатина.
УРОВЕНЬ С
1. Определить концентрацию ионов Ag+ в 0,01 M растворе K[Ag(CN)2], содержащем кроме того 0,05 моль/л NaCN. Константа устойчивости комплексного иона [Ag(CN)2]- равна 1·1021.
Дано: 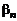 = 1·1021 = 1·1021 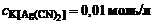 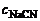 = 0,05 моль/л = 0,05 моль/л | Решение Равновесную концентрацию ионов Ag+ можно определить из выражения константы устойчивости комплексного иона: |
| [Ag+] – ? |
Ag+ + 2CN- <=> [Ag(CN)2]-. (13.1)
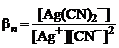 = 1·1021 . (13.2)
= 1·1021 . (13.2)
Введение в раствор комплексной соли сильного электролита NaCN, который диссоциирует по уравнению
NaCN = Na+ + CN- ,
приводит согласно принципу Ле-Шателье к смещению равновесия уравнения (13.1) в сторону образования комплексного иона, и устанавливается новое равновесие. Значение βn при этом не изменяется.
Обозначим равновесную концентрацию ионов серебра в новых условиях через х:
[Ag+] = х, моль/л.
Общая равновесная концентрация [CN-] равна сумме концентраций CN-, образовавшихся при диссоциации NaCN и [Ag(CN)2]-:
[CN-] = 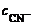 +
+ 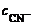 ;
;
из [Ag(CN)2]- из NaCN
из [Ag(CN)2]- 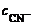 = 2х, моль/л;
= 2х, моль/л;
из NaCN 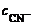 =
= 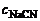 · α ·
· α · 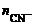 .
.
так как NaCN сильный электролит, α = 1, 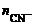 = 1, то
= 1, то 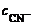 =
=
= 0,05 моль/л. Тогда
[CN-] = (2х + 0,05), моль/л.
Концентрацию иона [Ag(CN)2]- определяем из уравнения первичной диссоциации
K[Ag(CN)2] = К+ + [Ag(CN)2]- .

 · α · n; α = 1, так как первичная диссоциация протекает по типу диссоциации сильных электролитов, n = 1:
· α · n; α = 1, так как первичная диссоциация протекает по типу диссоциации сильных электролитов, n = 1:
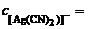 0,01 моль/л.
0,01 моль/л.
Тогда равновесная концентрация иона [Ag(CN)2-]
[Ag(CN)2-] = (0,01 – х) моль/л.
Подставляем полученные данные в выражение (13.2):
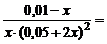 1·1021 .
1·1021 .
Так как х << 0,01, то значением х ввиду его малого значения в выражении (0,01 – х) и значением 2х в выражении (0,05 + 2х) можно пренебречь и записать данное выражение в виде
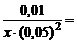 1·1021,
1·1021,
откуда х = 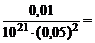 4·10-21 моль/л.
4·10-21 моль/л.
[Ag+] = 4·10-21 моль/л.
Ответ: [Ag+] = 4·10-21 моль/л.
2. Выпадает ли осадок NiS, если к 1М раствору [Ni(NH3)6]Cl2 прилить равный объем 0,005М раствора K2S?
К Н 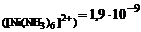 (таблица)
(таблица) 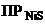 = 1·10-9(таблица)
= 1·10-9(таблица)
Дано: 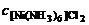 = 1 моль/л = 1 моль/л 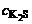 = 0,005 моль/л ПРNiS = 1·10-9 К Н = 0,005 моль/л ПРNiS = 1·10-9 К Н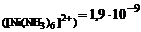 | Решение Осадок NiS образуется, если 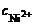 · · 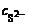 > ПРNiS. Концентрацию иона Ni2+ определяем по концентрации раствора [Ni(NH3)6]Cl2. > ПРNiS. Концентрацию иона Ni2+ определяем по концентрации раствора [Ni(NH3)6]Cl2. |
| Выпадает ли осадок NiS? |
Комплексная соль [Ni(NH3)6]Cl2 диссоциирует по уравнению
[Ni(NH3)6]Cl2 = [Ni(NH3)6]2+ + 2Cl– (первичная диссоциация). (13.3)
Из уравнения (13.3) определяем концентрацию комплексного иона:
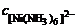 =
= 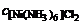 · α · n = 1 моль/л.
· α · n = 1 моль/л.
где α = 1; n = 1.
Комплексный ион в свою очередь диссоциирует равновесно:
[Ni(NH3)6]2+ <=> Ni2+ + 6NH3 (вторичная диссоциация). (13.4)
Обозначим равновесную концентрацию ионов никеля через х:
[Ni2+] = х, моль/л.
Тогда, согласно уравнению (13.4):
[NH3] = 6х, моль/л;
[Ni(NH3)62+] = (1 – х) моль/л.
Константа нестойкости комплексного иона из уравнения (13.4)
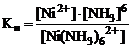 . (13.5)
. (13.5)
Подставим полученные данные в выражение (13.5):
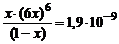 .
.
Так как х << 1, то значением х ввиду его малого значения в выражении (1 – х) можно пренебречь и данное выражение записать в виде
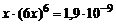 ,
,
откуда х = 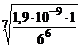 = 0,243 моль/л.
= 0,243 моль/л.
[Ni2+] = с 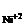 = 0,243 моль/л.
= 0,243 моль/л.
Из уравнения диссоциации
K2S = 2K+ + S2-
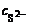 = с
= с 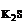 ·α·
·α· 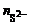 = 0,005 · 1 · 1 = 5·10-3 моль/л,
= 0,005 · 1 · 1 = 5·10-3 моль/л,
где α = 1; 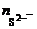 = 1.
= 1.
При сливании равных объемов растворов солей K2S и [Ni(NH3)6]Cl2 концентрация всех ионов уменьшится в 2 раза и составит:
с 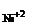 = ½ · 0,243 = 0,1215 моль/л;
= ½ · 0,243 = 0,1215 моль/л;
с 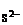 = ½ · 5 · 10-3 = 0,0025 моль/л.
= ½ · 5 · 10-3 = 0,0025 моль/л.
Произведение с 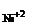 ·с
·с 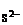 = 0,1215 · 0,0025 = 3·10-4, т.к. 3·10-4 > 1·10-9 (табличная величина ПРNiS), то осадок NiS выпадает.
= 0,1215 · 0,0025 = 3·10-4, т.к. 3·10-4 > 1·10-9 (табличная величина ПРNiS), то осадок NiS выпадает.
Ответ: осадок NiS выпадает.
3. К раствору, содержащему 0,2675 г комплексной соли
CoCl3·6NH3. добавили в достаточном количестве раствор AgNO3. Масса осажденного AgCl составила 0,4305 г. Определить координационную формулу соли, назвать её и написать уравнения диссоциации в водном растворе.
Дано: 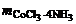 = 0,2675 г = 0,2675 г 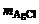 = 0,4305 г = 0,4305 г | Решение Для написания координационных формул необходимо знать состав внутренней и внешней сферы этой соли. Из раствора комплексной соли можно осадить в виде AgCl↓, только ионы Cl-, входящие во внешнюю сферу. |
| Формула комплексной соли – ? |
Таким образом, в состав осадка (AgCl) входят ионы Cl-, находящиеся только во внешней сфере комплексной соли.
Обозначим число ионов Cl- во внешней сфере комплексной соли n.
Тогда число ионов Cl- во внутренней сфере комплексной соли (3 – n).
При добавлении к раствору комплексной соли раствора AgNO3протекает реакция
[Co(NH3)6Cl(3-n)]Cln + nAgNO3 = nAgCl↓ + [Co(NH3)6Cl(3-n)](NO3)n .
Поскольку в молекуле AgCl на 1 ион Ag+ приходится 1 ион Cl- , то из одной молекулы комплексной соли образуется n молекул AgCl.
[Co(NH3)6Cl(3-n)]Cln – nAgCl
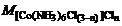 – nMAgCl
– nMAgCl
267,5 г – n143,5 г
0,2675 г – 0,4305 г
n = 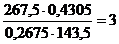 .
.
Следовательно, все три иона Cl- находятся во внешней сфере. Формула комплексной соли [Co(NH3)6]Cl3.
Первичная диссоциация соли
[Co(NH3)6]Cl3 = [Co(NH3)6]3+ + 3Cl- .
Вторичная диссоциация:
[Co(NH3)6]3+ <=> Co3+ + 6NH 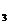 .
.
[Co(NH3)6]Cl3 – хлорид гексаaмминкобальта (III).
Ответ: [Co(NH3)6]Cl3.
ЖЕСТКОСТЬ ВОДЫ
УРОВЕНЬ А
1. Какие из указанных соединений: Fe(HCO3)2, CaCl2, MgSO4, Ca(HCO3)2, Fe(NO3)2, Mg(HCO3)2, обусловливают:
а) постоянную жесткость воды;
б) временную жесткость воды?
Ответ: а) постоянная (некарбонатная) жесткость воды обусловлена присутствием в воде CaCl2, MgSO4, Fe(NO3)2;
б) временная (карбонатная) жесткость воды обусловлена присутствием в воде гидрокарбонатов Fe(HCO3)2, Ca(HCO3)2, Mg(HCO3)2.
2. Какие из указанных уравнений реакций протекают при устранении временной жесткости воды:
а) MgCl2 + Na2CO3 + H2O = Mg(OH)2↓+ 2NaCl + CO2↑;
б) 3CaSO4 + 2Na3PO4 = Ca3(PO4)2↓ + 3Na2SO4;
в) Fe(HCO3)2 + 2Ca(OH)2 = Fe(OH)2↓ + 2CaCO3↓ + 2H2O;
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3↓?
Ответ: для устранения временной жесткости в воду добавляют гашеную известь Сa(OH)2; при этом протекает реакция.
Fe(HCO3)2 +2Ca(OH)2 = Fe(OH)2↓ + 2CaCO3↓ + 2H2O:
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3↓ (вторичный процесс).
3. Какие из указанных уравнений реакций протекают при устранении постоянной жесткости воды:
а) Mg(HCO3)2 + 2Ca(OH)2 = Mg(OH)2↓+ 2CaCO3↓ + 2H2O;
б) CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4;
в) Ca(HCO3)2 = CaCO3↓ + CO2↑ + H2O?
Ответ: для устранения постоянной жесткости в воду добавляют техническую соду (Na2CO3), при этом протекает реакция
б) CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4 .
УРОВЕНЬ В
