Протекающей при стандартных условиях.
| Дано: Уравнение реакции | Решение Записываем реакцию в ионном виде: |
| Кс – ? |
Feo(к) + Cu+2(р-р) + SO 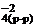 <=> Fe+2(р-р) + SO
<=> Fe+2(р-р) + SO 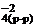 + Cuo(к) – полное ионное уравнение.
+ Cuo(к) – полное ионное уравнение.
Cu+2(р-р) + Feo(к) < = > Fe+2(р-р) + Cu0(к) – сокращенное ионное уравнение
НОК ДМ

 окис-ль Сu+2 + 2ē = Cu 1
окис-ль Сu+2 + 2ē = Cu 1 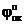 = 0,34 В (см. табл. 11.1)
= 0,34 В (см. табл. 11.1)
 восст-ль Fe0 – 2ē = Fe+2 1
восст-ль Fe0 – 2ē = Fe+2 1 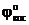 = –0,44 В (см. табл. 11.1)
= –0,44 В (см. табл. 11.1)
Cu+2 + Fe0 = Cu0 + Fe+2
ε0 = 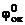 –
– 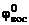 ; ε0 = 0,34 – (–0,44) = 0,78 В.
; ε0 = 0,34 – (–0,44) = 0,78 В.
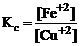 .
.
Так как приведенная реакция является окислительно-восстанови-тельной, то
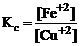 =
= 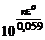 ,
,
где n – НОК.
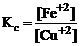 =
= 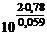 = 1026
= 1026
Высокое значение Кс свидетельствует о прктически полном смещении равновесия вправо.
Ответ: Кс = 1026
УРОВЕНЬ С
1. Определить состав смеси (% масс.) карбоната магния и оксида магния, если при прокаливании смеси получено 40 см3 оксида углерода (IV) (н.у.), а при взаимодействии продукта, полученного после прокаливания, с ортофосфорной кислотой получено 0,8 г ортофосфата магния. Составить уравнения реакций.
Дано: MgO и MgCO3 V 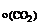 = 40 см3 m = 40 см3 m 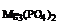 = 0,8 г = 0,8 г | Решение: mсмеси = m(MgO)исх + 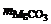 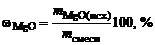 мас. мас. 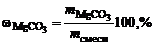 мас. мас. |
ω 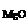 – ? ω – ? ω 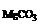 – ? – ? |
Массу MgCO3 в смеси определяем используя уравнение реакции, протекающей при прокаливании:
MgCO3 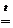 MgO + CO2 . (12.1)
MgO + CO2 . (12.1)
84,3 г 22,4 л
m  0,04 л,
0,04 л,
где 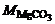 = 84,3 г/моль, V
= 84,3 г/моль, V 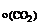 = 0,04 л,
= 0,04 л,
откуда
m 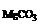 =
= 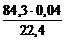 = 0,15 г.
= 0,15 г.
Используем уравнение (12.1) также для расчета mMgO, полученного по реакции (12.1):
MgCO3 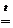 MgO + CO2
MgO + CO2
84,3 г 40,3 г
0,15 mMgO, уравнения (12.1),
где 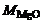 = 40,3 г/моль,
= 40,3 г/моль,
откуда mMgO (12.1) = 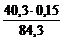 = 0,07 г.
= 0,07 г.
После прокаливания смесь состоит только из MgО (mMgO(общ) =
= mMgO (12.1) + mMgO(исх)).
При взаимодействии продукта, полученного после прокаливания с ортофосфорной кислотой, протекает реакция
3MgO + 2H3PO4 = Mg3(PO4)2 + 3H2O.
Составляем пропорцию:
3∙ 40,3 г 262,9 г
mMgO(общ) 0,8 г,
где МMgО = 40,3 г/моль, М 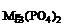 = 262,9 г/моль,
= 262,9 г/моль,
откуда mMgO(общ) = 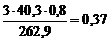 г.
г.
mMgO(исх) = mMgO(общ) – mMgO (12.1) = 0,37 – 0,07 = 0,3 г.
Таким образом
mсмеси = mMgO(исх) + 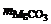 = 0,30 + 0,15 = 0,45 г.
= 0,30 + 0,15 = 0,45 г.
Состав исходной смеси
ω 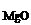 =
= 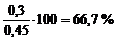 мас.
мас.
ω  = 100 – 66,7 = 33,3 % мас.
= 100 – 66,7 = 33,3 % мас.
2. Составить схему получения металлического кадмия из 10 г смеси оксидов CdO и ZnO гидрометаллургическим методом.
В качестве растворителя оксидов использовать разбавленную серную кислоту. Определить состав смеси (% мас.) и массу полученного кадмия, если в качестве восстановителя CdO использовали СО, а объем образовавшегося СО2 составляет 300 см3 (н.у.).
Дано: mCdO + ZnO = 10 г V 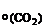 = 300 см3 = 300 см3 | Решение Составляем схему разделения оксидов и записываем уравнения реакций по стадиям: 1. Растворение оксидов кадмия и цинка в H2SO4: |
ω 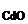 – ? ω – ? ω 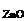 – ? mCd – ? – ? mCd – ? |
CdO + H2SO4 = CdSO4 + H2O;
ZnO + H2SO4 = ZnSO4 + H2O.
2. Осаждение гидроксидов кадмия и цинка гидроксидом натрия при стехиометрическом соотношении солей и гидроксида натрия:
CdSO4 + 2NaOH = Cd(OH)2↓ + Na2SO4;
ZnSO4 + 2NaOH = Zn(OH)2↓ + Na2SO4.
3. Растворение амфотерного гидроксида цинка в избытке щелочи:
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4].
избыток растворимая соль
Так как Na2[Zn(OH)4] – растворимая соль, то в осадке остается только гидроксид кадмия.
4. Отделение осадка Cd(OH)2 от раствора фильтрацией, промывка, сушка.
5. Разложение осадка Cd(OH)2 при нагревании:
Cd(OH)2 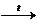 СdO + H2O↑.
СdO + H2O↑.
6. Восстановление CdO оксидом углерода (II) при нагревании:
CdO + CO 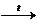 Cd + CO2.
Cd + CO2.
112,4 г 22,4 л
mCd 0,3 л,
где mCd = 112,4 г/моль,
откуда
m 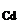 =
= 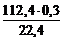 = 1,5 г.
= 1,5 г.
Определяем содержание СdO в смеси:
CdO Cd
128,4г 112,4 г
mCdO 1,5 г,
где MCdO = 128,4 г/моль,
откуда m 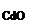 =
= 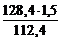 = 1,71 г.
= 1,71 г.
Определяем
ω 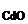 =
= 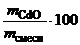 =
= 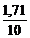 ·100 = 17,1 %.
·100 = 17,1 %.
ω 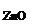 = 100 – 17,1 = 82,9 %.
= 100 – 17,1 = 82,9 %.
Ответ: ω 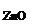 = 82,9 %, ω
= 82,9 %, ω 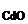 = 17,1 %; m
= 17,1 %; m 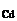 = 1,5 г.
= 1,5 г.
3. При растворении 0,5 г алюминиевой бронзы, состоящей из меди и алюминия, в хлороводородной кислоте выделилось 43,56 см3 водорода, собранного над водой и измеренного при 300 К и
740 мм рт. ст. Давление паров воды при 300 К равно 26,74 мм рт. ст. Определить состав сплава (% мас.).
Дано: mбронзы = 0,5 г HCl – растворитель V 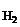 = 43,56 см3 Т = 300 К Р = 740 мм рт. ст. Р = 43,56 см3 Т = 300 К Р = 740 мм рт. ст. Р 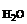 = 26,74 мм рт. ст. = 26,74 мм рт. ст. | Решение В соответствии со следствием из ряда стандартных электродных потенциалов металлов в хлороводородной кислоте могут растворяться только те металлы, у которых 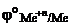 < 0. < 0. |
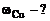 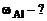 |
Определяем стандартные электродные потенциалы:
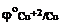 = + 0,34 В,
= + 0,34 В, 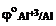 = –1,67 В.
= –1,67 В.
Следовательно, в хлороводородной кислоте из сплава будет растворяться только алюминий.
Уравнение реакции имеет вид
Al + HCl = AlCl3 + H2↑.
 НОК ДМ
НОК ДМ
Al – 3e = Al3+ 1 2
H+ + e = H 3 6
 2Al + 6H+ = 2Al3+ + 3H2
2Al + 6H+ = 2Al3+ + 3H2
2Al + 6HCl = 2AlCl3 + 3H2↑.
Массу алюминия в сплаве можно рассчитать по полученному уравнению реакции:
2МAl – 3 · 22400 см3 Н2.
mAl – 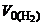 .
.
Откуда
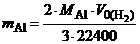 , (12.2)
, (12.2)
где МAl = 27 г/моль
Объем водорода при н.у. 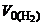 рассчитываем по объединенному уравнению газового состояния:
рассчитываем по объединенному уравнению газового состояния:
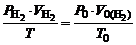 .
.
Откуда
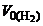 =
= 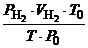 =
=
= 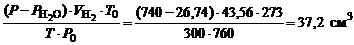 .
.
где 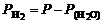 .
.
Подставляя величину 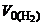 в формулу (12.2), получаем
в формулу (12.2), получаем
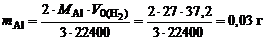 .
.
Рассчитываем содержание металлов в сплаве:
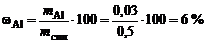 мас.
мас.
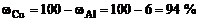 мас.
мас.
Ответ: 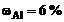 мас.,
мас., 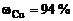 мас.
мас.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
УРОВЕНЬ А
1. Назвать следующие комплексные соединения: K3[Fe(CN)6]; [PtCl 3(NH3)3]Cl; [Co(NO2)3(NH3)3].
Ответ:
а) K3[Fe(CN)6] – гексацианоферрат (III) калия.
б) [Pt(NH3)3Cl 3]Cl – хлорид трихлоротриамминплатины (IV).
в) [Co(NH3)3(NO2)3] – тринитротриамминкобальт.
2. Написать формулы следующих химических соединений:
