Ответ обосновать значениями стандартных электродных потенциалов.
Ответ: по табл. 11.1 определяем стандартные электродные потенциалы титана, никеля, меди, цинка и железа (II):
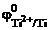 = –1,63 В;
= –1,63 В; 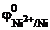 = -0,25 В;
= -0,25 В; 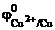 = +0,34 В;
= +0,34 В;
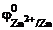 = –0,76В;
= –0,76В; 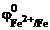 = –0,44 В.
= –0,44 В.
Так как анодную защиту железной детали можно осуществить металлами с 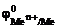 <
< 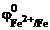 , то искомыми металлами являются а) Ti ; г) Zn.
, то искомыми металлами являются а) Ti ; г) Zn.
2. Написать уравнение Нернста для определения электродного потенциала металлического и водородного электродов. Указать единицы измерения.
Ответ: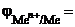
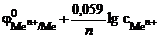 , В;
, В;
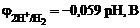 .
.
3. Из приведенного ряда металлов выбрать те, которые могут служить катодом при стандартных условиях в гальванических элементах, анод у которых цинковый: а) Mn; б) Bi; в) Al; г) Sn.
Ответ обосновать значениями стандартных электродных потенциалов.
Ответ: по табл. 11.1 определяем стандартные электродные потенциалы марганца, висмута, алюминия, олова и цинка:
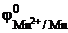 = –1,05 В;
= –1,05 В; 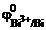 = + 0,23 В;
= + 0,23 В; 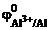 = –1,67 В;
= –1,67 В; 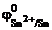 =
=
= –0,14 В; 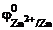 = –0,76 В.
= –0,76 В.
Так как катодом при стандартных условиях в гальванических элементах, анод у которых цинковый, могут служить металлы с 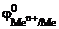 >
> 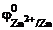 , то искомыми металлами являются б) Bi; г) Sn.
, то искомыми металлами являются б) Bi; г) Sn.
УРОВЕНЬ В
1. а) Алюминиевый электрод погружен в 5∙10-4 М раствор сульфата алюминия. Вычислить значение электродного потенциала алюминия.
Дано: Металл – Al 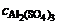 = 5∙10-4 моль/л = 5∙10-4 моль/л | Решение Электродный потенциал алюминия рассчитываем по уравнению Нернста: 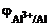 = = 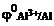 + + 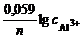 |
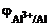 –? –? |
По табл. 11.1 определяем стандартный электродный потенциал алюминия:
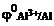 = –1,67 В.
= –1,67 В.
Записываем уравнение электродного процесса, протекающего на поверхности алюминиевого электрода в растворе соли:
Al – 3ē = Al3+.
n – число электронов, участвующих в электродном процессе.
Для данной реакции n равно заряду иона алюминия Al3+(n = 3). Рассчитываем концентрацию ионов алюминия в растворе Al2(SO4)3:
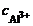 =
= 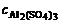 ∙ α ∙
∙ α ∙ 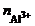 .
.
Разбавленный раствор Al2(SO4)3 – сильный электролит.
Следовательно, α = 1. По уравнению диссоциации Al2(SO4)3.
Al2(SO4)3 = 2Al3+ + 3SO 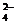
число ионов Al3+, образующихся при диссоциации одной молекулы Al2(SO4)3, равно 2.
Следовательно, 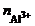 = 2.
= 2.
Тогда 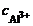 = 5∙10-4∙1∙2 =
= 5∙10-4∙1∙2 = 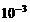 моль/л.
моль/л.
Рассчитываем электродный потенциал алюминиевого электрода:
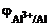 = -1,67 +
= -1,67 + 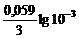 = –1,73 В.
= –1,73 В.
Ответ: 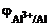 = –1,73 В.
= –1,73 В.
б) Потенциал цинкового электрода, погруженного в раствор своей соли, равен –0,75 В. Вычислить концентрацию ионов цинка в растворе.
Дано: Металл – Zn 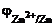 = –0,75 В = –0,75 В | Решение Электродный потенциал цинка рассчитываем по уравнению Нернста: 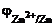 = = 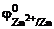 + + 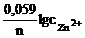 . . |
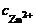 – ? – ? |
Откуда:
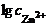 =
= 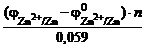
По табл. 11.1 определяем стандартный электродный потенциал цинка:
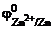 = 0,76 В, n – равно заряду иона цинка Zn2+ (n = 2).
= 0,76 В, n – равно заряду иона цинка Zn2+ (n = 2).
Тогда
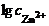 =
= 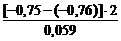 = 0,338.
= 0,338.
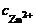 = 100,339 моль/л = 2,18 моль/л
= 100,339 моль/л = 2,18 моль/л
Ответ: 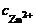 = 2,18 моль/л.
= 2,18 моль/л.
Составить две схемы гальванических элементов (ГЭ), в одной из которых олово служило бы анодом, в другой – катодом. Для одной из них написать уравнения электродных процессов и суммарной токообразующей реакции. Вычислить значение стандартного напряжения ГЭ.
Решение
В гальваническом элементе анодом является более активный металл с меньшим алгебраическим значением электродного потенциала, катодом – менее активный металл с большим алгебраическим значением электродного потенциала.
По табл. 11.1 находим 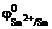 = –0,14 В.
= –0,14 В.
а) Олово является анодом ГЭ.
В качестве катода можно выбрать любой металл с 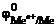 >
> 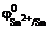 .
.
Выбираем медь 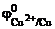 = + 0,34 В. В паре Sn–Cu олово будет являться анодом ГЭ, медь – катодом. Составляем схему ГЭ:
= + 0,34 В. В паре Sn–Cu олово будет являться анодом ГЭ, медь – катодом. Составляем схему ГЭ:
А(-) Sn │ Sn2+ ││ Cu2+ │ Cu(+)K
или
А(-) Sn │ SnSO4 ││ CuSO4 │ Cu(+)K.
Уравнения электродных процессов:
НОК ДМ
 На A(-) Sn – 2ē = Sn2+ 1 – окисление
На A(-) Sn – 2ē = Sn2+ 1 – окисление
На К(+) Cu2+ + 2ē = Cu 1 – восстановление
 |
Sn + Cu2+ = Sn2+ + Cu – суммарное ионно-молекулярное уравнение токообразующей реакции;
Sn + CuSO4 = SnSO4 + Cu – суммарное молекулярное уравнение токообразующей реакции.
Рассчитываем стандартное напряжение ГЭ:
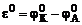 =
= 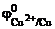 –
– 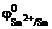 = +0,34 – (–0,14) = 0,48 В.
= +0,34 – (–0,14) = 0,48 В.
б) Олово является катодом ГЭ.
В качестве анода ГЭ можно выбрать любой металл с 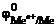 <
< 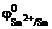 , кроме щелочных и щелочноземельных металлов, так как они реагируют с водой.
, кроме щелочных и щелочноземельных металлов, так как они реагируют с водой.
Выбираем магний 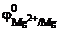 = –2,37 В.
= –2,37 В.
В паре Mg–Sn магний является анодом, олово – катодом.
Составляем схему ГЭ:
А(-) Mg │ Mg2+ ││ Sn2+ │ Sn(+)K
или
А(-) Mg │ MgSO4 ││ SnSO4 │ Sn(+)K.
3. Составить схему коррозионного гальванического элемента, возникающего при контакте железа с цинком:
а) в атмосферных условиях (Н2О + О2);
б) кислой среде (Н2SO4);
в) кислой среде в присутствии кислорода (HCl + O2).
