Реакция между веществами А и В описывается уравнением
А(г) + 2В(г) = 2С(г).
Константа скорости этой реакции равна 0,1. Начальные концентрации реагирующих веществ со(А) = 0,4 моль/л, со(В) = 0,8 моль/л. Вычислить начальную скорость реакции и определить во сколько раз она изменится, если концентрация вещества А уменьшится на 0,1 моль/л.
Дано: Уравнение реакции, К = 0,1 с 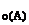 = 0,4 моль/л с = 0,4 моль/л с 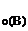 = 0,8 моль/л с = 0,8 моль/л с 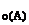 уменьшается на 0,1 моль/л уменьшается на 0,1 моль/л | Решение В простейших одностадийных реакциях скорость пропорциональна концентрациям реагирующих веществ в степенях, равных их стехиометрическим коэффициентам в уравнении реакции. 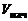 = K·с = K·с 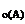 · · 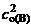 = = 0,1∙0,4·0,82 = = 0,0256 моль/(л∙с). = = 0,1∙0,4·0,82 = = 0,0256 моль/(л∙с). |
Vнач – ? 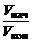 = ? = ? |
Исходные вещества реагируют между собой согласно стехиометрическим коэффициентам в уравнении реакции.
1моль А – 2 моль В
0,1 моль А – х моль В
х = 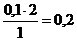 моль.
моль.
Следовательно, уменьшение концентрации вещества А на 0,1 моль/л сопровождается уменьшением концентрации вещества В на 0,2 моль/л, тогда:
Vкон = К·сА· 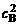 .
.
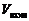 = 0,1(0,4 – 0,1)(0,8 – 0,2)2 = 0,0108 моль/(л·с).
= 0,1(0,4 – 0,1)(0,8 – 0,2)2 = 0,0108 моль/(л·с).
В связи с уменьшением концентрации реагирующих веществ в ходе реакции скорость реакции уменьшается:
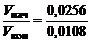 = 2,37,
= 2,37,
т.е. скорость реакции уменьшилась в 2,37 раза.
Ответ: 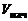 = 0,0256 моль/(л∙с).
= 0,0256 моль/(л∙с).
При уменьшении концентрации вещества А на 0,1 моль/л, скорость реакции уменьшилась в 2,37 раза.
2. Энергия активации некоторой реакции равна 60 кДж/моль. Во сколько раз изменится скорость реакции: а) при повышении температуры от 320 до 360 К? б) если она протекает при 298 К в присутствии катализатора (Еак (кат)= 48 кДж/моль)?
Дано: Еак = 60 кДж/моль а) Т1 = 320 К, Т2 = 360 К б) Т = 298 К, 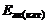 = 48кДж/моль = 48кДж/моль | Решение а) Из уравнения Аррениуса получаем 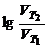 = = 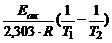 ; ; 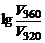 = = 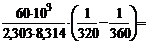 1,09, где 103 – коэффициент пересчета килоджоулей в джоули, тогда 1,09, где 103 – коэффициент пересчета килоджоулей в джоули, тогда 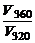 =101,09 = 12,3 раза. =101,09 = 12,3 раза. |
а) 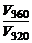 – ? б) – ? б) 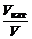 – ? – ? |
б) Зависимость скорости реакции от наличия катализатора выражается уравнением
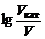 =
= 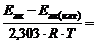
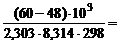 2,103,
2,103,
откуда 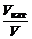 = 101,03= 127.
= 101,03= 127.
Ответ:
а) при повышении температуры от 320 до 360 К скорость реакции возрастает в 12,3 раза;
б) в присутствии катализатора скорость реакции возрастает в 127 раз.
3. Используя справочные данные по ΔfHº(298 K) и Sº(298 K) веществ, определить температуру, при которой константа равновесия реакции CO2(г) + C(к) <=> 2CO(г) равна единице. Записать выражение для константы равновесия данной реакции.
| Дано: Уравнение реакции, Кр = 1 | Решение CO2(г) + C(к) <=> 2CO(г), 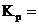 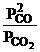 . . |
| Т – ? |
Твердые вещества в выражение Кр не включаются.
Значения ΔfHº(298 K) и Sº (298 K) веществ берем из таблицы.
| CO2(г) + | C(к) = | 2CO(г) | |
| ΔfHº(298K), кДж/моль | –393,5 | 2∙(–110,5) | |
| Sº(298K), Дж/(моль·К) | 213,7 | 5,7 | 2∙(197,5) |
ΔrHº(298 K) – TΔrSº (298 K) = –2,303RTlgKp.
По условию Кр = 1, следовательно, lgKp = 0, тогда
ΔrH°(298 K) – TΔrS°(298 K) = 0,
T = 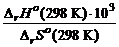 ,
,
где 103 – коэффициент пересчета килоджоулей в джоули.
ΔrHº(298 K) = 2ΔfHº(298 K, CO(г)) – [ΔfHº(298 K, CO2(г)) +
+ ΔfHº(298 K, Cк)]
ΔrHº(298 K) = 2(–110,5) – [(–393,5) + 0] = 172,5 кДж.
ΔrSº(298 K) = 2 Sº(298 K, CO(г)) – [Sº(298 K, CO2(г)) + Sº(298 K, C(k))] =
= 2·197,5 – (213,7 + 5,74) = 175,56 Дж/К.
Т = 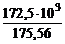 = 982,6 K.
= 982,6 K.
Ответ: Кр = 1 при 982,6 К.
УРОВЕНЬ С
1. Определить значения ΔrН°(298 К) и ΔrS°(298 К) процесса испарения бромида бора, если при температурах (-10 ºС) и (+91 ºС) давления насыщенных паров соответственно равны 10 и 760 мм рт.ст.
Дано: 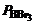 = 10 мм рт.ст. при t = –10 °С = 10 мм рт.ст. при t = –10 °С 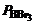 = 760 мм рт.ст. при t = 91 °С = 760 мм рт.ст. при t = 91 °С | Решение Для процесса испарения бромида бора BBr3(ж) <=> BBr3(г). Константа равновесия Кр равна относительному давлению пара (атм.), – безразмерная величина: |
| ΔrН°(298 К) – ? ΔrS°(298 К) – ? |
Кр = 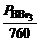 .
.
Константа равновесия связана с термодинамическими характеристиками следующим соотношением:
–19,15·T·lgKр = ΔrНº(298 К) – T ΔrSº(298 К).
Зная константы равновесия при двух абсолютных температурах, составляем систему уравнений:
–19,15·263·lg 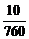 = ΔrНº(298 К) – 263ΔrSº(298 К).
= ΔrНº(298 К) – 263ΔrSº(298 К).
–19,15·364·lg 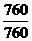 = ΔrНº(298 К) – 364ΔrSº(298 К).
= ΔrНº(298 К) – 364ΔrSº(298 К).
Вычисляем левые части обоих уравнений:
9467,68 = ΔrНº(298 К) – 263 ΔrSº(298 К).
0 = ΔrНº(298 К) – 364ΔrSº(298 К).
Из 2-го уравнения выражаем ΔrНº(298 К) = 364ΔrSº(298 К) и подставляем в 1-ое уравнение
9467,68 = 364ΔrSº(298 К) – 263 ΔrSº(298 К).
Откуда ΔrSº(298 К) = 93,74 Дж/К.
Полученное значение ΔrSº(298К) подставляем в уравнение
0 = ΔrНº(298 К) – 364(93,74).
Откуда ΔrНº(298 К) = 34,12 кДж.
Ответ: ΔrНº(298 К) = 34,12 кДж.
ΔrSº(298 К) = 93,74 Дж/К.
2. На основании принципа Ле Шателье определить, в каком направлении сместится равновесие в следующей системе:
2SO2(г) + O2(г) <=> 2SO3(г), ΔrHº(298 K) = -284,2 кДж,
при: а) понижении температуры; б) повышении концентрации SO3; в) повышении давления.
