Опыт 1. Бромирование предельных углеводородов.
В две пробирки поместите 3-4 мл циклогексана, добавьте 4-5 капель раствора брома в четыреххлористом углероде и перемешайте. Одну пробирку накройте колпачком из черной бумаги. Поставьте обе пробирки под источник УФ-света. Через 3-4 мин облучения снимите черный колпачок и сравните обе пробирки. На свету раствор брома обесцвечивается.
Схема реакции монобромирования циклогексана:
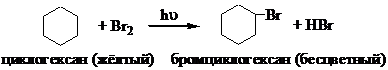
Вопросы:
1. Почему для проведения реакции бромирования циклогексана необходимо облучение УФ-светом?
2. Опишите по стадиям механизм реакции.
Опыт 2. Бромирование непредельных углеводородов.
В пробирку поместите 2-3 капли бромной воды, добавьте по каплям циклогексен до обесцвечивания раствора. Параллельно проведите аналогичный опыт с циклогексаном. Обесцвечивание не наблюдается.
Схема реакции:
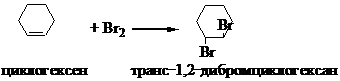
Вопросы:
1. Для каких целей используется данная реакция в качественном анализе?
2. Опишите механизм и обьясните стереоселективность реакции.
Опыт 3. Окисление непредельных углеводородов раствором перманганата калия (реакция Вагнера).
В пробирку поместите 2 капли 0,1н раствора KMnO4, добавьте по каплям циклогексен до обесцвечивания раствора. Обратите внимание на возможное образование бурого осадка оксида марганца (IV). Для сравнения проведите аналогичный опыт с циклогексаном. Обесцвечивание раствора не наблюдается.
Схема реакции:
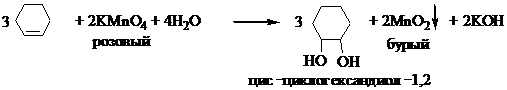
Вопросы:
1. Для каких целей используется данная реакция в качественном анализе?
2. Объясните изменение степени окисления марганца при реакции в нейтральной среде.
Опыт 4. Отношение бензола и толуола к бромной воде и окислению.
В 2 пробирки поместите по 2 капли бензола и толуола, добавьте 3 капли бромной воды. Обесцвечивание раствора не наблюдается.
В 2 пробирки поместите по 2 капли бензола и толуола, добавьте по 2 капли 0,01н (0,2%) KMnO4, энергично встряхните. Обесцвечивания раствора не наблюдается. Добавьте в обе пробирки по 1 капле 2н Н2SO4, нагрейте. Обесцвечивание наблюдается в пробирке с толуолом.
Схема реакции:
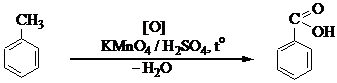
Вопросы:
1. Какие продукты образуются при окислении изопропилбензола и 1,2-диметилбензола?
2. Для каких целей используется в органической химии реакция окисления гомологов бензола?
Опыт 5. Бромирование анилина.
В пробирку поместите 1 каплю анилина и 5-6 капель воды, хорошо взболтайте и прибавьте несколько капель бромной воды до появления белого осадка 2,4,6-триброманилина.
Схема реакции:
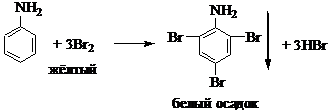
Вопросы:
1. Сравните реакционную способность бензола и анилина в реакции бромирования.
2. Объясните ориентирующее влияние аминогруппы в реакциях замещения электрофильного (SЕ).
3. Опишите механизм SЕ.
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ.
1. Покажите графически распределение электронной плотности, выделите и назовите возможные реакционные центры в каждом из следующих соединений:
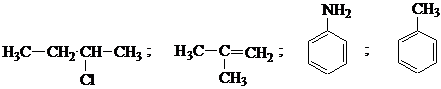
2. Укажите тип и сравните стабильность промежуточных частиц:
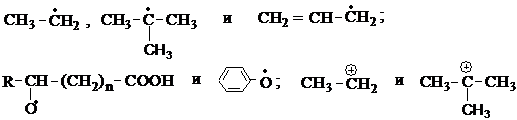
3. Напишите структурные формулы каждого из следующих соединений по их систематическому названию:
– 2-метил-4,4-диэтилгептан;
– 2-изопропил-5-метилциклогексанол;
– транс-2,2,5,5-тетраметилгексен-3;
– пентадиен-1,3;
– 2,4,6-тринитрофенол (пикриновая кислота);
– 3,4,5-тригидроксибензойная кислота (галловая кислота).
4. Назовите по заместительной номенклатуре IUРАС каждое из следующих соединений:
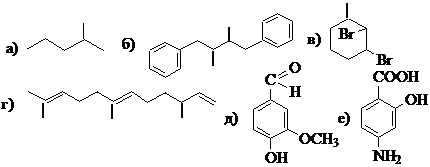
5. Напишите схему реакции бромирования 2-метилбутана при облучении УФ-светом, опишите по стадиям механизм SR. Объясните региоселективность реакции.
6. Как протекают реакции хлорирования циклопентана на свету? Напишите схему реакции монохлорирования циклопентана. Опишите механизм.
7. С помощью каких реакций можно получить бромэтан из
а) этана; б) этена.
Напишите схемы реакций, опишите их механизмы. Объясните причину различия в механизмах реакций для этана и этена.
8. Предскажите продукты каждой из приведенных ниже реакций, объясните особенности их протекания. Напишите схемы реакций, опишите механизм.
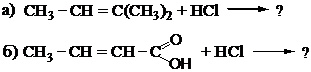
9. В цикле трикарбоновых кислот на одной из стадий фумаровая кислота (транс-бутендиовая кислота) превращается в яблочную (2-гидроксибутандиовая кислота). Предложите реагент для такого превращения. Объясните роль кислотного катализа, опишите механизм реакции.
10. Терпин – лекарственное средство, применяемое при хроническом бронхите – получают путем полной гидратации лимонена в кислой среде в соответствии с правилом Марковникова. Напишите уравнение реакции гидратации лимонена с образованием терпина.
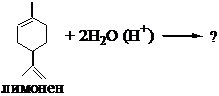
11. Гидратация цис–аконитовой кислоты (3-карбоксипентен-2-диовая кислота-1,5) может протекать как по правилу Марковникова, так и против него. Напишите схемы реакций, объясните особенности их протекания, назовите продукты по заместительной номенклатуре. Опишите механизм реакции с участием кислотного катализатора.
12. Холестерин – стероид, присутствующий практически во всех животных липидах, крови и желчи. Он является также компонентом желчных камней. Загрязненный примесями, холестерин можно выделить из желчных камней путем экстракции органическими растворителями. На одной из стадий последующей очистки холестерина проводят реакцию с Br2 в CHCl3 и кристаллизацию продукта. Напишите схему реакции и прогнозируйте ее стереоспецифичнось.
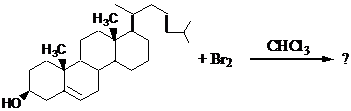
13. Напишите структуру продуктов следующих реакций:
а) бромирования пропена; б) бромирования бензола.
Объясните различия в механизмах данных реакций.
14. Промежуточным продуктом в синтезе анестезина является n-нитротолуол. Получите его по следующей схеме:
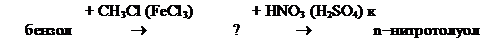
Объясните, используя правило ориентации в бензольном кольце, почему нельзя изменить последовательность этих стадий на обратную?
15. Салициловая кислота (2-гидроксибензойная кислота) является исходным продуктом для синтеза ряда лекарственных препаратов. Определите направление ориентации электрофильной частицы в реакции бромирования салициловой кислоты. Опишите механизм реакции.
16. Укажите все стадии возможных лабораторных синтезов из бензола с использованием любых реагентов:
а) м-хлорнитробензола; б) n-хлорнитробензола.
ЗАНЯТИЕ 6
