Определение поверхностного натяжения по методу отрывающейся капли
4 часа
Цель работы:
1.Освоить методику определения поверхностного натяжения.
2.Выявить зависимость поверхностной активности карбоновых кислот от строения их молекул.
План занятия
1. Сдача теоретического минимума (допуска) к лабораторной работе.
2. Ознакомление с оборудованием и методикой экспериментальной работы.
3. Определение поверхностного натяжения карбоновых кислот.
4. Составление отчета о работе.
Основная литература
1. Зимон А.Д. Физическая химия. Изд. 3-е. М.: Агар, 2006. – с. 33-45.
2. Зимон А.Д. Коллоидная химия. Изд. 5-е. М.: Агар, 2007. – с. 76-89.
Дополнительная литература
1. Болдырев А.И. Физическая и коллоидная химия, - М.: Высшая школа, 2003.
2. Чанг Р. Физическая химия с приложениями к биологическим системам. - М.: Мир, 1991.
Вопросы для самоподготовки
1.Что называется поверхностным натяжением? Как оно возникает? В каких единицах измеряется?
2. От каких факторов зависит поверхностное натяжение? Поясните действие этих факторов
3. Почему вода имеет более высокое поверхностное натяжение, чем другие жидкости?
4. Почему капли жидкости стремятся иметь форму шара?
5. Почему маленькая капля ртути круглая, а большая сплюснутая?
6. Какие вещества называются поверхностно-активными? Примеры. Каков механизм их действия?
7. Какие вещества называются поверхностно-неактивными? Примеры. Каков механизм их действия?
8. Чем объясняется вогнутость и выпуклость мениска в капиллярных трубках? Подъем жидкости в тонких капиллярах?
9. Сформулируйте правило Траубе-Дюкло. Для каких условий оно применимо?
10. Как зависит поверхностная активность веществ от длины углеводородного радикала и наличия функциональных групп?
11. Какие методы измерения поверхностного натяжения Вам известны? В чем их суть?
Краткие методические указания.
Перед выполнением практической работы необходимо детально ознакомиться с сущностью различных методов определения поверхностного натяжения. Метод отрывающейся капли позволяет заменить сталагмометр обычной аналитической бюреткой. Однако в этом случае у каждой бюретки число капель в определенном объеме(2 мл) будет своим, так как величина капли и ее вес будет зависеть от диаметра вытянутого конца бюретки. Однако общая тенденция зависимости величины поверхностного натяжения от строения молекул поверхностно-активных веществ будет одной и той же. Для получения стабильных результатов необходимо добиться медленного и плавного вытекания жидкости из бюретки. Лучше всего использовать бюретку с хорошо смазанным краном.
Принадлежности для работы
Сталагмометр (вместо сталагмометра можно использовать аналитическую бюретку с краном или стеклянном шариком). Штатив с лапкой, стеклянная воронка, четыре стакана на 100 мл, 1,0 М растворы муравьиной, уксусной, пропионовой и масляной кислот, дистиллированная вода.
Ход работы
Бюретку укрепляют вертикально в лапке штатива, 2-3 раза промывают дистиллированной водой и заполняют до верхней нулевой отметки, предварительно удалив пузырек воздуха из носика бюретки. Если бюретка с краном, то ее заполняют жидкостью выше нулевой отметки. Осторожно приоткрывают кран таким образом, чтобы жидкость вытекала медленно. В этом случае капли, отрывающиеся от конца бюретки, будут одинаковыми по объему и массе. Для получения достоверных результатов достаточно 4-5 определений числа капель в 2 мл жидкости. Частота отрыва капель должна составлять примерно 1 каплю за 2 секунды. Отсчет капель начинают в момент касания мениска нулевой отметки, а заканчивают при касании мениска отметки в 2 мл. Ток жидкости можно не останавливать и продолжать отсчет далее, начиная его сначала с отметки 2, 4, 6 и т.д. миллилитров.
Отсчет числа капель воды продолжают до тех пор, пока два последних отсчета дадут полное совпадение числа капель или их число будет отличаться не более чем на одну каплю. Полученное число капель дистиллированной воды в определенном объеме (2 мл) обозначают, как n0 и используют для подстановки в соответствующую формулу. После окончания отсчета остаток воды из бюретки полностью сливают.
Если бюретка со стеклянной бусинкой, а не с краном, то в этом случае ток жидкости вызывают, надавливая двумя пальцами на бусинку заключенную в отрезок резинового шланга укрепленного на конце бюретки. Бусинку сжимают медленно и плавно, стараясь, чтобы капли отрывались равномерно - одна капля за 2 секунды. Число отсчетов капель не менее 3-4-х, до полного совпадения числа капель.
Таким же образом определяют число капель в 2 мл выданных исследуемых 1 М растворах карбоновых кислот: муравьиной, уксусной, пропионовой, молочной и масляной. После опыта с каждым из растворов бюретку 2-3 раза промывают дистиллированной водой от остатков соответствующей кислоты.
Начинать опыты (после воды) следует с кислотой имеющей самый короткий радикал, то есть с муравьиной и далее в порядке удлинения углеводородного радикала. Поверхностное натяжение исследуемых растворов вычисляют по формуле:
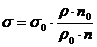
Где σ - поверхностное натяжение исследуемого раствора в Дж/м2
σ0 -поверхностное натяжение воды при температуре опыта, (берется из справочной таблицы).
ρ и ρ0 -плотность исследуемого раствора и плотность воды при температуре опыта(берется из справочной таблицы)
n0 -число капель воды в исследуемом объеме(2 мл)
n -число капель раствора в том же объеме(2 мл)
Результаты расчетов вносят в следующую таблицу.
Таблица 1.
| Карбоновая кислота | Концентрация раствора, м/литр | Поверхностное натяжение, Дж/ м2 |
| Муравьиная Уксусная Пропионовая Молочная Масляная | 1,0 1,0 1,0 1,0 1,0 |
Отчет о работе.
1. Сделать расчеты для значений поверхностного натяжения исследованных растворов.
2. Сделать вывод о влиянии длины углеводородного радикала на поверхностную активность в ряду карбоновых кислот.
3. Сделать вывод о влиянии числа функциональных групп в молекулах карбоновых кислот на их поверхностную активность.
Справочные данные:
Поверхностное натяжение воды (18°С) 0,0731 Дж/ м2
Плотность воды (18°С) 0,9991 г/мл
Плотность одномолярных растворов (18°С)
муравьиная- 0,9996 г/мл
уксусная- 0,9998 г/мл
пропионовая- 1,003 г/мл
молочная- 1,007 г/мл
масляная- 1,009 г/мл
