Получение золя гидроксида железа (iii).
КОАГУЛЯЦИЯ
Дисперсной называется двух- или многофазная, т.е. гетерогенная система, в которой, по крайней мере, одна из фаз представлена очень маленькими частицами, размеры которых тем не менее заметно превосходят молекулярные. Частицы раздробленного вещества при этом называются дисперсной фазой, а гомогенная фаза, в которой они распределены (растворитель), представляет собой дисперсионную среду. Примерами дисперсных систем могут служить дымы, туманы, взвеси различных веществ, например глины в воде и т.д.
Дисперсные системы классифицируют по агрегатному состоянию дисперсной фазы и дисперсионной среды. Системы, представляющие собой мелкие капельки жидкости в жидкой дисперсионной среде, называются эмульсиями. Примеры эмульсий молоко, латексы, различные косметические препараты и т.д. Высокодисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой называют золями при невысокой концентрации дисперсной фазы (когда частицы обособлены) и гелями, когда частицы агрегируют и образуют связно дисперсную систему. В случае грубых дисперсий твердого вещества в жидкой дисперсионной фазе различают малоконцентрированные суспензии и высококонцентрированные пасты.
Дисперсные системы различаются по величине частиц раздробленного вещества, или, как говорят, по степени дисперсности. Различают грубодисперсные и коллоидно-дисперсные системы. В суспензиях и эмульсиях радиус частиц больше 0,1 мк. Такие дисперсные системы, как, например, взвесь глины в воде, не обладают осмотическим давлением, не фильтруются через бумажные фильтры и являются неустойчивыми, т.е. не остаются долго во взвешенном состоянии в жидкой среде, а выпадают под действием силы тяжести на дно сосуда. Это кинетически неустойчивые системы. С повышением степени дисперсности, т.е. уменьшением частиц дисперсной фазы, системы приобретают новые качества. Так, дисперсные системы, состоящие из частиц с радиусом от 0,1 мк до 1 ммк, качественно отличны от суспензий. Частицы таких систем находятся в непрерывном хаотическом движении, вследствие чего обладают и осмотическим давлением, и способностью к диффузии. Благодаря непрерывному движению частиц они остаются кинетически устойчивыми. Такие системы в проходящем свете прозрачны, в то время как суспензии мутны. Подобного рода дисперсные системы часто называют коллоидными растворами. Частицы коллоидных растворов (золей) значительно больше молекул, так как они представляют собой агрегаты из достаточно большого числа молекул или атомов.
В суспензиях частицы можно наблюдать при помощи микроскопа и тем самым обнаружить поверхность раздела фаз. Коллоидные частицы из-за незначительных размеров нельзя обнаружить даже под микроскопом.
В истинных растворах размер частиц доведен до размеров молекул или ионов. В них нет поверхности раздела между составляющими компонентами, т.е. растворителем и растворенным веществом. Истинные растворы агрегативно устойчивы.
Коллоидные системы по термодинамической устойчивости делятся на лиофобные и лиофильные. Термодинамически устойчивые системы, образующиеся при самопроизвольном диспергировании одной из фаз, называются лиофильными. Самопроизвольному диспергированию способствует усиление взаимодействия дисперсной фазы с дисперсионной средой. Примерами лиофильных коллоидных систем могут служить растворы мыл и других поверхностно-активных веществ. К ним также относят растворы белков и других высокомолекулярных соединений.
Основным свойством лиофобных систем является их термодинамическая неустойчивость, связанная с большим запасом свободной поверхностной энергии на развитой межфазной поверхности раздела. Самопроизвольно из макроскопических фаз они не образуются. Получение их требует затраты внешней энергии – механической (растирание), химической (проведение химических реакций), электрической (распыление под действием электрического тока). Однако такие коллоидные системы могут быть кинетически устойчивыми, т.е. сохраняться без изменений в течение более или менее длительного времени.
Существуют две группы методов получения лиофобных коллоидных систем. Методы, основанные на раздроблении крупных частиц на более мелкие, получили название методов диспергирования. Методы, связанные с агрегацией молекул или ионов в более крупные частицы, называются конденсационными. Важное условие для получения устойчивой коллоидной системы – присутствие стабилизаторов, т.е. веществ, которые, адсорбируясь на поверхности коллоидных частиц, создавали бы достаточно интенсивное взаимодействие между поверхностью и окружающей средой (растворителем).
К методам конденсации относятся следующие способы получения коллоидных систем.
· Конденсация молекул испаряющегося вещества, соединяющихся в мелкие частицы.
· Замена растворителя, т.е. такое изменение среды, при котором вещество из растворимого становится нерастворимым.
· Химические реакции в растворе, сопровождающиеся образованием трудно растворимых веществ.
Однако во всех этих случаях коллоидные системы получаются тогда, когда растворимость дисперсной фазы ничтожна мала. При несоблюдении этого условия возможно образование молекулярных растворов. Кроме того, необходимо, чтобы между частицами и средой существовало взаимодействие, препятствующее связыванию частиц друг и другом.
Рассмотрим строение коллоидных частиц на примере золя гидроксида железа (III). Его получают реакцией гидролиза по уравнению:
FeCl3 + 3H2O ® Fe(OH)3 + 3HCl.
Поверхностные молекулы агрегата Fe(OH)3 вступают в химическое взаимодействие с HCl:
Fe(OH)3 + HCl ® FeOCl + 2H2O.
Молекулы FeOCl, подвергаясь диссоциации, образуют ионы FeO+ и Cl-. Из растворов на поверхности коллоидных частиц адсорбируются ионы близкие по своей природе к составу ядра – правило Липатова. В рассматриваемом случае это будут ионы FeO+. Строение частиц золя гидроксида железа (III) схематически можно изобразить следующим образом:
FeOCl ® FeO+ + Cl-
nFe(OH)3 + mFeO+ + mCl- ® [(Fe(OH)3)n m FeO+ (m-x)Cl-]+x xCl-
Fe(OH)3 –ядро коллоидной частицы, на его поверхности находятся адсорбированные ионы FeO+, которые придают ядру положительный заряд. Они называются потенциалобразующими. К заряженному ядру притягиваются противоионы Cl-, формируя двойной электрический слой (ДЭС). Часть противоионов Cl- находится вблизи поверхности в так называемом адсорбционном слое. Противоионы в адсорбированном слое вместе с ядром составляют гранулу. Этот слой перемещается совместно с частицей. Остальное количество противоионов Cl- находится в свободном объеме, образуя диффузный слой (см. рис. 10.1, работа 10). В целом рассматриваемая коллоидная частица (гранула) несет некоторый положительный заряд. При сближении двух таких частиц, несущих на поверхности одноименный заряд, будет происходить отталкивание, препятствующее их слипанию (электростатический барьер). Сближению коллоидных частиц препятствует также и слой молекул растворителя, в частности воды, входящих в сольватную (гидратную) оболочку ионов на поверхности частицы. Кроме того, на поверхности коллоидных частиц могут адсорбироваться молекулы специально добавляемых веществ-стабилизаторов (адсорбционно-сольватный барьер).
Наличие электростатического и адсорбционно-сольватного барьера, препятствующих агрегации (соединению) частиц, обеспечивают агрегативную устойчивость лиофобным коллоидным системам, т.е. такие системы не изменяются заметно в течение длительного времени (иногда десятилетиями), несмотря на термодинамическую неустойчивость.
Так как лиофобные дисперсные системы являются термодинамически неравновесными, в них могут идти процессы укрупнения частиц и соответственно уменьшения межфазной поверхности. Наиболее характерный и общий для дисперсных систем путь перехода к равновесному состоянию – коагуляция, т.е. слипание частиц дисперсной фазы. Часто коагуляция сопровождается появлением мути, изменением окраски коллоидных растворов, образованием осадка (явная коагуляция). Когда происходит укрупнение частиц без видимых внешних изменений, говорят о скрытой коагуляции.
Коагуляция может происходить при действии на систему различных факторов: механическое воздействие (перемешивание или встряхивание), резкое охлаждение или нагревание, пропускание электрического тока. Иногда коагуляция может произойти в результате «старения» или химических изменений, происходящих в золе.
Добавление растворов электролитов также вызывает коагуляцию лиофобных золей. При этом коагулирующее действие оказывает один из ионов электролита: либо катион, либо анион.
Порогом коагуляции называется минимальная концентрация электролита, вызывающая коагуляцию.
Коагулирующий ион несет заряд, противоположный заряду коллоидной частицы, при этом порог коагуляции тем меньше, чем больше заряд (валентность) коагулирующего иона – правило Шульце-Гарди.
При добавлении раствора электролита к золю противоионы нейтрализуют заряд на поверхности коллоидной частицы (происходит сжатие ДЭС), что позволяет частицам золя легче приближаться друг к другу, и это воздействие тем сильнее, чем больший заряд несет противоион.
При добавлении некоторых веществ нередко наблюдается повышение устойчивости лиофобных золей к коагулирующему действию электролитов. Такое стабилизирующее действие на дисперсные системы называется коллоидной защитой. Защитными свойствами обладают белковые вещества (желатин, альбумины, казеин), полисахариды (крахмал, декстрин), некоторые поверхностно-активные вещества. Если, например, к золю гидроксида железа (III) добавить некоторое количество желатина, то для коагуляции такого золя требуется значительно больше электролита, чем для коагуляции незащищенного золя. Коллоидную защиту объясняют адсорбцией стабилизаторов на поверхности частиц дисперсной фазы и образованием слоя.
Коллоидная защита широко используется при получении устойчивых лиофобных золей, применяемых в качестве лекарственных препаратов. Например, колларгол и протаргол содержат 8 и 70% высокодисперсного металлического серебра, стабилизированного гидролизатами белков.
Коллоидная защита играет существенную роль в физиологических процессах. Содержание карбоната и фосфата кальция в крови значительно превышает их растворимость в воде. Отложению этих солей препятствуют защитные вещества крови, которые не позволяют коллоидным частицам нерастворимых солей объединяться в крупные агрегаты и осаждаться. Образование желчных и мочевых камней в организме связано с уменьшением при патологических состояниях защитного действия определенных веществ по отношению к билирубину, холестерину и уратам.
Цель работы.
1. Получить золь гидроксида железа
2. Ознакомиться с коагуляцией гидрофобного золя электролитами. Определить порог коагуляции золя электролитами.
Реактивы.
· Хлорид железа FeCl3, раствор 2%-ный.
· Растворы электролитов: KCl – 1 н, K2SO4 – 0,01 н, K3[Fe(CN)6] – 0,001 н.
· Вода дистиллированная.
Оборудование и посуда.
· Термостойкий стакан на 250 мл.
· Штатив с 12-ю пробирками.
· Пипетки на 5 и 10 мл.
· Электроплитка.
Выполнение работы.
Опыт №1. Получение золя гидроксида железа (III).
100–150 мл дистиллированной воды нагревают в стакане до кипения. Затем в кипящую воду постепенно при нагревании добавляют 5-10 мл 2%-ного раствора FeCl3, доводят до кипения. Полученный коллоидный раствор гидроксида железа (III) желто-коричневого цвета осторожно охлаждают до комнатной температуры. Приготовленный золь используют для определения порога коагуляции электролитов и для наблюдения электрофореза (работа 10).
Опыт №2. Определение порога коагуляции золя электролитами.
1. В двенадцать чистых пробирок наливают пипетками объемы дистиллированной воды и растворов электролитов, указанные в таблице 9.1.
2. Во все пробирки пипеткой добавляют по 5 мл охлажденного до комнатной температуры золя. Содержимое пробирок хорошо перемешивают.
3. Через 1 час отмечают, в каких пробирках наблюдается явная коагуляция (помутнение) и седиментация. Результаты наблюдений заносят в таблицу 9.2: в строке напротив соответствующего электролита записывают «+», если коагуляция наблюдается, «–», если коллоидный раствор в пробирке прозрачен.
Таблица 9.1
| № пробирки | |||||||
| Золь гидроксида железа (III), мл | |||||||
| Дистиллированная вода, мл | 4,5 | ||||||
| Раствор электролита, мл | 0,5 | ||||||
| Результат наблюдения через 1 час («+» – если есть помутнение и осадок «–» –если коагуляция не наблюдается) | |||||||
| KCl | |||||||
| K2SO4 | |||||||
| K3[Fe(CN)6] | |||||||
Для каждого электролита отмечают наименьший объем, при добавлении которого наблюдалась коагуляция золя.
Обработка результатов.
1. Порог коагуляции выражается в миллимолях электролита на литр коллоидного раствора (ммоль/л). Порог коагуляции вычисляют по формуле:
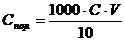 ,
,
где С – концентрация раствора добавленного электролита, моль/л, V – наименьшее число миллилитров раствора электролита, достаточное для коагуляции золя, мл (см. таблицу 9.1), 10 – суммарный объем золя после добавления электролита, мл.
2. Вычисляют порог коагуляции для каждого электролита и результаты записывают в таблицу 9.2.
Таблица 9. 2
| Электролит | Коагулирующий ион | Порог коагуляции |
| KCl | ||
| K2SO4 | ||
| K3[Fe(CN)6] |
Контрольные вопросы.
1. Какие существуют методы получения дисперсных систем?
2. Чем отличается коллоидно-дисперсные системы от истинных растворов и грубодисперсных систем?
3. Приведите строение мицелл золя гидроксида железа (III), иодида серебра, полученного при избытке иодида калия и при избытке нитрата серебра.
4. В чем заключается явление коагуляции?
5. Что такое порог коагуляции и как его можно определить экспериментально?
6. В чем заключается правило Шульце-Гарди?
7. Что такое коллоидная защита?
РАБОТА 10
