Алгоритм ответа по химии элементов
1. Электронная формула (семейство и тип элемента).
2. Графическое изображение валентных электронов в нормальном и возбужденном состояниях.
3. Окислительно – восстановительные свойства атомов.
4. Возможные устойчивые степени окисления.
5. Примеры соединений (оксиды, гидроксиды, соли, водородные соединения неметаллических элементов.)
6. Характер соединений и их свойства.
7. Является макро или микроэлементом.
8. Биологическая роль ионов и соединений.
9. Токсичность.
10. Использование простых веществ и соединений в ветеринарной медицине.
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1. Глинка, Н. Л. Задачи и упражнения по общей химии : учеб. пособие / Н. Л. Глинка. - Изд. стер. - М. : КноРус, 2012. - 240 с.
2. Глинка, Н. Л. Общая химия : [учеб. пособие] / Н. Л. Глинка. - М. : КноРус, 2011. - 746 с.
3. Егоров, В. В. Неорганическая и аналитическая химия. Аналитическая химия : учебник / В. В. Егоров, Н. И. Воробьева, И. Г. Сильвестрова. - Санкт-Петербург ; Москва ; Краснодар : Лань, 2014. - 139 с.
4. Задачи и упражнения по общей химии : учеб. пособие для вузов / [Адамсон Б. И. и др.] ; под ред. Н. В. Коровина. - Изд. 2-е, испр. - М. : Высш. шк., 2004. - 255 с.
5. Князев, Д. А. Неорганическая химия : учеб. для вузов / Д. А. Князев, С. Н. Смарыгин. - 3-е изд., испр. - М. : Дрофа, 2005. - 587 с.
6. Коровин, Н. В. Общая химия : учебник / Н. В. Коровин. - Изд. 10-е, доп. - М. : Высш. шк., 2008. - 557 с.
7. Неорганическая химия : Биогенные и абиогенные элементы : учеб. пособие / [В. В. Егоров и др.] ; под ред. В. В. Егорова. - СПб. ; М. ; Краснодар : Лань, 2009. - 307 с.
8. Попков, В. А. Общая химия. Биофизическая химия. Химия биогенных элементов : учебник для вузов / В. А. Попков, Ю. А. Ершов, А. С. Берлянд ; под ред. Ю. А. Ершова. - 9-е изд. - Москва : Юрайт, 2012. - 556 с.
9. Саргаев, П. М. Неорганическая химия / П. М. Саргаев. - М. : КолосС, 2004. - 267 с.
10. Хомченко, Г. П. Неорганическая химия : учебник / Г. П. Хомченко, И. К. Цитович. - Изд. 2-е, перераб. и доп., репр. - СПб. : Квадро, 2009. - 460 с.
11. Цитович, И. К. Курс аналитической химии : учебник / И. К. Цитович. - Изд. 9-е, стер. - СПб. ; М. ; Краснодар : Лань, 2007. - 485 с.
| ПРИЛОЖЕНИЕ А Таблица А.1- Растворимость солей в воде | Катион | Pb2+ | М | М | Н | Р | Р | Н | Н | Р | Н | Н | Н | Н | Н | (Р – растворимое вещество, М – малорастворимое, Н- труднорастворимое; черта означает, что вещество не существует или разлагается водой |
| Sn2+ | Р | Р | Р | - | - | Н | - | Р | - | - | - | Н | Н | |||
| AI3+ | Р | Р | Р | Р | Р | - | - | Р | - | Н | - | Н | Н | |||
| Hg2+ | Р | М | Н | Р | Р | Н | Н | - | - | - | Н | Н | - | |||
| Zn2+ | Р | Р | Р | Р | Р | Н | М | Р | Н | Н | Н | Н | Н | |||
| Ba2+ | Р | Р | Р | Р | Р | Р | Н | Н | Н | Н | Н | Н | Р | |||
| Sr2+ | Р | Р | Р | Р | Р | Р | Р | Н | Н | Н | М | Н | М | |||
| Ca2+ | Р | Р | Р | Р | Р | Р | Н | М | Н | Н | М | Н | М | |||
| Mg2+ | Р | Р | Р | Р | Р | - | Н | Р | Н | Н | Р | Н | Н | |||
| Ag+ | Н | Н | Н | Р | Р | Н | Н | М | Н | - | Н | Н | - | |||
| Cu2+ | Р | Р | - | Р | Р | Н | Н | Р | - | - | Н | Н | Н | |||
| NH4+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | Р | |||
| K+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | |||
| Na+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | |||
| Li+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | |||
| Анион | CI− | Br− | J− | NO3− | CH3COO− | S2− | SO32 | SO42- | CO32- | SiO32- | Cr042- | PO43- | OH− |
ПРИЛОЖЕНИЕ Б
Сильные и слабые электролиты
Сильные электролиты(α > 30%): все соли; HCI, HBr, HI, HCIO4, H2SO4, НMnО4, HClО3,HNO3; гидроксиды щелочных и щелочноземельных металлов, (Li, Na, K, Rb, Cs, Fr, Ca, Ba, Sr); гидроанионы сильных кислот, например, HSO4−; гидроксокатионы сильных оснований, например, CaOH+.
Слабые электролиты(α < 30%): H2O, NH3∙H2O2, HF, HCIO, HClO2, H2S, H2SO3, H2CO3, H2SiO3, H3PO4, H3BO3, CH3COOH, HNO2 и др.; гидроксокатионы труднорастворимых оснований, например, AIOH2+, AI(OH)2+ и др.; органические кислоты; гидраанионы слабых кислот, например, HCO3−, H2PO4−, HPO42−, HSO3− и др.; комплексные ионы, например, [Fe(CN)6]3−, [AI(OH)6]3- и др.
ПРИЛОЖЕНИЕ В
Ряд стандартных электродных потенциалов в водных растворах при 25 0С
 Окисленная УСИЛИНИЕ ОКИСЛИТЕЛЬНЫХ СВОЙСТВ
Окисленная УСИЛИНИЕ ОКИСЛИТЕЛЬНЫХ СВОЙСТВ
форма Li+ K+ Ca2+ Na2+ Mg2+ AI3+ Mn2+
Восстанов-
 ленная Li K Ca Na Mg AI Mn
ленная Li K Ca Na Mg AI Mn
форма УСИЛЕНИЕ ВОССТАНОВИТЕЛЬНЫХ СВОЙСТВ
Е0, В -3,0 -2,9 -2,8 -2.7 -2,3 -1,66 -1,18
 Окисленная
Окисленная
форма Zn2+ Cr3+ Fe2+ Sn2+ 2H+ Cu2+ Ag+ Au3+
Восстановленная
 форма Zn Cr Fe Sn H2 Cu Ag Au
форма Zn Cr Fe Sn H2 Cu Ag Au
Е0, В -0,76 -0,74 -0,44 -0,25 -0,14 0,0 +0,34 +0,80
ПРИЛОЖЕНИЕ Г
Ряд активности кислот
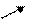
 HCl, HBr, HJ HF, H2S, H2SO3, H2CO3,
HCl, HBr, HJ HF, H2S, H2SO3, H2CO3,

 H2SO4
H2SO4
HNO3, HClO4 H3PO3, H3PO4 и другие слабые кислоты
 |
Реакции в водных растворах между растворами солей и кислот протекают в этом направлении, например:
H2SO4 + NaCl(к) 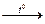 HCl↑ + NaHSO4,
HCl↑ + NaHSO4,

 Na2SO4 + 2HCl реакция не протекает.
Na2SO4 + 2HCl реакция не протекает.
Исключением являются реакции образования труднорастворимых солей с малыми значениями произведений растворимости в разбавленных растворах сильных кислот, например:
ZnCl2 + H2S → ZnS↓ + HCl,
ПP(ZnS) = 3,6 x 10-24.
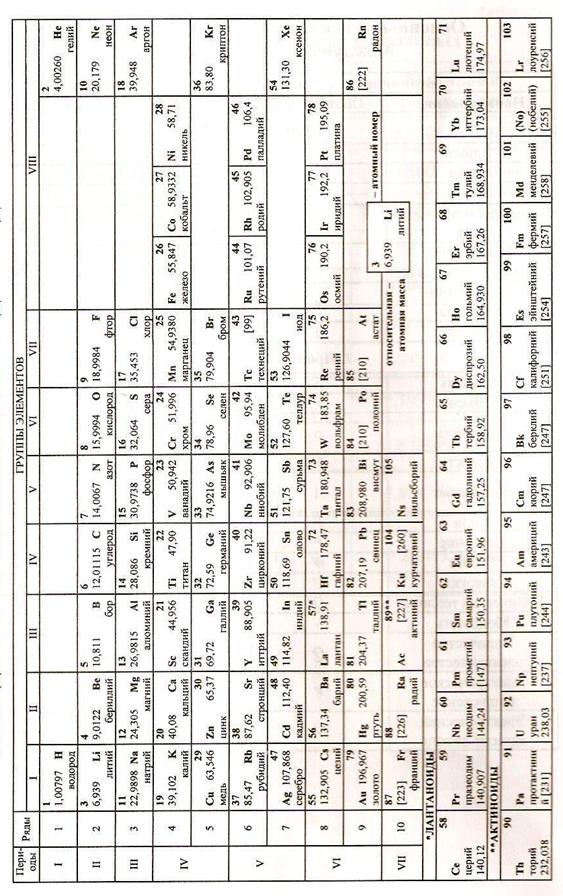
| Таблица Д.1 – Периодическая система элементов Д.И. Менделеева ПРИЛОЖЕНИЕ Д |
| ПРИЛОЖЕНИЕ Е Таблица Е.1 - Взаимодействие металлов с концентрированными серной и азотной кислотами, с разбавленной азотной кислотой | Продукты реакции | Соль металла +SO2 + H2O | Кроме соли металла и воды возможно образование следующих продуктов: SO2, S, H2S | Соль металла + вода + H2S | Соль металла + вода + NO2, | Соль металла + вода + NO | Пассивируются HNO3 | Не взаимодействуют с HNO3 | Соль металла + вода + NO | Соль металла + вода + NH3 (или NH4NO3 при избытке кислоты) или N2. |
| Тип кислоты | Концентрированная H2SO4 | Концентрированная HNO3 | Разбавленная HNO3 | |||||||
| Тип металла | Малоактивные металлы и Pb, Sn, Mo, Ni, Cd. | Металлы, стоящие в середине ряда напряжений металлов | Активные металлы, стоящие в начале ряда напряжений (по Al) | Малоактивные металлы, кроме Au и платиновых металлов | Активные металлы, кроме Al, Cr, Fe | Al, Cr, Fe | Au и платиновые металлы | Малоактивные металлы, кроме Au и платиновых металлов | Активные металлы |
ПРИЛОЖЕНИЕ Ж
Таблица Ж.1 – Термодинамические константы некоторых веществ
| Вещество | ∆ 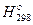 , кДж/моль , кДж/моль | ∆ 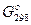 , кДж/моль , кДж/моль | 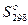 , Дж/(моль · К) , Дж/(моль · К) | |||
| Ag (к) | 42,69 | |||||
| AgBr (к) | − 99,16 | − 95,94 | 107,1 | |||
| AgCl (к) | − 126,8 | − 109,7 | 109,7 | |||
| AgI (к) | − 64,2 | − 66,3 | 114,2 | |||
| AgF (к) | − 202,9 | − 184,9 | 83,7 | |||
| AgNO3 (к) | − 120,7 | − 32,2 | 140,9 | |||
| Ag2O (к) | − 30,56 | − 10,82 | 121,7 | |||
| Ag2CO3 | − 506,1 | − 437,1 | 167,4 | |||
| Al (к) | 28,31 | |||||
| Al2O3 (к) | − 1675,0 | − 1676,4 | 50,94 | |||
| Al(OH)3 (к) | − 1275,7 | − 1139,72 | 71,1 | |||
| AlCl3 (к) | − 697,4 | − 636,8 | 167,0 | |||
| Al2(SO4)3 (к) | − 3434,0 | − 3091,9 | 239,2 | |||
| As (к) | 35,1 | |||||
| As2O3 (к) | − 656,8 | − 575,0 | 107,1 | |||
| As2O5 (к) | − 918,0 | − 772,4 | 105,4 | |||
| Au (к) | 47,65 | |||||
| AuF (к) | − 74,3 | − 58,6 | 96,4 | |||
| AuF3 (к) | − 348,53 | − 297,48 | 114,2 | |||
| Au(OH)3 (к) | − 418,4 | − 289,95 | 121,3 | |||
| AuCl3 (к) | − 118,4 | − 48,53 | 146,4 | |||
| B (к) | 5,87 | |||||
| B2O3 (к) | − 1264,0 | − 1184,0 | 53,85 | |||
| B2H6 (г) | 31,4 | 82,8 | 232,9 | |||
| Ba (к) | 64,9 | |||||
| BaO (к) | − 556,6 | − 528,4 | 70,3 | |||
| BaCO3 (к) | − 1202,0 | − 1138,8 | 112,1 | |||
| Be (к) | 9,54 | |||||
| BeO (к) | − 598,7 | − 581,6 | 14,10 | |||
| BeCO3 (к) | − 981,57 | − 944,75 | 199,4 | |||
| Bi (к) | 56,9 | |||||
| BiCl3 (г) | − 270,7 | − 260,2 | 356,9 | |||
| BiCl3 (к) | − 379,1 | − 318,9 | 189,5 | |||
| Br2 (г) | 30,92 | 3,14 | 245,35 | |||
| HBr (г) | − 36,23 | − 53,22 | 198,48 | |||
| C (алмаз) | 1,897 | 2,866 | 2,38 | |||
| C (графит) | 5,74 | |||||
| CO (г) | − 110,5 | − 137,27 | 197,4 | |||
| Продолжение таблицы Ж.1 | ||||||
| Вещество | ∆ 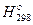 , кДж/моль , кДж/моль | ∆ 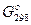 , кДж/моль , кДж/моль | 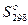 , Дж/(моль · К) , Дж/(моль · К) | |||
| CO2 (г) | − 393,51 | − 394,38 | 213,6 | |||
| COCl2 (г) | − 223,0 | − 210,5 | 289,2 | |||
| CS2 (г) | 115,3 | 65,1 | 237,8 | |||
| CS2 (ж) | 87,8 | 63,6 | 151,0 | |||
| C2H2 (г) | 226,75 | 209,2 | 200,8 | |||
| C2H4 (г) | 52,28 | 68,12 | 219,4 | |||
| CH4 (г) | − 74,85 | − 50,79 | 186,19 | |||
| C2H6 (г) | − 84,67 | − 32,89 | 229,5 | |||
| C6H6 (ж) | 49,04 | 124,50 | 173,2 | |||
| CH3OH (ж) | − 238,7 | − 166,31 | 126,7 | |||
| C2H5OH (ж) | − 227,6 | − 174,77 | 160,7 | |||
| CH3COOH (ж) | − 484,9 | − 392,46 | 159,8 | |||
| Ca (к) | 41,62 | |||||
| CaO (к) | − 635,1 | − 604,2 | 39,7 | |||
| CaF2 (к) | − 1214,0 | − 1161,0 | 68,87 | |||
| CaCl2 (к) | − 785,8 | − 750,2 | 113,8 | |||
| CaC2 | − 62,7 | − 67,8 | 70,3 | |||
| Ca3N2 (к) | − 431,8 | − 368,6 | 104,6 | |||
| Ca(OH)2 (к) | − 986,2 | − 896,76 | 83,4 | |||
| CaSO4 (к) | − 1424,0 | − 1320,3 | 106,7 | |||
| CaSiO3 (к) | − 1579,0 | − 1495,4 | 87,45 | |||
| Ca3(PO4)2 (к) | − 4125,0 | − 3899,5 | 240,9 | |||
| CaCO3 (к) | − 1206,0 | − 1128,8 | 92,9 | |||
| Cl2 (г) | 223,0 | |||||
| HCl (г) | − 92,30 | − 95,27 | 186,7 | |||
| HCl (ж) | − 167,5 | − 131,2 | 55,2 | |||
| HClO (ж) | − 116,4 | 80,0 | 129,7 | |||
| Cr (к) | 23,76 | |||||
| Cr2O3 (к) | − 1141,0 | − 1046,84 | 81,1 | |||
| Cr(CO)6 (к) | − 1075,62 | − 982,0 | 359,4 | |||
| Cs (к) | 84,35 | |||||
| Cs2O (к) | − 317,6 | − 274,5 | 123,8 | |||
| CsOH (к) | − 406,5 | − 355,2 | 77,8 | |||
| Cu (к) | 33,3 | |||||
| Cu2O (к) | − 167,34 | − 146,36 | 93,93 | |||
| CuO (к) | − 165,3 | − 127,19 | 42,64 | |||
| Cu(OH)2 (к) | − 443,9 | − 356,90 | 79,50 | |||
| CuF2 (к) | − 530,9 | − 485,3 | 84,5 | |||
| CuCl2 (к) | − 205,9 | − 156,1 | 113,0 | |||
| CuBr2 (к) | − 141,42 | − 126,78 | 142,34 | |||
| Продолжение таблицы Ж.1 | ||||||
| Вещество | ∆ 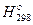 , кДж/моль , кДж/моль | ∆ 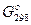 , кДж/моль , кДж/моль | 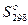 , Дж/(моль · К) , Дж/(моль · К) | |||
| CuI2 (к) | − 21,34 | − 23,85 | 159,0 | |||
| Cu2S (к) | − 82,01 | − 86,19 | 119,24 | |||
| CuS (к) | − 48,5 | − 48,95 | 66,5 | |||
| CuSO4 (к) | − 771,1 | − 661,91 | 113,3 | |||
| CuCO3 (к) | − 594,96 | − 517,98 | 87,9 | |||
| Cu(NO3)2 (к) | − 307,11 | − 114,22 | 193,3 | |||
| Fe (к) | 27,15 | |||||
| FeO (к) | − 263,68 | − 244,35 | 58,79 | |||
| FeCl2 (к) | − 341,0 | − 302,08 | 119,66 | |||
| Fe2O3 (к) | − 821,32 | − 740,99 | 89,96 | |||
| Fe(OH)3 (к) | − 824,25 | − 694,54 | 96,23 | |||
| FeCl3 (к) | − 405,0 | − 336,39 | 130,1 | |||
| FeSO4 (к) | − 992,57 | − 829,69 | 107,51 | |||
| FeCO3 (к) | − 744,75 | − 637,88 | 92,9 | |||
| GeO (к) | − 305,4 | − 276,1 | 50,2 | |||
| GeO2 (к) | − 539,74 | − 531,4 | 52,30 | |||
| H2 (г) | 130,6 | |||||
| H2O (г) | − 241,84 | − 228,8 | 188,74 | |||
| H2O (ж) | − 285,84 | − 237,5 | 69,96 | |||
| H2O2 (ж) | − 187,36 | − 117,57 | 105,86 | |||
| Hg (к) | 76,1 | |||||
| HgCl2 (к) | − 230,12 | − 185,77 | 144,35 | |||
| Hg2Cl2 (к) | − 264,85 | − 210,66 | 195,81 | |||
| I2 (к) | 116,73 | |||||
| I2 (г) | 62,24 | 19,4 | 260,58 | |||
| HI (г) | 25,94 | 1,30 | 206,33 | |||
| HIO (ж) | − 158,9 | − 98,7 | 24,32 | |||
| K (к) | 64,35 | |||||
| K2O (к) | − 361,5 | − 193,3 | 87,0 | |||
| KOH (к) | − 425,93 | − 374,47 | 59,41 | |||
| KNO3 (к) | − 492,71 | − 393,13 | 132,93 | |||
| KNO2 (к) | − 370,28 | − 281,58 | 117,15 | |||
| K2SO4 (к) | − 1433,44 | − 1316,37 | 175,73 | |||
| KHSO4 (к) | − 1158,1 | − 1043,49 | 187,89 | |||
| KH (к) | − 56,9 | − 38,49 | 67,95 | |||
| Li (к) | 28,03 | |||||
| Li2O (к) | − 595,8 | − 560,2 | 37,9 | |||
| LiOH (к) | − 487,8 | − 443,1 | 42,81 | |||
| Mg (к) | 32,55 | |||||
| MgO (к) | − 601,24 | − 569,6 | 26,94 | |||
| Продолжение таблицы Ж.1 | ||||||
| Вещество | ∆ 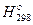 , Дж/моль , Дж/моль | ∆ 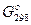 , кДж/моль , кДж/моль | 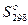 , Дж/(моль · К) , Дж/(моль · К) | |||
| Mg(OH)2 (к) | − 924,66 | − 833,7 | 63,14 | |||
| MgCO3 | − 1096,21 | − 1029,3 | 65,69 | |||
| MnSO4 | − 1063,74 | − 955,96 | 112,13 | |||
| N2 (г) | 191,5 | |||||
| N2O (г) | 81,55 | 103,6 | 220,0 | |||
| NO (г) | 90,37 | 86,69 | 210,62 | |||
| NO2 (г) | 33,89 | 51,84 | 240,45 | |||
| N2O4 (г) | 9,37 | 98,29 | 304,3 | |||
| NH3 (г) | − 46,19 | − 16,64 | 192,5 | |||
| HNO3 (ж) | − 173,0 | − 79,91 | 156,16 | |||
| NH4Cl (к) | − 315,39 | − 343,64 | 94,56 | |||
| NH4OH (ж) | − 366,69 | − 263,8 | 179,9 | |||
| Na (к) | 51,42 | |||||
| Na2O (к) | − 430,6 | − 376,6 | 71,1 | |||
| NaOH (к) | − 426,6 | − 377,0 | 64,18 | |||
| NaCl (к) | − 410,9 | − 384,0 | 72,36 | |||
| Na2CO3 (к) | − 1129,0 | − 1047,7 | 136,0 | |||
| Na2SO4 (к) | − 1384,0 | − 1266,8 | 149,4 | |||
| Na2SiO3 (к) | − 1518,0 | − 1426,7 | 113,8 | |||
| O2 (г) | 205,03 | |||||
| P (красный) | − 18,41 | − 13,81 | 22,8 | |||
| PCl3 (г) | − 277,0 | − 286,27 | 311,7 | |||
| PCl5 (г) | − 369,45 | − 324,55 | 362,9 | |||
| HPO3 (ж) | − 982,4 | − 902,91 | 150,6 | |||
| H3PO4 (ж) | − 1271,94 | − 1147,25 | 200,83 | |||
| Pb (к) | 64,9 | |||||
| PbO (к) | − 217,86 | − 188,49 | 67,4 | |||
| PbO2 (к) | − 276,6 | − 218,99 | 76,44 | |||
| PbCl (к) | − 359,2 | − 313,97 | 136,4 | |||
| PbSO4 (к) | − 918,1 | − 811,24 | 147,28 | |||
| PbS (к) | − 94,28 | − 92,68 | 91,20 | |||
| Rb (к) | 76,2 | |||||
| Rb2O (к) | − 330,12 | − 290,79 | 109,6 | |||
| RbOH (к) | − 413,80 | − 364,43 | 70,7 | |||
| S (ромб) | 31,88 | |||||
| SO2 (г) | − 296,9 | − 300,37 | 248,1 | |||
| SO3 (г) | − 395,2 | − 370,37 | 256,23 | |||
| H2S (г) | − 20,15 | − 33,02 | 205,64 | |||
| H2S (ж) | − 39,33 | − 27,36 | 122,2 | |||
| Продолжение таблицы Ж.1 | ||||||
| Вещество | ∆ 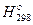 , Дж/моль , Дж/моль | ∆ 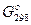 , кДж/моль , кДж/моль | 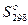 , Дж/(моль · К) , Дж/(моль · К) | |||
| H2SO4 (ж) | − 811,3 | − 742,0 | 156,9 | |||
| H2Se (г) | 85,77 | 71,13 | 221,3 | |||
| SiO2 (к) | − 859,3 | − 803,75 | 42,09 | |||
| SnO (к) | − 286,0 | − 257,32 | 56,74 | |||
| SnO2 (к) | − 580,8 | − 519,65 | 52,34 | |||
| SrO (к) | − 590,4 | − 559,8 | 54,4 | |||
| SrCO3 (к) | − 1221,3 | − 1137,6 | 97,1 | |||
| H2Te (г) | 154,39 | 138,48 | 234,3 | |||
| Zn (к) | 41,59 | |||||
| ZnO (к) | − 349,0 | − 318,19 | 43,5 | |||
| ZnS (к) | − 201,0 | − 198,32 | 57,7 | |||
| ZnSO4 (к) | − 978,2 | − 871,57 | 124,6 | |||
Условные обозначения: к –кристаллический;г– газообразный;
ж– жидкий;ромб– ромбический
ПРИЛОЖЕНИЕ З
Таблица З. 1 -Стандартные теплоты (энтальпии) образования ∆Н°298 некоторых веществ
| Вещество | Состояние | ∆Н°298, кДж/моль | Вещество | Состояние | ∆Н°298, кДж/моль |
| С2H2 | г | +226,75 | СO | г | -110,52 |
| CS2 | г | +115,28 | CH3OH | г | -201,17 |
| NO | г | +90,37 | C2H5OH | г | -235,31 |
| C6H6 | г | +82,93 | H2O | г | -241,83 |
| C2H4 | г | +52,28 | H2O | ж | -285,84 |
| H2S | г | -20,15 | NH4Cl | к | -315,39 |
| NH3 | г | -46,19 | CO2 | г | -393,51 |
| CH4 | г | -74,85 | Fe2O3 | к | -882,10 |
| C2H6 | г | -84,67 | Ca(OH)2 | к | -986,50 |
| HCl | г | -92,31 | Al2O3 | к | -1669,80 |
Таблица З. 2 -Стандартная энергия Гиббса образования ∆G°298 некоторых веществ
| Вещество | Состояние | ∆G°298, кДж/моль | Вещество | Состояние | ∆G°298, кДж/моль |
| BaCO3 | к | -1138,8 | FeO | к | -244,3 |
| CaCO3 | к | -1128,75 | H2O | ж | -237,19 |
| Fe3O4 | к | -1014,2 | H2O | г | -228,59 |
| BeCO3 | к | -944,75 | PbO2 | к | -219,0 |
| CaO | к | -604,2 | CO | г | -137,27 |
| BeO | к | -581,61 | CH4 | г | -50,79 |
| BaO | к | -528.4 | NO2 | г | +51,84 |
| CO2 | г | -394,38 | NO | г | -86,69 |
| NaCl | к | -384,03 | C2H2 | г | +209,20 |
| ZnO | к | -318,2 |
Таблица З. 3 -Стандартные абсолютные энтропии S°298 некоторых веществ
| Вещество | Состояние | ∆S°298, Дж/К · моль | Вещество | Состояние | ∆S°298, Дж/К · моль |
| C | Алмаз | 2,44 | H2O | г | 188,72 |
| C | Графит | 5,69 | N2 | г | 191,49 |
| Fe | к | 27,2 | NH3 | г | 192,50 |
| Ti | к | 30,7 | CO | г | 197,91 |
| S | Ромб | 31,9 | C2H2 | г | 200,82 |
| TiO2 | к | 50,3 | O2 | г | 205,03 |
| FeO | к | 54,0 | H2S | г | 205,64 |
| H2O | ж | 69,94 | NO | г | 210,20 |
| Fe2O3 | к | 89,96 | CO2 | г | 213,65 |
| NH4Cl | к | 94,5 | C2H4 | г | 219,45 |
| CH3OH | ж | 126,8 | Cl2 | г | 222,95 |
| H2 | г | 130,59 | NO2 | г | 240,46 |
| Fe3O4 | к | 146,4 | PCl3 | г | 311,66 |
| CH4 | г | 186,19 | PCl5 | г | 352,71 |
| HCl | г | 186,68 |
Таблица З. 4 -Стандартные электродные потенциалы (Е°) некоторых металлов (ряд напряжений металлов)
| Электрод | Е°, В | Электрод | Е°, В |
| Li+/Li | -3,045 | Cd2+/Cd | -0,403 |
| Rb+/Rb | -2,925 | Co2+/Co | -0,277 |
| K+/K | -2,924 | Ni2+/Ni | -0,25 |
| Cs+/Cs | -2,923 | Sn2+/Sn | -0,136 |
| Ba2+/Ba | -2,90 | Pb2+/Pb | -0,127 |
| Ca2+/Ca | - 2,87 | Fe3+/Fe | -0,037 |
| Na+/Na | -2,714 | 2H+/H2 | 0,000 |
| Mg2+/Mg | -2,37 | Sb3+/Sb | +0,20 |
| Al3+/Al | -1,70 | Bi3+/Bi | +0,215 |
| Ti2+/Ti | -1,603 | Cu2+/Cu | +0,34 |
| Zr4+/Zr | -1,58 | Cu+/Cu | +0,52 |
| Mn2+/Mn | -1,18 | Hg22/2Hg | +0,79 |
| V2+/V | -1,18 | Ag+/Ag | +0,80 |
| Cr2+/Cr | -0,913 | Hg2+/Hg | +0,85 |
| Zn2+/Zn | -0,763 | Pt2+/Pt | +1,19 |
| Cr3+/Cr | -0,74 | Au3+/Au | +1,50 |
| Fe2+/Fe | -0,44 | Au+/Au | +1,70 |
Учебное издание
