Тема 11. комплексные соединения
Комплексные соединения КС (высшего порядка) – такие комплексные соединения, в состав которых входят комплексные ионы, способные существовать как в кристаллическим состоянии, так и в растворе.
Строение комплексных соединений объясняет координационная теория Вернера.
Молекулы комплексных соединений состоят из:
I. Внутренней сферы – часть молекулы в квадратной скобке, в ее состав входят:
1. Ион-комплексообразователь (Ц.А.), координирующий (удерживающий вокруг себя лиганды.
2. Лиганды («ligo» –лат. –связываю) - частицы, расположенные вокруг (Ц.А.)
Число σ-связей между Ц.А. и лигандами называется координационным числом (К.Ч.) (Ц.А.)
II. Внешней сферы – остальные частицы, более удаленные от (Ц.А.)
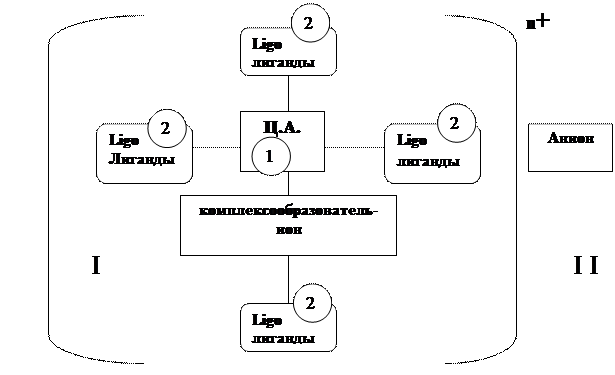
|
Рисунок 1 - Схема строения КС:
I - Внутренняя сфера, II - Внешняя сфера
Например [NH4]Cl
I Внутренняя сфера - [NH4]+
1) Ц.А. - (N-3)
2) Лиганды – (4Н+)
К.Ч.(N-3)=4
II Внешняя сфера – (Cl-)
Хлорид аммония образуется при взаимодействии:
NH3 (г) + HCl (г) → [NH4]Cl (к)
аммиак хлороводород
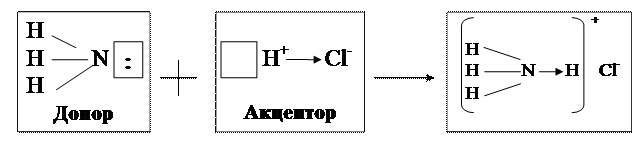
Ц.А.(N-3) играет роль донора, а протон (Н+) – акцептора, но в большинстве случаев комплексообразователь- акцептор, а лиганды- донорные частицы.
В комплексных соединениях между комплексообразователем и лигандами есть хотя бы одна ковалентная σ-связь, образованная по донорно-акцепторному механизму.
Между ионами внутренней и внешней сферы связь ионная, поэтому ионные (К.С.)-сильные электролиты, диссоциирующие на ионы внутренней и внешней сферы.
[NH4]Cl→[NH4]++Cl-
В зависимости от заряда внутренней сферы комплексные соединения классифицируют:
 |  |
Ионные – заряженные, Молекулярные –
являются сильными электронейтральные -
электролитами: неэлектролиты:
а) Катионные
[Ag(NH3)2]+Cl [Pt(NH3)2Cl4]0
[Cu(NH3)4]2+(OH)2 [Co(NH3)3(NO2)3]0
б) Анионные
Na[Al(OH)4]-
K3[Fe(CN)6]3-
Принята следующая запись внутренней сферы [M (L+)(L0)(L-)]:
1место – Ц.А. – М
2 место лиганды – L по порядку: положительные – L+
нейтральные – L0
отрицательные – L-
Факторы, влияющие на комплексообразующую способность Ц.А.:
1. Природа комплексообразователя:
а) самые хорошие комплексообразователи – это элементы f и d семейства,
б) далее идут элементы р –семейства,
в) слабые комплексообразователи – элементы s –семейства;
2. Величина заряда Ц.А.
Таблица 6 – Зависимость К.Ч. от заряда Ц.А.
| Заряд Ц.А. | Координационное число (К.Ч.) |
| 1+ (Ag+,Cu+) | |
| 2+ (Cu2+,Zn2+,Fe2+,Pt2+) | 4(6) |
| 3+(Fe3+,Co3+,Cr3+) | 6(4) |
| 4+(Pt4+,Pd4+) | 8(6) |
| Mo4+ |
Например: K2+[Pt2+(Cl-1)4]2- К.Ч. (Pt2+)=4
: K2+[Pt4+(Cl-1)6]2- -К.Ч. (P42+)=6
Вывод: чем больше величина заряда комплексообразователя, тем больше число противоположных частиц (К.Ч.)
3. Радиус (R) лигандов.
Например: 1)Na3[Al(F)6] (криолит) 2) Na[Al(Cl)4 ]
К.Ч (Al3+) = 6, R(F-) < К.Ч.(Al3+)=4 R(Cl-)>
Вывод: чем меньше радиус лиганда, тем больше величина К.Ч. (Ц.А.).
Лигандами могут быть:
1)электронейтральные молекулы, имеющие в своем составе донорные атомы: H2O, NH3, CO, SO2,NO, NO2,O2,N2, фосфины, амины, аминокислоты, спирты, кетоны, белки и т.д.)
2)ионы: H+,H-,OH-,F-,Cl-,Br--,J-,CN-,SCN-,NO2-, SO32-,S2- и т. д.
Дентантность лигандов – это число σ-связей, которые образуют лиганды с Ц.А.
Монодентантные лиганды образуют только одну σ-связей с Ц.А.
 Полидентантые лиганды образуют более одной σ-связей с Ц.А.
Полидентантые лиганды образуют более одной σ-связей с Ц.А.
2σ-св.-би,
3σ-св.-три, дентантные
4σ-св.-тетро,
Например, образование глицерата меди (II)
 | |||
 | |||

 H H
H H




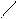

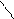
 CH2 O[H HO] :O – CH2 CH2 – О O – CH2
CH2 O[H HO] :O – CH2 CH2 – О O – CH2



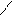
 Cu
Cu












 CH O: + Cu+2 [OH + H]O CH
CH O: + Cu+2 [OH + H]O CH  CH O О– CH + 2H2O
CH O О– CH + 2H2O
H H

 CH2OH OHCH2 CH2OH HOCH2
CH2OH OHCH2 CH2OH HOCH2
глицерат меди (II), р-р ярко-синего цвета
Комплексные соединения, в которых Ц.А. окружен полидентантными лигандами (подобно раку, который своей клешней захватывает добычу), называются клешневидными или внутрикомплексными, или хелатными.
В молекуле хелатов появляются устойчивые пяти- или шести-членные кольца (циклы).
Внутрикомплексные соединения – это такие соединения, в молекулах которых в результате процесса комплексообразования возникают устойчивые пяти или шестичленные циклы.
Хелатный эффект – повышенная устойчивость внутрикомплексных соединений за счет образования хелатных циклов.
Чем больше хелатных колец в молекуле, тем устойчивее молекула.
Устойчивые хелаты широко распространены в природе и играют важную биологическую роль в жизнедеятельности многих биологических систем.
Например, гемоглобин, в котором комплексообразователем является Fe2+, образующий 4 пятичленных хелатных кольца с атомами азота органических гетероциклов (порфиринов), выполняющих роль полидентантных лигандов. Хлорофилл (зеленый пигмент растений) содержит в качестве комплексообразователя Mg2+. Витамин В12, в котором комплексообразователь – Co3+.
Хелатные комплексы широко используются в аналитической химии.
Свойства ионных комплексных соединений:
1.Различают первичную и вторичную диссоциацию комплексных соединений. Например [Cu(NH3)4]SO4
Первичная диссоциация протекает по типу сильного электролита – необратимо (→) на ионы внешней и внутренней сферы, энергия ионной связи мала, поэтому связь слабая, легко рвется
[Cu(NH3)4]SO4→[Cu(NH3)4]2++SO42-
Вторичная диссоциация связана с диссоциацией внутренней сферы и протекает по типу слабого электролита обратимо (↔) и ступенчато (число ступеней равно К.Ч. комплексообразователя), т.к. разрываются прочные ковалентные σ-связи между комплексообразователем и лигандами с трудом, и конечным продуктом диссоциации являются ион Ц.А. и лиганд.
[Cu(NH3)4]2+↔ NH30+[Cu(NH3)3]2+
[Cu(NH3)3]2+↔ NH30+[Cu(NH3)2]2+
[Cu(NH3)2]2+↔ NH30+[Cu(NH3)]2+
[Cu(NH3)4]2+↔ NH3+Cu2+
Вывод константы нестойкости. Кн выводится по суммарному уравнению вторичной диссоциации:
V1
[Cu(NH3)4]2+↔ 4NH3 + Cu2+
(ж) (ж) (ж)
1) V1=V2 (ЗДМ)
2) V1=K1[Cu(NH3)42+]
3) V2=K2[NH3]4·[Cu2+]
4) K1[Cu(NH3)42+] = K2[NH3]4·[Cu2+]
5) K1/К2=[NH3]4·[Cu2+]/[Cu(NH3)42+]
6) K1/К2=Кр=Кд=К н
7) Кн = [NH3]4·[Cu2+] / [Cu(NH3)42+]
Кн - количественная характеристика устойчивости (прочности) комплексных ионов – величина постоянная (справочная)
Чем меньше величина Кн, тем устойчивее комплексное соединение.
Кн [Cu(NH3)4]2+=4,6∙10-14
Кн [Fe(CN)6]4-=5∙10-37 < , значит более устойчив
Часто используется К устойчивости – это обратная величина Кн.
Куст.=1/Кн
Чем > Куст., тем устойчивее (К.С.).
Раздел II. ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬННОЙ РАБОТЫ
Задание к тема 1. Основные классы неорганических соединений
а) напишите молекулярные и ионные уравнения, протекающие между предложенными веществами;
б) составьте уравнения реакций, протекающих в цепи превращений;
в) составьте уравнения всех реакций, протекающих между веществами;
г) назовите перечисленные ниже соединения и определите класс.
1. а) CO2: 1) HCl, 2) H2O, 3) KOH, 4) CaCO3 + H2O, 5) MgO;
б) Ca → CaO → Ca(OH)2 → CaCO3 → Ca(HCO3)2 → CaCl2;
в) H3PO4 и KOH;
г) KHCO3, Al2(SO4)3, Mg(OH)Cl, H2SO4, Fe2O3, KMnO4, HBr, H2O2.
2. а) Fe(OH)2: 1) CaO, 2) H2SO4, 3) KOH, 4) O2 + H2O, 5) SO3 (t˚);
б) P → P2O3 → P2O5 → H3PO4 → K2HPO4 → K3PO4;
в) Fe(OH)3 и HCl;
г) Al(OH)Cl2, CO, HMnO4, HCl, Fe(OH)3, KH2PO4, K2CrO4, CuSO4.
3. а) K2CO3: 1) HClO4, 2) H2O, 3) KOH, 4) HBr, 5) FeO;
б) Al2O3 → Al → Al(OH)3 → K[Al(OH)4] → AlCl3 → Al(OH)3;
в) Al(OH)3 и NaOH;
г) Cd(OH)2, K2CO3, H2S, BaO, Pb(ON)NO3, HclO4, FeCl3.
4. а) HCl: 1) Cu, 2) NH4OH, 3) Cu(OH)2, 4) K2SO4, 5) FeO;
б) S → SO2 → SO3 → H2SO4 → KHSO4 → K2SO4;
в) H2CO3 и Ca(OH)2;
г) K2O2, HI, PbO2, Ca(HCO3)2, Zn(NO3)2, Co(OH)2, Al(OH)2Cl.
5. а) CaO : 1) HNO3, 2) H2O, 3) KOH, 4) SO2, 5) Ca(HCO3)2;
б) Fe(OH)2 → FeO → Fe → FeCl2 → FeCl3 → Fe(OH)Cl2;
в) Fe(OH)3 и HNO3;
г) A2O3, AgNO3, FeSO4, HPO3, Mg(OH)2Cl, Zn(OH)2, NaHSO4, Cu2O.
6. а) KHCO3 : 1) H2SO4, 2) K2O, 3) KOH, 4) CO2, 5) Ca;
б) Cu2S → CuO → CuSO4 → Cu → CuCl2 → Cu(OH)Cl;
в) Al(OH)3 и NaOH;
г) Mn(OH)3, CO2, Al(NO3)3, Fe(OH)2Cl, H2CO3, Mg(HCO3)2, PH3.
7. а) KOH : 1) HClO, 2) Ca(OH)2, 3) CuSO4, 4) CO2, 5) Al(OH)Cl2;
б) C → CO → CO2 → H2CO3 → KHCO3 → K2CO3;
в) FeCl3 и KOH;
г) Mn2O7, Ba(OH)2, Ca3(PO4)2, HNO3, KHSO3, CoCl2, Zn(OH)NO3.
8. а) HClO4: 1) SO3, 2) FeO, 3) MnSO4, 4) HNO3, 5) NaOH;
б) PbO → Pb → Pb(NO3)2 → Pb(OH)2 → K2[Pb(OH)4] → K2SO4;
в) Al(OH)3 и HCl;
г) Fe(OH)2, Cl2O3, HBr, Mg(NO3)2, Na2O2, AlOHSO4, PbS, Kal(SO4)2.
9. а) FeO : 1) H2SO4, 2) Al2O3, 3) K2CO3, 4) CO2, 5) KOH;
б) N2 → NH3 → NO → NO2 → HNO3 → KNO3;
в) KH2PO4 и KOH;
г) H2CrO4, Cu(OH)2, Fe(OH)SO4, CaHPO4, Zn(NO3)2, BaBr2, MnO2.
10. а) Al(OH)Cl2: 1) HCl, 2) H2O, 3) NaOH, 4) K2CO3, 5) CO2;
б) KCl → K → K2O4 → H2O2→ O2 → ZnO;
в) H2S и Ba(OH)2;
г) SO3, H4P2O7, AlPO4, NaHSO3, Mn(NO3)2, Mg(OH)2, (FeOH)2SO4.
11. а) H2O: 1) K2O, 2) CO2, 3) MnCl2, 4) Al2O3, 5) H2SO4;
б) CaCl2 → Cl2 → KCl → HCl → FeCl2 → FeCl3;
в) H3PO4 и NaOH;
г) Cr2O3, HNO2, HCl, FeSO4, HclO4, Al(OH)3, KHCO3, Fe(OH)Cl2.
12. а) Na2SO3: 1) HCl, 2) BaCl2, 3) KOH, 4) CaSO4, 5) SO3;
б) Ca3N2 → NH3 → NH4Cl→ NH4OH → Al(OH)3 → Al2O3;
в) AlOHCl2 и KOH;
г) HBr, K2Cr2O7, OF2, NaI, KHSO4, Fe(OH)2Cl, H2SO3, Ba(OH)2.
13. а) H2CO3: 1) HCl, 2) CaCl2, 3) KOH, 4) SO2, 5) BaO;
б) SiO2 → K2SiO3 → H2SiO3 → SiO2 → Si → Ca2Si;
в) Cr(OH)3 и HNO3;
г) HPO3, Fe2(SO4)3, Al(OH)2Cl, Mg(HCO3)2, P2O5, H2S, Co(OH)2.
14. а) Al2O3 : 1) H2SO4, 2) CaO, 3) KOH, 4) SO2, 5) K2SO4;
б) Na → NaH → NaOH → Cu(OH)2 → K2[Cu(OH)4] → CuSO4;
в) Cr(OH)3 и NaOH;
г) Be(OH)2, H3BO3, Na2ZnO2, H2O2, Mn2O3, Cu(NO3)2, Co(OH)Cl.
15. а) NaOH: 1) ZnO, 2) SO2, 3) KHCO3, 4) Al(OH)Cl2, 5) H2S;
б) S → SO2 → H2SO3 → KHSO3 → K2SO3 → K2S2O3;
в) Fe(OH)2 и H2SO4;
г) HI, Ag2O, Pb(CH3ClO)2, [Fe(OH)2]2SO4, Ca(HCO3)2, Cu2S, CuOHCl.
16. а) CuSO4: 1) H2S, 2) BaCl2, 3) KOH, 4) HNO3, 5) CO2;
б) Ca → Ca(OH)2 → CaCO3 → CaO → Ca3(PO4)2 → CaSO4;
в) K2HPO и HCl;
г) Mg3N2, KH2PO4, Mn(OH)3, Al(OH)Cl2, NaHCO3, Zn(OH)2, K2Cr2O7.
17. а) Al(OH)3: 1) HClO4, 2) KCl, 3) KOH, 4) CaO + t˚, 5) CO2;
б) P → P2O3 → P2O5 → H3PO4 → NaH2PO4 → Na3PO4;
в) FeCl3 и KOH;
г) CrO3, FeOHCl, KOH, HClO4, KAlO2, CaHPO4, KAl(SO4)2, K2O2.
18. а) ZnO 1) H2SO4, 2) H2O, 3) NaOH, 4) CaO, 5) K3PO4;
б) Al2O3 → Al → Al(OH)3 → K[Al(OH)4] → AlCl3 → Al(OH)3;
в) Al(OH)2Cl и HCl;
г) H2SiO3, Pb(OH)NO3, KMnO4, Zn(NO3)2, Ba(OH)2, CuI, K2HPO4.
19. а) H2SO4: 1) KCl, 2) K2O, 3) Zn(OH)2, 4) CO2, 5) Zn;
б) S → SO2 → SO3 → H2SO4 → KHSO4 → K2SO4;
в) H3PO4 и NaOH;
г) Be(OH)2, H2SO4, Co(NO3)2, CdCl2, Cr2O3, Ca(HCO3)2, MnOHCl.
20. а) NaOH: 1) HCl, 2) Ba(OH)2, 3) Al(OH)2Cl, 4) FeCl2, 5) SO2;
б) Cr2O3 → Cr → CrCl3 → Cr(OH)3 → KCrO2 → K2CrO4;
в) Ni(OH)3 и HCl;
г) CuSO4, PbCl2, Mn2O7, K[Al(OH)4], H2CO3, AlOHSO4, KH.
21. а) CaO: 1) HCl, 2) CuSO4, 3) FeO, 4) CO2, 5) Al2O3;
б) Fe → FeCl3 → Fe(OH)3 → Fe2O3 → Fe → FeCl2;
в) CoCl2 и NaOH;
г) Al2(SO4)3, K2HPO4, H3PO4, MgOHCl, Mg(OH)2, PH3, N2O.
22. а) BeO: 1) HCl, 2) H2O, 3) NaOH, 4) K2O, 5) NaCl;
б) Cu → CuCl2 → Cu(OH)2 → CuO → Cu → Cu(NO3)2;
в) Cr(OH)3 и HBr;
г) CoS, Fe3O4, CuCl2, AlOHSO4, P2O5, NaHCO3, CO.
23. а) N2O5: 1) NaCl, 2) H2O, 3) KOH, 4) CaO, 5) CO2;
б) Si → SiO → K2SiO3 → H2SiO3 → KHSiO3 → K2SiO3:
в) Cr(OH)3 и HBr;
г) H2SO3, H2P4O7, K3[Fe(CN)6], Na2O2, NO, K3PO4.
24. а) HBr: 1) Zn, 2) KOH, 3) SO3, 4) FeO, 5) H2SO4;
б) N2 → NO → NO2 → HNO3 → Zn(NO3)2 → ZnO;
в) FeCl2 и KOH;
г) K2Cr2O7, NaHS, K4[Fe(CN)6], Pb(OH)2, H2O2, H4SiO4.
25. а) КОН: 1) Al, 2) H2O, 3) H3PO4, 4) SO2, 5) FeCl2;
б) K → K2S → S → SO2 → SO3 → H2SO4;
в) Al(OH)3 и HBr;
г) Fe2O3, KHSO4, Na[Al(OH)4], Fe(OH)3, SO3, HCN, CO2.
Задание к теме 2. Строение атома
1) составьте электронную формулу атома элемента с соответствующим порядковым номером;
2) графически изобразите валентные электроны в нормальном и возбужденном состояниях,
3) укажите окислительно-восстановительные свойства атома.
4) определите устойчивые степени окисления в нормальном и возбужденном состояниях;
| № варианта | Порядковый номер элемента | № варианта | Порядковый номер элемента | |
| 21 и 7 | 20 и 13 | |||
| 23 и 5 | 31 и 3 | |||
| 19 и 16 | 33 и 11 | |||
| 22 и 6 | 35 и 6 | |||
| 20 и 9 | 12 и 34 | |||
| 24 и 8 | 19 и 32 | |||
| 26 и 15 | 4 и 25 | |||
| 30 и 14 | 49 и 14 | |||
| 29 и 4 | 50 и 33 | |||
| 30 и 17 | 51 и 16 | |||
| 22 и 5 | 53 и 24 | |||
| 27 и 9 | 47 и 7 | |||
| 22 и 52 |
5) приведите примеры соединений в устойчивых степенях окисления,
6) укажите характер оксидов и гидроксидов.
Задание к теме 3. Ковалентная связь
Определите тип гибридизации и геометрию частиц по алгоритму:
1. Найдите центральный атом ц.а. в частице – тот атом, с.о. которого выше независимо от знака.
2. Определите число периферийных атомов –к.ч, которое указывает на число σ-связей.
3. Составьте графическое изображение валентных электронов ц.а. в соответствующей степени окисления.
4. Определите тип гибридизации, зная, что в гибридизации участвуют только те валентные А.О., которые образуют σ-связи (орбитали с неспаренными электронами, а также орбитали со спаренными электронами последнего энергетического уровня (Э.У.).
5. Изобразите гибридизацию рисунком.
6. Покажите перекрывания А.О. ц.а. с периферийными атомами.
7. Нарисуйте геометрию частицы.
| № варианта | Частицы | № варианта | Частицы |
| 1. | СН4, SO2 | 14. | PCl3, H2S |
| 2. | BeH2, CO2 | 15. | PF5, CO |
| 3. | BH3, SO3 | 16. | POCl3, SO3 |
| 4. | H2S, SF4 | 17. | PCl5, BCl3 |
| 5. | NH3, SCl6 | 18. | SO2, SeCl4 |
| 6. | SiH4, SF6 | 19. | H3PO4, SiO2 |
| 7. | BeCl2, SO2Cl2 | 20. | HClO, NH3 |
| 8. | BCl3, POCl3 | 21. | HClO3, H2O |
| 9. | SeH2, H2O | 22. | HClO2, PH3 |
| 10. | PH3, CO | 23. | HClO4, NH3 |
| 11. | [NH4]+, CO2 | 24. | H2CO3, SO2 |
| 12. | CCl4, NF3 | 25. | TeF6, PF5 |
| 13. | SiCl4, BeH2 |
Задание к теме 4. Энергетика химических реакций
1. Какие из приведённых реакций протекают самопроизвольно:
а) 4 HCl(г) + O2 = 2 H2O + Cl2;
б) N2 + 2 O2 = 2 NO2,
если: DG°обр.HCl = - 95,27 кДж/моль;
DG°обр.H2O = -237,5 кДж/моль;
DG°обр.NO2 = + 51,84 кДж/моль.
Ответ подтвердите, рассчитав DGх.р.
2. Восстановление PbO2 водородом протекает по уравнению:
PbO2 + H2 = H2O(г) + PbO, DНх.р. = - 182,8 кДж.
Определите теплоту образования PbO, если:
DН°обр.PbO2 = - 276,6 кДж/моль;
DН°обр.Н2О = - 241,84 кДж/моль.
3. Возможно ли самопроизвольное протекание реакции в стандартных условиях: 2 Al + Fe2O3 = Al2O3 + 2 Fe,
если: DG°обр.Fe2O3 = - 740,99 кДж/моль;
DG°обр.Al2O3 = - 1576,4 кДж/моль.
Ответ подтвердите расчётом.
4. Определите теплоту образования SO2, если для реакции:
SO2 + 2 H2S = 3 S + 2 H2O(ж), DНх.р. = - 1528 кДж.
и известны теплоты образования:
DН°обр.Н2О = - 285,84 кДж/моль;
DН°обр.Н2S = - 20,15 кДж/моль.
5. Исходя из величины DGх.р. определите, возможна ли реакция:
Al2O3 + 3 SO3 = Al2(SO4)3,
если: DG°обр.Al2O3 = - 1576,4 кДж/моль;
DG°обр.SO3 = - 370,37 кДж/моль;
DG°обр.Al2(SO4)3 = -3091,9 кДж/моль.
6. Окисление аммиака протекает по уравнению:
4 NH3 + 3 O2 = 2 N2 + 6 H2O(ж), DHх.р. = 1528 кДж.,
теплота образования воды (DН°обр.Н2О) равна - 285,84 кДж/моль.
Определите теплоту образования аммиака.
7. Можно ли использовать приведённую ниже реакцию для получения аммиака в стандартных условиях:
NH4Cl + NaOH(к) = NaCl(к) + NH3(г) + H2O?
Рассчитайте DG°х.р., если: DG°обр.Н2О = - 228,8 кДж/моль;
DG°обр.NH4Cl = - 343,64 кДж/моль;
DG°обр.NaOH = -377,0 кДж/моль;
DG°обр.NaCl = - 384,0 кДж/моль;
DG°обр.NH3 = - 16,64 кДж/моль.
8. Определите тепловой эффект реакции: 2 PbS + 3 O2 = 2 PbO + 2 SO2, зная стандартные значения теплот образования веществ:
DН°обр.PbS = - 94,28 кДж/моль;
DН°обр.PbO = -217,86 кДж/моль;
DH°обр.SO2 = -296,9 кДж/моль.
9. Какие из приведённых реакций протекают самопроизвольно:
а) 3 H2 + N2 « 2 NH3;
б) N2O4 « 2 NO2 (г),
если: DG°обр.NH3 = - 16,64 кДж/моль;
DG°обр.N2O4 = + 98,29 кДж/моль;
DG°обр.NO2 = + 51,84 кДж/моль.
Ответ подтвердите, рассчитав DGх.р.
10. Реакция горения сероуглерода идёт по уравнению:
CS2 + 3 O2 = CO2 + 2 SO2.
При получении 4,48 л. СО2, измеренных при нормальных условиях, выделяется 223 кДж тепла. Вычислить тепловой эффект реакции.
11. Прямая или обратная реакция будет протекать при стандартных условиях в системе: СН4 (г) + СО2 (г) « 2 СО (г) + 2Н2 (г), если:
DG°обр.СН4 = - 50,79 кДж/моль;
DG°обр.СО2 = - 394,38 кДж/моль;
DG°обр.СO = - 137,27 кДж/моль?
Рассчитайте DG прямой реакции.
12. Определите теплоту образования РН3 из уравнения реакции:
2 РН3 + 4 О2 = Р2О5 + 3 Н2О, DНх.р. = - 2360 кДж., если известно, что DН°обр.Р2О5 = - 1492,0 кДж/моль;
DН°обр.Н2О = - 285,8 кДж/моль.
13. Разложение нитрата аммония возможно по двум схемам:
а) NH4NO3 = N2O + 2 H2O;
б) NH4NO3 = N2 + ½ O2 + 2 H2O. Какая реакция более вероятна?
DG°обр.NH4NO3 = - 176,0 кДж/моль;
DG°обр.H2О = - 218,0 кДж/моль;
DG°обр.N2О = 103,6 кДж/моль.
14. Вычислите, сколько тепла выделяется при сгорании 200 литров метана по реакции: СН4 + 2 О2 = СО2 + 2 Н2О, если известно, что
DН°обр.СН4 = - 74,84 кДж/моль;
DН°обр.СО2 = - 393,5 кДж/моль;
DН°обр.Н2О = -285,8 кДж/моль.
15. Какие из перечисленных оксидов могут быть восстановлены водородом до свободного металла при 298 К: СаО, SnO2, Al2O3, если известны стандартные изобарные потенциалы образования веществ:
DG°обр.Н2О = - 237,8 кДж/моль; DG°обр.СаО = - 604,2 кДж/моль;
DG°обр.SnO2 = - 519,3 кДж/моль; DG°обр.Al2О3 = 1582 кДж/моль.
16. Вычислите тепловой эффект реакции при стандартных условиях:
C6H6 + 15/2 O2 = 6 CO2 + 3 H2O,
если: DН°обр.С6Н6 = 82,9 кДж/моль;
DН°обр.Н2О = - 285,84 кДж/моль;
DН°обр.СО2 = - 393,5 кДж/моль.
17. Прямая или обратная реакция будет протекать при стандартных условиях в системе: 2 NO + O2 « 2 NO2,
если: DG°обр.NО = 86,69 кДж/моль;
DG°обр.NO2 = 51,84 кДж/моль?
18. Вычислите тепловой эффект реакции:
Fe2O3 + 3 H2 = 2 Fe + 3 H2O,
если теплоты образования веществ известны:
DН°обр.Н2О = - 285,84 кДж/моль;
DG°обр.Fe2О3 = - 822,2 кДж/моль.
19. Определить, пойдёт ли самопроизвольно следующая реакция:
СО2 + 4 Н2 = СН4 + 2 Н2О
при следующих данных:
DS°обр.СО2 = 0,231 кДж/моль *К; DН°обр.СО2 = - 393,5 кДж/моль;
DS°обр.Н2 = 0,13 кДж/моль *К; DН°обр.СН4 = - 74,8 кДж/моль;
DS°обр.СН4 = 0,186 кДж/моль *К; DН°обр.Н2О = - 285,84 кДж/моль.
DS°обр.Н2О = 0,07 кДж/моль *К.
20. Сколько тепла можно получить от сжигания 80 г метана? Теплота сгорания метана равна – 890 кДж.
21. На основании стандартных теплот образования и абсолютных стандартных энтропий веществ определите, пойдёт ли самопроизвольно следующая реакция:
4 NH3 (г) + 5 O2 (г) = 4 NO(г) + 6 H2O(г)
при следующих данных:
DS°обр.NH3 = 0,192 кДж/моль *К; DН°обр.NH3 = - 46,19 кДж/моль;
DS°обр.O2 = 0,205 кДж/моль *К; DН°обр.NO = + 37,90 кДж/моль;
DS°обр.NO = 0,210 кДж/моль *К; DН°обр.Н2О = - 241,84 кДж/моль.
DS°обр.Н2О = 0,188 кДж/моль *К.
22. Вычислите, сколько тепла выделится при сгорании 165 л. (н.у.) ацетилена С2Н2, если продуктами сгорания являются диоксид углерода и пары воды и выделяется 786 кДж тепла.
23. Возможна ли реакция при Т = 500 К:
Fe2O3 (к) + 3 С = 2 Fe + 3 CO
При следующих данных:
DS°обр.Fe2O3 = 0,089 кДж/моль *К; DН°обр.Fe2O3 = 822,1 кДж/моль;
DS°обр.C = 0,006 кДж/моль *К; DН°обр.СO = 110,52 Дж/моль;
DS°обр.Fe = 0,027 кДж/моль *К;
DS°обр.CO = 0,197 кДж/моль *К.
24. При сгорании 11,5 г жидкого этилового спирта выделилось 308,71 кДж. тепла. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксид углерода.
25. На основании стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите DGх.р.:
С2Н4 (г) + 3О2 (г) = 2 СО2 (г) + 2 Н2О(ж)
DS°обр.С2Н4 = - 0,022 кДж/моль *К; DН°обр.С2Н4 = 52,28 кДж/моль;
DS°обр.О2 = 0,210 кДж/моль *К; DН°обр.СО2 = - 391,51 Дж/моль;
DS°обр.СО2 = 0,213 кДж/моль *К; DН°обр.Н2О = 285,84 кДж/моль;
DS°обр.Н2O= 0,007 кДж/моль *К.
Задание к теме 5. Кинетика химических реакций
1. Выведите константу равновесия для обратимой реакции:
CuO +H2 « Cu +H2O
к. г. к. г.
2. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
2 SO2 +O2 « 2 SO3; DHp. = - 196,6 кДж.
Вычислите равновесную концентрацию SO2 и O2, если их исходные концентрации соответственно равны 8 и 6 моль/л, а [SO3]равн.=4моль/л
3. Выведите константу равновесия для обратимой реакции:
Fe2O3 + CO « 2 FeO + CO2.
к. г. к. г.
Найдите равновесные концентрации СО и СО2, если их начальные концентрации соответственно равны 0,05 и 0,01 моль/л , а константа равновесия при 1000˚С равна 0,5.
4. Реакция окисления оксида серы: 2 SO2 + O2 « 2 SO3, началась при концентрации SO2 = 0,06 моль/л. и O2 = 0,05 моль/л. К моменту наступления равновесия [SO3] = 0,02 моль/л. Вычислите равновесные концентрации остальных веществ.
5. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
2 CO + O2 « 2 CO2; DHp. = - 566 кДж.
Выведите константу равновесия.
6. Выведите константу равновесия для обратимой реакции:
CaCO3 « CaO +CO2 + ΔН
к. к. г.
В каком направлении будет смещаться равновесие с повышением температуры в данной реакции?
7. В реакции: N2 + 3 H2 « 2 NH3, в состоянии равновесия концентрации веществ были следующие: N2 = 0,1 моль/л, H2 = 0,3 моль/л, NH3 = 0,4 моль/л. Вычислите исходные концентрации азота и водорода.
8. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
4 HCl + O2 « 2 Cl2 +2 H22O; DHp. = -202,4 кДж.
г. г. г. ж.
Выведите константу равновесия системы.
9. Выведите константу равновесия для обратимой реакции:
CO2 + C « 2 CO.
г. к. г.
В каком направлении будет смещаться равновесие с повышением давления.
10. При 508 °С константа скорости реакции: H2 + I2 « 2 HI, равна 0,16 моль/л*мин. Исходные концентрации Н2 = 0,04 моль/л, а I2 = 0,05 моль/л. Вычислите начальную скорость и скорость в тот момент, когда концентрация водорода станет равной 0,03 моль/л.
11. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
3 O2 « 2O3; DHp. = 184,6 кДж.
Выведите константу равновесия системы.
12. В системе: CO(Г) + Cl2(Г) « COCl2(Г), начальные концентрации CO и Cl2 были равны 0,28 моль/л и 0,09 моль/л; равновесная концентрация COСl2 равна 0,02 моль/л. Найдите константу равновесия.
13. Выведите константу равновесия для обратимой реакции:
SO3(г) + C(к) « SO2(г) + CO(г). В каком направлении будет смещаться равновесие с повышением давления?
14. Начальные концентрации веществ, участвующих в реакции: 4HCl+O2«2Cl2+2H2O, составляют: HCl–4,8 моль/л, O2–1,8моль/л, Cl2–0,01моль/л. Определите концентрации всех реагирующих веществ после того, как концентрация О2 уменьшилась до 1,0 моль/л.
15. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
N2 + O2 « 2 NO; DHр. = 180,7 кДж.
Выведите константу равновесия.
16. Выведите константу равновесия для обратимой реакции:
2 SO2 + O2 « 2SO3.
г. г. г.
Вычислите равновесную концентрацию SO2 и O2, если их исходные концентрации соответственно равны 6 и 4 моль/л, а [SO3]равн.=2 моль/л
17. В каком направлении будет смещаться равновесие с повышением температуры и давления для реакции:
CO + Cl2 « COСl2; DHp. = 112,5 кДж.
Вычислите Кр и начальную концентрацию хлора и СО, если равновесная концентрация вещества: [COСl2] = 0,3 моль/л, [CO] = 0,2 моль/л, [Cl2] = 1,2 моль/л
18. Выведите константу равновесия для обратимой реакции:
2H2S + 3 O2 « 2 SO2 + 2 H2O.
г. г. г. г.
В каком направлении будет смещаться равновесие с повышением давления в системе?
19. При синтезе аммиака к данному моменту времени прореагировало 0,9моль/л водорода, его начальная концентрация была равна 1,4 моль/л. Определите концентрацию оставшегося водорода и прореагировавшего азота. Выведите константу равновесия системы.
20. Выведите константу равновесия для обратимой реакции:
CaO + 3 C « CaC2 + CO.
к. к. к. г.
21. Для реакции: FeO(К) + CO(Г) « Fe(К) + CO2(Г) константа равновесия при 1000°С равна 0,5. Начальные концентрации СО и СО2 были соответственно равны 0,05 моль/л и 0,01 моль/л. Найдите их равновесные концентрации.
22. В каком направлении будет смещаться равновесие с повышением температуры и понижением давления для реакции:
N2 + 3 H2 « 2 NH3; DHp. = -92,4 кДж?
Каковы исходные концентрации водорода и азота, если: равновесные концентрации: [H2] = 9 моль/л, [N2] = 3 моль/л, [NH3] = 4 моль/л.
23. Концентрация NO и O2, образующих NO2 были соответственно равны 0,03моль/л и 0,05 моль/л. Как изменится скорость реакции, если концентрацию О2 повысить до 0,1 моль/л, а NO – до 0,06 моль/л?
24. Выведите константу равновесия для обратимой реакции:
4 P + 5 O2 « 2 P2O5.
к. г. к.
25. В процессе реакции, протекающей по уравнению: 2 А +3 В « С. За определённый промежуток времени концентрация вещества А уменьшилась на 0,3 моль/л. Как изменилась при этом концентрация вещества В и скорость реакции?
Задание к теме 6. Способы выражения концентраций растворов
1. Какую массу воды следует прибавить к раствору КОН массой 150 г и массовой долей 2 %, чтобы получить раствор с массовой долей КОН 1% и ρ=1,008 г/см3? Рассчитайте: См, Сн 1 % раствора КОН.
2. На нейтрализацию 25 мл 0,1 н раствора щавелевой кислоты (Н2С2О4) израсходовано 20 мл гидроксида натрия. Рассчитайте Сн щелочи.
3. К 80 г раствора хлорида калия с массовой долей вещества 15 % прибавили 20 г воды. Рассчитайте ω %, Сн, См полученного раствора.
4. Какой объём 0,1 н раствора гидроксида калия потребуется на нейтрализацию 20 мл 0,2 н раствора азотной кислоты?
5. Смешали 300 г 20 % раствора и 500 г 30 % раствора соляной кислоты. Рассчитайте ω %, Сн, См полученного раствора.
6. На нейтрализацию 25 мл 0,1 н раствора КОН израсходовано 50 мл раствора соляной кислоты. Рассчитайте Сн кислоты.
7. Какую массу воды следует прибавить к 200 мл 30 % раствора гидроксида калия плотностью 1,33 г/см3, чтобы получить раствор с массовой долей КОН 10 % и ρ = 1,08 г/см3? Рассчитайте: См, Сн полученного раствора КОН.
8. На нейтрализацию 30 мл 0,16 н раствора гидроксида натрия израсходовано 50 мл раствора серной кислоты. Рассчитайте Сн кислоты.
9. Смешали 10 мл 10 % раствора азотной кислоты плотностью 1,054 г/см3 и 100 мл 30 % раствора того же вещества плотностью 1,184 г/см3. Рассчитайте
ω %, Сн, См полученного раствора.
10. На нейтрализацию 50 мл 0,15 н раствора гидроксида натрия израсходовано 45 мл соляной кислоты. Рассчитайте Сн кислоты.
11. К 500 мл 32 % азотной кислоты плотностью 1,20 г/см3 прилили 1 л воды. Чему равна ω %, Сн, См полученного раствора?
12. Какой объём 0,05 н раствора серной кислоты потребуется на нейтрализацию 100 мл 0,1 н раствора гидроксида калия?
13. Сколько воды надо прибавить к 0,1 л 40% раствора гидроксида калия плотностью 1,411 г/см3, чтобы получить 18 % раствор плотностью 1,16г/см3? Рассчитайте Сн, См полученного раствора.
14. Какой объём 0,05 н раствора щавелевой кислоты (Н2С2О4) потребуется на нейтрализацию 20 мл 0,1 н раствора гидроксида натрия?
15. К 256,4 мл 96 % серной кислоты плотностью 1,84 г/см3 прилили воду объёмом 800 мл. Чему равна ω %, Сн, См полученного раствора?
16. Какой объём 0,1 н раствора азотной кислоты потребуется на нейтрализацию 50 мл 0,15 н раствора гидроксида калия?
17. Сколько воды нужно прибавить к 10 кг раствора гидроксида натрия с массовой долей 80 %, чтобы получить раствор с массовой долей 20 % и плотностью 1,22 г/см3? Рассчитайте См, Сн 20 % щелочи.
18. Определите нормальность раствора азотной кислоты, если на нейтрализацию 20 мл её израсходовано 18 мл 0,1 н раствора гидроксида калия.
19. Из 300 г 10 % раствора хлорида натрия выпариванием удалили 150 г воды. Чему равна ω %, Сн, См полученного раствора?
20. Определите объём 0,05 н раствора щавелевой кислоты (Н2С2О4) необходимый на нейтрализацию 20 мл 0,1 н раствора гидроксида натрия.
21. К 500 мл раствора серной кислоты с массовой долей кислоты 87% добавили 2 л воды. Чему равна ω %, Сн, См полученного раствора?
22. На нейтрализацию 50 мл 0,5 н раствора гидроксида натрия израсходовано 25 мл серной кислоты. Рассчита
