Тема 4. энергетика химических реакций
 |
| Термохимия – изучает тепловые эффекты химических реакций (первый и второй законы термодинамики) | Тепловой эффект химической реакции – тепло, которое выделяется или поглощается в данной химической реакции. | Система – всякий материальный объект, состоящий из большого числа частиц и обособленный от окружающей среды физическими или воображаемыми границами. |
 Первый закон термодинамики:
Первый закон термодинамики:
Тепло, сообщаемое системе (Q) расходуется на изменение её внутренней энергии (DU) и на совершение работы против сил внешнего давления (А).
|
|
, где А = р *DV Þ
 |
Система перешла из состояния 1 в состояние 2
|
| ||||
 | |||||

 состояние 1 состояние 2
состояние 1 состояние 2
начальное конечное
 Химические реакции
Химические реакции
 |  | ||
Изобарные (р – const) Изохорные (V – const)


 1 (U1, V1, p – const) 1 (U1, V – const) DV = 0
1 (U1, V1, p – const) 1 (U1, V – const) DV = 0
 2 (U2, V2, p – const) 2 (U2, V – const)
2 (U2, V2, p – const) 2 (U2, V – const)
|
сгруппируем относительно
1-ого и 2-ого состояния
Qp = (U2 + p *V2) – (U1 + p *V1)
U + p *V = H (энтальпия)
Теплосодержание системы
Qp = H2 – H1, QР = DH Qv = DU
Вывод: тепловой эффект химической реакции равен:


 изменению энтальпии системы изменению внутренней энергии
изменению энтальпии системы изменению внутренней энергии
системы
! Таких реакций больше.
 Термохимические уравнения характеризуются признаками:
Термохимические уравнения характеризуются признаками:
а) отражено фазовое состояние (г., ж., тв.);
б) возможны дробные коэффициенты;
в) коэффициенты показывают число моль реагирующих и образующихся веществ;
г) указывается тепловой эффект
 |  |
 ЭкзотермическиеЭндотермические
ЭкзотермическиеЭндотермические
Протекают с выделением тепла Протекают с поглощением тепла
(теплосодержание системы (теплосодержание системы
уменьшается) возрастает)
|
|
 |
Закон Гесса»:тепловой эффект химической реакции не зависит от пути протекания реакции, а зависит от начального и конечного состояния системы.
 С + О2 DH1 СО2 DН1 = DН2 + DН3
С + О2 DH1 СО2 DН1 = DН2 + DН3
гр. г. г. DН2 = DН1 - DН3

 + DН3
+ DН3
½ Изменение энергии (DН) часто изображают треу -
O2 О2 гольником, стороны которого – разные пути проте -
 DН2 ½ кания реакции(DН2 нельзя непосредственно изме -
DН2 ½ кания реакции(DН2 нельзя непосредственно изме -
СО(г) + рить в лаборатории)
 Первое следствие из закона Гесса:
Первое следствие из закона Гесса:
Тепловой эффект химической реакции (DНх.р.) равен сумме стандартных теплот образования (DН °обр.) конечных продуктов реакции за вычетом суммы
стандартных теплот образования исходных веществ с учётом стехиометрических коэффициентов (n).
|
n – стехиометрические коэффициенты
DН °обр. – стандартная теплота образования
- это тепло, которое выделяется или поглощается при образовании 1 моль сложного вещества из простых молекул или атомов.
DН °обр. (кДж/моль)– справочная величина.

 Системы
Системы
 |  | ||
Изолированная Открытая
(модельная, теоретическая) – нет (реальная) – есть теплообмен с
теплообмена с окружающей средой окружающей средой энергией и







 веществом
веществом
 |










 изоляция
изоляция
 |  |
 Энтропия - D S = DQ Чем тело больше нагрето, тем вероятнее,
Энтропия - D S = DQ Чем тело больше нагрето, тем вероятнее,
 T что оно будет охлаждаться сильнее.
T что оно будет охлаждаться сильнее.
    Изменение энтропии в изолированной системе. Изменение энтропии в изолированной системе. DSA = - ΔQА - ΔTA тепло, которое тело А отдаёт телу В. DSв = + ΔQВ - TВ тепло, которое тело В получает.
DS системы = DSА + DSВ = - ΔQA + ΔQB TA TB
TВ TA
Второй закон термодинамики В изолированных системах самопроизвольно протекают только такие процессы, в которых энтропия возрастает. DS > 0 Энтропия - DS – мера беспорядка в системе (справочная величина) DSо обр. – Дж/моль *К |  Изменение свободной энергии Гиббса (изобарно- изотермического потенциала) для реальных (открытых) систем DGх.р. – критерий самопроизвольного протекания химической реакции. DGх.р. – свободная энергия. DНх.р. – полная энергия (энтальпийный фактор) Т *DS – связанная энергия (энтропийный фактор) 1. Химическая реакция возможна, если DGх.р. < 0 2.Химическая реакция невозможна, если DGх.р. > 0 3. В системе наступило динамическое химическое равновесие, если DGх.р. = 0 Изменение свободной энергии Гиббса (изобарно- изотермического потенциала) для реальных (открытых) систем DGх.р. – критерий самопроизвольного протекания химической реакции. DGх.р. – свободная энергия. DНх.р. – полная энергия (энтальпийный фактор) Т *DS – связанная энергия (энтропийный фактор) 1. Химическая реакция возможна, если DGх.р. < 0 2.Химическая реакция невозможна, если DGх.р. > 0 3. В системе наступило динамическое химическое равновесие, если DGх.р. = 0 |
|
Свободную энергию Гиббса можно рассчитать 2 способами:
 Расчет DGх.р.
Расчет DGх.р.




 -ΔQA = ΔQB , так как теплообмен возможен только между телами
-ΔQA = ΔQB , так как теплообмен возможен только между телами
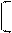 DS системы = ΔQB 1 – 1 >0
DS системы = ΔQB 1 – 1 >0