Тема 1. введение. классификация, номенклатура и изомерия органических соединений
ТЕМА 1. ВВЕДЕНИЕ. КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА И ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Введение. Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с познанием их биологических функций. Основными объектами ее изучения служат биологические полимеры (биополимеры) и биорегуляторы.
Биополимеры– высокомолекулярные природные соединения, являющиеся структурной основой всех живых организмов и играющие определенную роль в процессах жизнедеятельности. К биополимерам относят пептиды и белки, полисахариды (углеводы), нуклеиновые кислоты. В эту группу включают и липиды, которые сами по себе не являются высокомолекулярными соединениями, но в организме обычно связаны с другими биополимерами.
Биорегуляторы – соединения, которые химически регулируют обмен веществ. К ним относят витамины, гормоны, многие синтетические биологически активные соединения, в том числе лекарственные вещества.
Биоорганическая химия неразрывно связана с органической химией, базируется на её идеях и методах, т.к. большинство компонентов живой материи представлено органическими соединениями. Они могут синтезироваться в организме, поступать извне или модифицироваться в нем. Живой организм является «химическим производством», в каждой клетке его непрерывно протекают тысячи различных химических реакций, обеспечивающих существование и развитие организма.
Совокупность химических реакций, протекающих в организме, называют обменом веществ, или метаболизмом. Вещества, образующиеся в клетках, тканях и органах растений и животных в процессе метаболизма, называют метаболитами.
Метаболизмвключает два направления – катаболизм и анаболизм.
К катаболизму относят реакции распада веществ, попадающих в организм с пищей. Как правило, они сопровождаются окислением органических соединений и протекают с выделением энергии.
Анаболизм – синтез сложных молекул из более простых, в результате которого осуществляется образование и обновление структурных элементов живого организма.
Метаболические процессы протекают с участием ферментов, т. е. специфических белков, которые находятся в клетках организма и играют роль катализаторов биохимических процессов (биокатализаторы).
Метаболиты – естественные, присущие организму вещества. С другой стороны, существуют соединения, называемые антиметаболитами, т. е. являющиеся антагонистами естественных метаболитов. К ним относятся природные или синтетические биологически активные соединения, близкие по строению к метаболитам и вступающие с ними в конкуренцию в биохимических процессах. Антиметаболиты (в силу своего структурного сходства) способны вступать вместо метаболитов в биохимические реакции, которые с их участием будут заканчиваться иным результатом, чем с участием метаболитов.
Современная теория строения органических соединений создана выдающимся русским учёным А.М. Бутлеровым.
Основные положения теории строения органических соединений А.М. Бутлерова
1. Атомы в молекуле располагаются в определенной последовательности согласно их валентности. Валентность атома углерода в органических соединениях равна четырем.
2. Свойства веществ зависят не только от того, какие атомы и в каких количествах входят в состав молекулы, но и от того, в каком порядке они соединены между собой.
3. Атомы или группы атомов, входящих в состав молекулы, взаимно влияют друг на друга, от чего зависят химическая активность и реакционная способность молекул.
4. Изучение свойств веществ позволяет определить их химическое строение.
Взаимное влияние соседних атомов в молекулах является важнейшим свойством органических соединений. Это влияние передается или по цепи простых связей или по цепи сопряженных (чередующихся) простых и двойных связей.
Сопряженные системы
Различают два типа сопряженных систем (и сопряжений).
 1. p, p-сопряжение — электроны делокализованы между двумя (и более) кратными связями. Например, в делокализации электронов в молекуле бутадиена участвуют четыре атома углерода: СН2=СН–СН=СН2 « СН2–¾СН–¾СН–¾СН2
1. p, p-сопряжение — электроны делокализованы между двумя (и более) кратными связями. Например, в делокализации электронов в молекуле бутадиена участвуют четыре атома углерода: СН2=СН–СН=СН2 « СН2–¾СН–¾СН–¾СН2
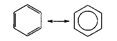 В молекуле бензола делокализация происходит с участием 6 атомов углерода (три двойные связи, каждую образует 2 электрона, по одному от каждого атома):
В молекуле бензола делокализация происходит с участием 6 атомов углерода (три двойные связи, каждую образует 2 электрона, по одному от каждого атома):
Кроме того, при осуществлении «кругового» сопряжения, как в бензоле, система получает дополнительный существенный выигрыш энергии, называемый энергией сопряжения. Например, энергия сопряжения молекулы бензола равна 15 кДж/моль.
2. р, p-сопряжение — в делокализации принимают участие электроны p-связи и р-орбитали гетероатома; например, в молекулах ацетамида и пиррола:
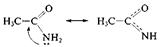 | 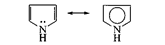 | ||
В случае молекулы ацетамида в делокализации участвуют три атома (С, О, N); в случае молекулы пиррола — пять атомов (4 атома С и атом N). Чем длиннее система сопряжения, тем более она устойчива. Ароматическая система представляет собой устойчивую плоскую циклическую сопряженную полиеновую структуру, содержащую (4п + 2) p-электронов (п = 1, 2, 3, ...). Например, бензол – ароматическая структура (6 p-электронов), а 1,3,5,7-циклооктатетраен – нет (8 p-электронов).
Делокализация электронов является одним из важных факторов повышения устойчивости молекул и ионов, поэтому это явление широко распространено в биологически важных молекулах (витамины, гем, хлорофилл, гемоглобин и др.).
Витамин А относится к сесквитерпенам (терпены – 10 углеродов и 3 дв. связи), содержится в масле, молоке, яичном желтке, рыбьем жире; свиное сало и маргарин его не содержат. Это витамин роста; недостаток его в пище вызывает убыль в весе, высыхание роговицы глаз, понижение сопротивляемости к инфекции. Витамин А заменяют каротином (тритерпен) С40Н56, (пигмент моркови); в организме человека каротин превращается в витамин А.

 Н3С
Н3С




 Н3С СН3 СН3 СН3
Н3С СН3 СН3 СН3

 СН=СН–С=СН–СН=СН–С=СН–СН=СН–СН=С–СН=СН–СН=С–СН=СН–
СН=СН–С=СН–СН=СН–С=СН–СН=СН–СН=С–СН=СН–СН=С–СН=СН–
СН3 СН3
СН3 b-каротин Н3С СН3


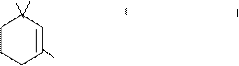 Н3С СН3 СН3 СН3
Н3С СН3 СН3 СН3
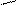 СН=СН–С=СН–СН=СН–С=СН–СН2 – ОН
СН=СН–С=СН–СН=СН–С=СН–СН2 – ОН
СН3 витамин А
В молекуле хлорофилла также присутствует развитая система сопряжённых связей – 4 остатка пиррола, образующих вместе порфириновое ядро, связанное с атомом магния. Хлорофилл — сложный эфир двухосновной кислоты и спиртов — метанола и фитола С20Н39ОН. По строению он близок к дыхательным ферментам (каталазе, пероксидазе) и к красящему веществу крови — гему.
Классификация органических соединений основана на анализе двух аспектов строения молекул – строения углеродного скелета и наличия функциональных групп.
 |
Рис. 1. Классификация органических соединений по строению углеродного скелета
Примеры алифатических углеводородов:
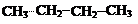 | |||||
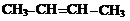 | 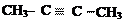 | ||||
предельные непредельные
алкан алкен (двойная связь) алкин (тройная связь)
Примеры 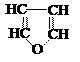
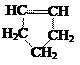
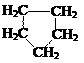 циклических углеводородов:
циклических углеводородов:
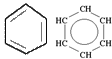 | |||
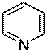 | |||
карбоциклические гетероциклические
предельное непредельное ароматическое непредельное ароматическое
Ряд сходных по строению соединений, обладающих близкими химическими свойствами, в котором отдельные члены ряда отличаются друг от друга лишь количеством групп –СН2–, называется гомологическим рядом, а группа –СН2– гомологической разностью.
Для любого гомологического ряда может быть выведена общая формула. Так, СпН2п+2 – формула алканов, СпН2п+1ОН – алифатических одноатомных спиртов.
Таблица 1. Классы производных углеводородов по наличию функциональных групп
| Функциональная группа | Класс | Пример |
| атомы галогенов (F, Cl, Br, I) | галогенопроизводные | СН3СН2Cl (хлорэтан) |
| гидроксильная (–ОН) | спирты (фенолы) | СН3СН2ОН (этанол, первичный спирт) СН3СН(ОН)СН3 (2-пропанол, вторичный спирт) |
| тиольная или меркапто- (–SН) | тиолы (меркаптаны) | СН3СН2SН (этантиол) |
| эфирная (–О–) | простые эфиры | СН3СН2–О–СН2СН3 (диэтиловый эфир) |
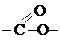 сложноэфирная сложноэфирная | сложные эфиры | СН3СН2СООСН3 (метиловый эфир уксусной кислоты или метилацетат) |
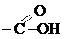 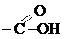 карбоксильная карбоксильная | карбоновые кислоты | 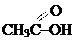 (уксусная кислота) (уксусная кислота) |
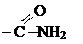 амидная амидная | амиды карбоновых кислот | 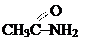 (амид уксусной кислоты или ацетамид) (амид уксусной кислоты или ацетамид) |
| карбонильная (–С=О) | альдегиды и кетоны | 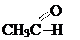 СН3СОСН3 (этаналь) (пропанон) СН3СОСН3 (этаналь) (пропанон) |
| сульфо- (–SО3Н) | сульфокислоты | СН3SО3Н (метансульфокислота) |
| амино- (–NH2) | амины | СН3СН2NH2 (этиламин, первичный амин) СН3NHСН3 (диметиламин, вторичный амин) |
| нитро- (–NO2) | нитросоединения | СН3СН2NО2 (нитроэтан) |
Атомы углерода, непосредственно соединенные с одним другим углеродным атомом называются первичными, соединенные с двумя атомами углерода – вторичными, с тремя другими атомами углерода – третичными, с четырьмя атомами С – четвертичными.
Номенклатура органических соединений: тривиальная, рациональная и систематическая номенклатура. Тривиальная номенклатура – совокупность исторически сложившихся названий. Так, по названию сразу понятно, откуда были выделены яблочная, янтарная или лимонная кислота, каким способом была получена пировиноградная кислота (пиролиз виноградной кислоты), знатоки греческого языка легко догадаются, что уксусная кислота – это что-то кислое, а глицерин – сладкое. Но название не отражает строение вещества.
Рациональная номенклатура строит название соединения на основании структуры более простого соединения (первого члена гомологического ряда). СН3ОН – карбинол, СН3СН2ОН – метилкарбинол, СН3СН(ОН)СН3 – диметилкарбинол и т.д.
По номенклатуре IUPAC (международная номенклатура), названия углеводородов и их функциональных производных базируются на названии соответствующего углеводорода с добавлением префиксов и суффиксов, присущих данному гомологическому ряду.
Алгоритм создания названия органического соединения:
1) выбрать в качестве основного углеродного скелета наиболее длинную последовательность углеродных атомов и назвать, обращая внимание на степень ненасыщенности соединения;
2) выявить все имеющиеся в соединении функциональные группы;
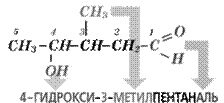 3) установить, какая группа является старшей (см. табл. 2), название этой группы отражается в названии соединения в виде суфикса и его ставят в конце названия соединения; все остальные группы дают в названии в виде приставок.
3) установить, какая группа является старшей (см. табл. 2), название этой группы отражается в названии соединения в виде суфикса и его ставят в конце названия соединения; все остальные группы дают в названии в виде приставок.
4) пронумеровать углеродные атомы основной
цепи, начиная со старшей группы;
5) перечислить приставки в алфавитном порядке
(умножающие добавки ди-, три- и т.д. не учитываются);
6) составить полное название соединения.
Начинать строить название соединения надо с названия родоначальной структуры, для чего абсолютно необходимо знать наизусть названия первых 10 членов гомологического ряда алканов (метан, этан, пропан, бутан, пентан, гексан, гептан, октан, нонан, декан). Также надо знать названия образующихся из них радикалов – при этом окончание –ан меняется на –ил.
Таблица 2. Номенклатура органических соединений
| Класс соединений | Функциональная группа | Приставка | Суффикс или окончание |
| карбоновые кислоты | - СООН | карбокси- | -овая кислота |
| сульфокислоты | – SO3H | cульфо- | сульфоновая кислота |
| нитрилы | – C º N | циан- | - нитрил |
| альдегиды | - СНО | оксо- | -аль |
| кетоны | – С = О | оксо- | -он |
| спирты | - ОН | гидрокси- | -ол |
| тиолы | – SH | меркапто- | -тиол |
| амины | - NН2 | амино- | -амин |
| алкены | – С = С – | - | -ен |
| алкины | - С ≡ С - | - | -ин |
| галогенопроизводные | -Br, -I, -F, -Cl | бром-, иод-, фтор-, хлор- | -бромид, -иодид, -фторид, -хлорид |
| нитросоединения | -NO2 | нитро- | - |
| углеводородные радикалы | СН3 – СН3СН2 – СН3СН2СН2 –  СН3СН – СН3 СН3СН – СН3 | метил- этил- пропил- изопропил- | – – – – |
В названиях спиртов, альдегидов, кетонов, карбоновых кислот, амидов, нитрилов, галогенангидридов суффикс, определяющий класс, следует за суффиксом степени ненасыщенности: например, 2-бутеналь. Соединения, содержащие другие функциональные группы, называются как производные углеводородов, например, 1-хлорпропан.
Названия кислотных функциональных групп помещают после названия углеводородного скелета: например, бензолсульфокислота.
Эфиры карбоновых кислот называются как производные родоначальных кислот. Окончание –овая кислота заменяется на –оат: например, метилпропионат – метиловый эфир пропановой кислоты.
Рассмотрим соединение, входящее в состав препаратов, применяемых для лечения заболеваний глаз: СН3 – С(СН3) = СН – СН2 – СН2 – С(СН3) = СН – СНО
Основная родоначальная структура – цепь из 8 атомов углерода, включающая альдегидную группу и обе двойные связи. Восемь атомов углерода – октан. Но есть 2 двойные связи – между вторым и третьим атомами и между шестым и седьмым. Одна двойная связь – окончание –ан надо заместить на –ен, двойных связей 2, значит на –диен, т.е. октадиен, а в начале указываем их положение, называя атомы с меньшими номерами – 2,6-октадиен. Но в соединении есть альдегидная группа, это не углеводород, а альдегид, поэтому добавляем суффикс –аль, без номера, он всегда первый – 2,6-октадиеналь. Ещё 2 заместителя – метильные радикалы у 3-го и 7-го атомов. Значит, в итоге получим: 3,7-диметил - 2,6-октадиеналь.
Н Н
+I- Эффектом характеризуются алкильные радикалы, -I эффектом– атомы галогенов, функциональные группы, содержащие кислород, азот, серу, кратные связи, а также группы, несущие положительный заряд.
Если в молекуле имеются системы сопряженных простых и кратных связей или атомы с неподеленными электронными парами, включенными в систему сопряжения, они могут участвовать в образовании общего p-электронного облака. Участие групп в сопряжении и влияние их на состояние p-электронного облака молекулы называют мезомерным эффектом (сдвиг электронной плотности сопряжённых p-связей) , или эффектом сопряжения (обычно обозначается заглавной буквой М; реже – заглавной буквой С). Для его обозначения используется изогнутая стрелка. У атомов азота, кислорода, фтора внешняя электронная оболочка заполнена, и они способны смещать p-электроны неподеленной электронной пары в сторону бензольного ядра или ненасыщенного углеродного атома:
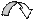 | |||
 |
СН3 - О - СН = Сd-Н2
Если в систему сопряжения входит кратная связь между разнородными атомами, то общее p-электронное облако смещается в сторону более электроотрицательного атома:
 Od-
Od-
СН2 = СН-Cd+
Н
Положительный мезомерный эффект проявляют группы: –ОН; –OR; –NH2; -NR2; –SH; галогены (смещение электронной плотности от гетероатома); отрицательный: группы -NO2, -CºN, -СООН, -SО3Н (смещение электронной плотности к гетероатому функциональной группы). Наличие индуктивного и мезомерного эффектов приводит к перераспределению электронной плотности в молекуле. В результате на одних атомах концентрируется частичный отрицательный, а на других – частичный положительный заряды. В свою очередь, это перераспределение зарядов определяет реакционную способность соединений, их кислотно-основные свойства, дипольный момент молекул, силу межмолекулярных связей (а значит и такие свойства как темперутуры кипения и плавления, растворимость).
ТЕМА 1. ВВЕДЕНИЕ. КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА И ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Введение. Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с познанием их биологических функций. Основными объектами ее изучения служат биологические полимеры (биополимеры) и биорегуляторы.
Биополимеры– высокомолекулярные природные соединения, являющиеся структурной основой всех живых организмов и играющие определенную роль в процессах жизнедеятельности. К биополимерам относят пептиды и белки, полисахариды (углеводы), нуклеиновые кислоты. В эту группу включают и липиды, которые сами по себе не являются высокомолекулярными соединениями, но в организме обычно связаны с другими биополимерами.
Биорегуляторы – соединения, которые химически регулируют обмен веществ. К ним относят витамины, гормоны, многие синтетические биологически активные соединения, в том числе лекарственные вещества.
Биоорганическая химия неразрывно связана с органической химией, базируется на её идеях и методах, т.к. большинство компонентов живой материи представлено органическими соединениями. Они могут синтезироваться в организме, поступать извне или модифицироваться в нем. Живой организм является «химическим производством», в каждой клетке его непрерывно протекают тысячи различных химических реакций, обеспечивающих существование и развитие организма.
Совокупность химических реакций, протекающих в организме, называют обменом веществ, или метаболизмом. Вещества, образующиеся в клетках, тканях и органах растений и животных в процессе метаболизма, называют метаболитами.
Метаболизмвключает два направления – катаболизм и анаболизм.
К катаболизму относят реакции распада веществ, попадающих в организм с пищей. Как правило, они сопровождаются окислением органических соединений и протекают с выделением энергии.
Анаболизм – синтез сложных молекул из более простых, в результате которого осуществляется образование и обновление структурных элементов живого организма.
Метаболические процессы протекают с участием ферментов, т. е. специфических белков, которые находятся в клетках организма и играют роль катализаторов биохимических процессов (биокатализаторы).
Метаболиты – естественные, присущие организму вещества. С другой стороны, существуют соединения, называемые антиметаболитами, т. е. являющиеся антагонистами естественных метаболитов. К ним относятся природные или синтетические биологически активные соединения, близкие по строению к метаболитам и вступающие с ними в конкуренцию в биохимических процессах. Антиметаболиты (в силу своего структурного сходства) способны вступать вместо метаболитов в биохимические реакции, которые с их участием будут заканчиваться иным результатом, чем с участием метаболитов.
Современная теория строения органических соединений создана выдающимся русским учёным А.М. Бутлеровым.
