Классификация комплексных соединений
1. По природе лигандов и центрального иона:
а) неорганические - 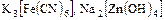 ;
;
б) органические - 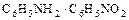 ;
;
в) смешанные - 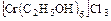 .
.
2. По заряду комплексного иона:
а) катионные - 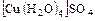 ;
;
б) анионные - 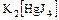 ;
;
в) нейтральные - 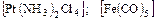 .
.
3. По аналогии с основными классами соединений:
а) комплексные кислоты - 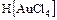 ;
;
б) основания - 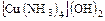 ;
;
в) соли - 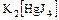 .
.
4. По природе лиганда:
а) гидроксокомплексы - 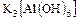 ;
;
б) аквакомплексы - 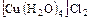 ;
;
в) аммиакаты - 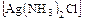 ;
;
г) ацидокомплексы (лигандами являются остатки кислот) - 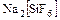 ,
, 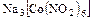 .
.
5. По внутренней структуре комплексных соединений:
а) моноядерные - 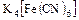 ;
;
б) полиядерные - 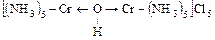
Реакции комплексообразования
1. Соли взаимодействуют с нейтральными молекулами
а) 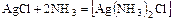 ;
;
б) 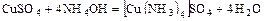 .
.
2. Из двух простых солей; центральным ионом является менее активный металл
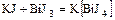 .
.
3. Реакции обмена между простой и комплексной солью
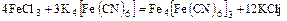 .
.
Химические свойства
1. Обменные реакции
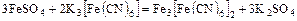 .
.
2. Реакции замещения одних лигандов на другие
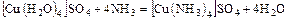 .
.
3. Окислительно-восстановительные реакции
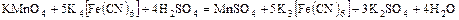
окислитель восстановитель
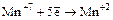 ,
,
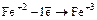 .
.
4. Диссоциация комплексных соединений может идти по нескольким ступеням; константы равновесия для каждой ступени считают по закону действующих масс.
I ступень – диссоциация молекулы, например
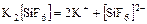
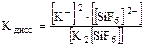 .
.
II ступень – распад комплексного иона. Этот процесс может идти поэтапно, когда лиганды отделяются по одному.
Краткая запись:
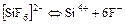 ,
,
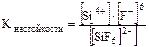 .
.
Кнестойкости характеризует устойчивость комплексного иона при растворении: чем больше константа нестойкости, тем менее устойчив комплексный ион.
Иногда используют обратную величину:
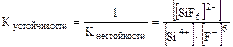 .
.
Номенклатура комплексных соединений
1. Молекулу называют слева направо в именительном падеже.
2. При названии комплексного иона вначале называют лиганды, а затем центральный ион.
3. Лиганды (если они разные) называют в алфавитном порядке с использованием греческих приставок (ди-, три-, тетра-, …).
4. а) Если лиганд – нейтральная молекула, то его называют без окончания
(H2O – «аква», NH3 – «аммин», СО – «карбонил», NO – «нитрозо»).
б) Если лиганд заряжен, то используют окончание «о»
(F - - «фторо», ОН - - «гидроксо», …).
5. При назывании центрального атома применяют: а)русское название элемента, если комплекс катионный; б) греческое или латинское название, если комплекс анионный.
6. При назывании по Штоку после названия центрального атома указывают его валентность, а в названии по Эвенсу-Бассету указывают заряд комплексного иона.
Пример:
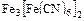 по Штоку: железо (II) гексацианоферрат (III);
по Штоку: железо (II) гексацианоферрат (III);
по Эвенсу-Бассету: железо (+2) гексацианоферрат (3-).
Природа сил комплексообразования
I. Метод валентных связей
За счёт свободных d – орбиталей центральный ион, как правило, будет акцептором электронных пар, а лиганды являются донорами. Орбитали центрального атома гибридизуются, причём на тип гибридизации влияет число лигандов и их электронная структура. Характер гибридизации определяет структуру комплексного иона.
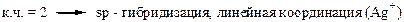
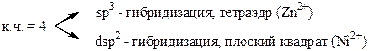
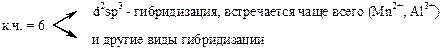
Иногда прочность связи усиливается благодаря появлению дативных связей (обратны донорно-акцепторным).
Пример:
Комплексное соединение содержит центральный ион 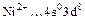 и лиганды
и лиганды 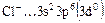 ;
; 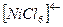 :
:
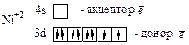
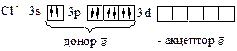
Таким образом, между 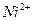 и
и 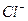 действуют связи:
действуют связи:
а) донорно-акцепторные;
б) дативные;
в) электростатические.
