Металлическая связь. Зонная теория кристаллов
Металлическая связь - это особый вид химической связи, реализующейся в металлах, сплавах, в соединениях металлов друг с другом (интерметаллидах). Основной особенностью металлической связи является ее электронодефицитность: взаимодействие осуществляется с использованием значительно меньшего числа валентных электронов, чем это необходимо для образования двухцентровых связей. Так, например, в кристалле натрия каждый атом имеет в ближайшем окружении восемь таких же атомов, в то время как единственный валентный электрон позволяет ему образовать лишь одну двухцентровую связь. Совершенно очевидно, что существование кристалла натрия возможно лишь за счет образования делокализованных связей, охватывающих все атомы кристалла.
Таким образом, металлическая связь - это многоцентровая связь, объединяющая большое число атомов за счет обобществления валентных электронов в пределах всего кристалла.
Характерными особенностями металлической связи являются ее ненаправленность и ненасыщаемость. Вследствие этого веществам с металлической связью присущ ряд общих свойств. Кристаллы таких веществ обладают высокой электропроводность и теплопроводностью. Веществам с металлической связью присущи пластичность (ковкость) и характерный металлический блеск.
Заметим, что наряду с металлической связью в кристалле металла могут проявляться и иные виды взаимодействия, вплоть до образования локализованных связей. Так, в кристалле ниобия, атомы которого имеют пять валентных электронов, лишь около 25 % от их числа идет на образование металлической связи.
Наиболее удовлетворительно металлическую связь описывает зонная теория кристаллов, представляющая собой распространение метода молекулярных орбиталей на системы с переменным и очень большим числом атомов (порядка числа Авогадро).
В основе зонной теории кристаллов лежит представление об энергетических зонах. Познакомимся с этим понятием на примере формирования кристалла щелочного металла, например, натрия. В изолированном атоме натрия электроны находятся на дискретных энергетических уровнях в соответствии с электронной конфигурацией 1s22s22p63s1. При сближении двух атомов натрия из двух 3s-орбиталей образуются связывающая ss и разрыхляющая ss* молекулярные орбитали (рис. 13).
Валентные электроны заполняют ss орбиталь, результатом чего является образование молекулы Na2. Взаимодействие трех атомов натрия приводит к образованию трех МО - связывающей, разрыхляющей и несвязывающей. Агрегату Na4 будет соответствовать формирование четырех МО (двух связывающей и двух разрыхляющих). По мере увеличения числа атомов в агрегате число молекулярных орбиталей будет расти, а отвечающие им энергетические уровни будут сближаться. При достаточно большом числе атомов (порядка числа Авогадро) формируется совокупность огромного числа энергетических уровней, в которой энергии двух соседних уровней отличаются на очень малую величину (порядка 10-20 - 10-22 кДж/моль). Подобные совокупности энергетических уровней называются энергетическими зонами.
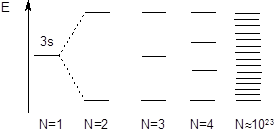
Рис. 13. Формирование 3s-зоны в кристалле натрия.
Энергетические зоны подчиняются законам квантово-механической теории. Так, для энергетических зон справедлив принцип Паули: если кристалл состоит из N атомов, емкость s-зоны составляет 2N электронов, р-зоны - 6N электронов и т.д. Соблюдается также правило Хунда: если в зоне имеются вырожденные уровни, электроны распределяются таким образом, чтобы число параллельных спинов было максимальным. Зона, в которой располагаются валентные электроны, называется валентной зоной; ближайшая к валентной вакантная зона называется зоной проводимости.
Энергетические зоны распространяются на все атомы кристалла, в результате чего любой электрон, участвующий в образовании металлической связи, принадлежит всем атомам, что обеспечивает свободное перемещение электрона по кристаллу.
В кристалле металла возможно перекрывание энергетических зон, образованных орбиталями разных энергетических подуровней. Зоны являются перекрывающимися, если верхний край нижней валентной зоны выше нижнего края зоны проводимости. Если зоны не перекрываются, то энергетический зазор между нижним краем зоны проводимости и верхним краем валентной зоны называется запрещенной зоной.
Зонная теория объясняет характерные свойства металлов. Так, высокая электрическая проводимость типичных металлов связана со свободным перемещением электронов в пределах кристалла. Очевидно, что металлическая проводимость проявляется в двух случаях:
1. Если валентная зона укомплектована электронами не полностью.
2. Если валентная зона и зона проводимости перекрываются. В этом случае валентные электроны заполняют энергетические уровни не только валентной зоны, но и зоны проводимости.
Если заполненная электронами валентная зона отделена от зоны проводимости запрещенной зоной, то свойства кристалла будут определяться шириной запрещенной зоны. Если ширина запрещенной зоны (DЕ) больше 400 кДж/моль, то кристалл не будет проводить электрический ток. Такие вещества называются диэлектриками. Примером диэлектрика может служить алмаз, для которого DЕ = 580 кДж/моль, а удельное сопротивление r составляет 1×106 Ом×см-1. При ширине запрещенной зоны, укладывающейся в интервал 10 - 400 кДж/моль, часть электронов, обладающих достаточной энергией, переходит в зону проводимости; такие вещества называются полупроводниками. Так, для кристаллического кремния DЕ = 105 кДж/моль, а r = 6×104 Ом×см-1 при комнатной температуре.
Понижение температуры по-разному влияет на проводимость металлических проводников и полупроводников: для первых проводимость с повышением температуры понижается, для вторых - повышается. Это явление также может быть объяснено в рамках зонной теории. В случае металлических проводников с повышением температуры электроны, поглощая тепловую энергию, перемещаются с низких уровней на вакантные уровни той же зоны или зоны проводимости. В результате уменьшается число незанятых уровней с относительно низкой энергией и, следовательно, проводимость кристалла. В случае полупроводника с повышением температуры возрастает доля электронов, способных преодолеть запрещенную зону, и проводимость кристалла увеличивается.
В результате обобществления электронов и свободного перемещения их в пределах всего кристалла в узлах кристаллической решетки металла находятся частицы, имеющие одноименный (положительный) эффективный заряд. В связи с этим слои атомов металла относительно легко смещаются друг относительно друга, Этим объясняется типичная для металлов пластичность.
