Лабораторная работа: «Влияние различных факторов на растворимость веществ в воде. Свойства растворов электролитов».
Влияние температуры на растворимость солей.
Налить в пробирку 2 мл воды. Шпателем добавить сухой карбонат натрия (~2 г) для получения насыщенного раствора. Нагреть пробирку. Слить прозрачный горячий раствор в пустую пробирку, и охладить под струей водопроводной воды. Записать явления, наблюдаемые при проведении опыта. Сделать вывод о влиянии температуры на растворимость твёрдых веществ.
Тепловые эффекты, вызываемые растворением электролитов.
Наблюдать тепловые явления, происходящие при приготовлении 30% растворов следующих электролитов: гидроксида натрия, роданида калия, хлорида натрия. Для этого в 3 стакана, содержащие по 3 г вещества добавить 7 мл воды. Наблюдать за изменением температуры в ходе растворения. Записать явления, наблюдаемые при проведении опыта. Сделать выводы.
Осаждение труднорастворимых солей.
Налить в две пробирки по 3 мл растворов бария хлорида и натрия хлорида. В 1-ю пробирку добавить 2 мл насыщенного раствора сульфата натрия, во 2-ю пробирку добавить 2 мл насыщенного раствора сульфата меди.
Записать явления, наблюдаемые при проведении опыта. Написать молекулярное, ионное и сокращенное ионное уравнения данных реакций.
Сделать выводы.
4. Измерение удельной электропроводности растворов электролитов в μСм/см (микроСименс/сантиметр). Результаты занести в таблицу:
| № | Электролит | Концентрация раствора, С (моль/л) | Константа диссоциации, К | Удельная электропроводность, χ (μСм/см) | Относительная сила электролита (сильный, слабый) |
| 1. | H2O (дист) | 1,8´10-16 | |||
| 2. | CH3COOH | 0,001 | 1,8´10-5 | ||
| 3. | NH4OH | 0,001 | 1,8´10-5 | ||
| 4. | HCl | 0,001 | 1,0´107 | ||
| 5. | NaOH | 0,001 | |||
| 6. | NaCl | 0,001 | |||
| 7. | BaSO4 | 0,001 | ПР = 6,3´10-13 |
Написать уравнения диссоциации для всех используемых электролитов и математические выражения констант диссоциации слабых электролитов.
Занятие № 7 Тема: «Кислотно-основное равновесие в организме. Водородный показатель
Биологических жидкостей».
1. Вопросы для обсуждения:
1. Диссоциация воды. Ионное произведение воды.
2. Водородный показатель. Шкала рН. рН биологических жидкостей. Ацидоз, алкалоз.
3. Теория кислот и оснований Аррениуса, Бренстеда-Лоури, Льюиса.
4. Типы протолитических реакций: нейтрализации, гидролиза, ионизации.
5. Гидролиз солей, типы гидролиза. Степень и константа гидролиза. Факторы, влияющие на степень гидролиза.
6. Роль гидролиза в биохимических процессах.
7. Буферные растворы. Классификация и химический состав.
8. Механизм буферного действия (гидрокарбонатного, фосфатного, ацетатного, аммиачного).
9. Расчёт pH буферных растворов. Уравнения Гендерсона–Хассельбаха для кислотного и щелочного буферных растворов.
10. Буферная ёмкость. Определение. Формулы для расчёта. Факторы, влияющие на буферную ёмкость.
11. Буферные системы крови. Понятие о кислотно-основном равновесии.
2. Ситуационные задачи:
Задача №1. Рассчитать pH и pOH раствора СН3СООН, С = 0,1 моль/л, если a = 0,012.
Решение:СН3СООН « СН3СОО- + H+
[H+] = C · a = 0,1 · 0,012 = 0,0012 = 1,2·10-3 M
pH = -log[H+]= -log 1,2·10-3 = 2,92
pОH = 14 - pH = 14 – 2,92 = 11,08
Задача №2.К 100 мл крови добавили 20 мл раствора NaOH (С = 0,1моль/л), при этом значение pH изменилось от 7,36 до 8,34. Рассчитать буферную ёмкость крови по щелочи
Решение:
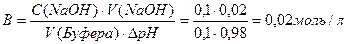
Задача №3. Рассчитать pH буферной смеси, приготовленной из 50 мл раствора NaH2PO4 (С = 0,2М) и 100 мл раствора Na2HPO4 (С = 0,1моль/л). Как изменится pH этого раствора после разбавления в 10 раз?
Решение: 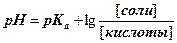 ; pKa (H2PO4-) = 7,2;
; pKa (H2PO4-) = 7,2; 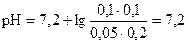 ;
;
После разбавления водой pH не изменится.
3. Выполнить тестовые задания (письменно):
| Константа диссоциации воды (моль/л) при температуре 25оС равна: | ||
| А | 1,8·10-18 | |
| Б | 1,8·10-14 | |
| В | 1,8·10-16 | |
| Г | 1,8·10-5 | |
| В каком пределе лежит значение [H+] в кислой среде? | ||
| А | [H+] > 10-7 | |
| Б | [H+] < 10-7 | |
| В | [H+] = 10-7 | |
| Водородный показатель плазмы крови в норме может колебаться в пределах: | ||
| А | 0,9 – 1,5 | |
| Б | 6,8 – 7,0 | |
| В | 8,5 – 9,5 | |
| Г | 7,36 – 7,4 | |
| Водородный показатель желудочного сока в норме может колебаться в пределах: | ||
| А | 0,9 – 1,5 | |
| Б | 6,8 – 7,0 | |
| В | 8,5 – 9,5 | |
| Г | 7,36 – 7,4 | |
| Молярная концентрация ионов [H+] желудочного сока равняется 10-1 моль/л. Чему равняется рОН. | ||
| А | ||
| Б | ||
| В | ||
| Г | ||
| Физиологическое значение рН мочи: | ||
| А | 1 - 3 | |
| Б | 3 - 6 | |
| В | 5 - 8 | |
| Г | 6 - 9 | |
| Алкалоз – это отклонение рН крови до: | ||
| А | 6,5 | |
| Б | 6,8 | |
| В | 7,7 | |
| Г | 7,1 | |
| Какая из солей гидролизуется в большей степени? K HCN = 7´10-10 K H2SO3 = 6´10-8 K HF = 1´10-4 | ||
| А | NaCN | |
| Б | Na2SO3 | |
| В | NaF | |
| Какая из приведённых солей подвергается гидролизу и обуславливает кислую реакцию среды: | ||
| А | NaCl | |
| Б | CH3COONH4 | |
| В | KCN | |
| Г | NH4Cl | |
| Какое значение рН имеет раствор при гидролизе соли, образованной слабой кислотой и сильным основанием: | ||
| А | рН < 7 | |
| Б | рН > 7 | |
| В | рН = 7 | |
| Определить реакцию среды при гидролизе соли, образованной слабым основанием и слабой кислотой, если Кд кислоты < Кд основания | ||
| А | Кислая | |
| Б | Щелочная | |
| В | Нейтральная | |
| Для коррекции кислотно-щелочного равновесия при ацидозе рекомендован раствор: | ||
| А | NaHCO3 | |
| Б | HCl | |
| В | NaCl | |
| Г | NaOH | |
| С целью предотвращения гидролиза, лекарственные препараты хранят: | ||
| А | В виде концентрированных растворов, при низкой температуре | |
| Б | В виде концентрированных растворов, при высокой температуре | |
| В | В виде разбавленных растворов, при низкой температуре | |
| Г | В виде разбавленных растворов, при высокой температуре | |
| Из предлагаемых веществ выбрать возможные компоненты для приготовления буферных растворов: | ||
| А | HCl, NaCl | |
| Б | NaOH, NaHCO3 | |
| В | NaH2PO4, Na2HPO4 | |
| Г | NaHCO3, CO2·H2O | |
| Из приведенных пар веществ выберите компоненты ацетатного буферного раствора | ||
| А | CH3COONH4, CH3COOH | |
| Б | (CH3COO)2Mg, CH3COOH | |
| В | CH3COONa, CH3COOH | |
| Г | (CH3COO)2Zn, CH3COOH | |
| рН основного буферного раствора можно рассчитать по формуле | ||
| А | 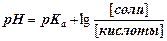 | |
| Б | 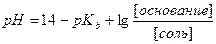 | |
| В | 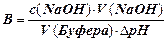 | |
| Г | pОH = -lg[ОН-] | |
| Единицы измерения буферной емкости: | ||
| А | Моль/л | |
| Б | % | |
| В | г/л | |
| Г | Моль/кг | |
| Максимальное значение буферной емкости при: | ||
| А | рН = рК | |
| Б | рН < рК | |
| В | рН > рК | |
| Г | рН = рК + 1 |
3. Задачи для самостоятельного решения (выполнить письменно):
1. Рассчитать pH растворов, в которых концентрация ионов H+ равна 8,1∙10-3 моль/л (см.таблицу десятичных логарифмов стр. 91):
2. Рассчитать pH растворов, в которых концентрация ионов OH- равна 4∙10-4 моль/л:
3. Как надо изменить концентрацию ионов Н+ в растворе, чтобы pH раствора увеличился на 1:
а) увеличить в 10 раз; б) увеличить на 1 моль/л; в) уменьшить в 10 раз
4. Рассчитать pH раствора HCl, С = 0,025 моль/л, если α = 0,96.
5. Рассчитать pH раствора NH4OH, С = 0,02 моль/л, если α = 0,013.
6. Изобразить схемы гидролиза (в молекулярном, ионном и сокращенном ионном виде) следующих солей, указать характер среды в растворе:
а) KCN
б) NH4Br
в) Na2SO4
7. Рассчитать pH гидрокарбонатного буферного раствора, состоящего из 16 мл раствора NaHСO3,
С = 0,1 моль/л и 40 мл раствора H2СO3, С = 0,04 моль/л. (pKa = 6,35).
8. Рассчитать рН аммиачного буферного раствора, приготовленного при смешивании 100 мл
раствора NН 4CI, С (NH4CI) = 0,2 моль/л и 200 мл раствора NН4OH, С (NH4ОН) = 0,1 моль/л
(pKb(NH4ОН) = 4,75).
9. К 100 мл крови добавили 14 мл раствора HCl, С = 0,1 моль/л, при этом значение pH изменится от 7,36 до 7,21. Рассчитать буферную ёмкость крови по кислоте.
4.Тематика рефератов по учебно-исследовательской работе студентов (УИРС):
| 1. | Роль гидролиза в процессах жизнедеятельности. |
| 2. | Буферные системы в организме человека. |
| 3. | Кислотно-щелочное равновесие крови. |
| 4. | Нарушения кислотно-основного состояния: ацидоз и алкалоз. |
