Факторы, влияющие на скорость химической реакции
Лекция № 2
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ
План лекции:
1. Введение
2. Основы химической кинетики. Факторы, влияющие на скорость химической реакции
3. Механизмы протекания химических реакций
4. Фотосинтез
5. Зрение
6. Ферментативный катализ
Цели изучения:познание кинетических закономерностей, определяющих протекание химических и биохимических процессов, изучение влияния различных факторов на скорость реакций.
Введение
Математический аппарат химической термодинамики позволяет определять тепловые эффекты химических реакций и прогнозировать направление протекания процессов, но при этом важнейшая для практики величина время, за которое протекает процесс, не рассматривается в рамках классической термодинамики.
Раздел химии, изучающий скорости и механизмы химических процессов, называется химической кинетикой.
Знание законов химической кинетики необходимо врачу, чтобы:
1) глубже понимать суть процессов, протекающих в организме;
2) определять оптимальные промежутки времени между приемами лекарственного средства;
3) оценивать остаточное количество токсиканта в организме.
2. Основы химической кинетики
Б. Зависимость скорости реакции от температуры.
При повышении температуры скорость реакции, как правило, увеличивается. Эта закономерность может быть выражена уравнением:
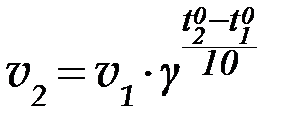 | (5) |
где 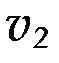 и
и 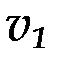 - скорости реакций при температурах
- скорости реакций при температурах 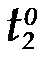 и
и 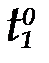 ;
;
γ - температурный коэффициент скорости реакции (температурный коэффициент Вант-Гоффа), который показывает во сколько раз возрастает скорость данной реакции при повышении температуры на 100.
Для большинства реакций g = 2-4. В таких случаях выполняется правило Вант-Гоффа:
При повышении температуры на каждые 100 скорость химической реакции возрастает в 2-4 раза.
Для ферментативных процессов, протекающих в биосистемах, g больше 4 (обычно около 7).
Основное влияние температура оказывает на константу скорости реакции. Эта зависимость выражается уравнением Аррениуса:
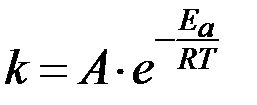 , , | (6) |
где: k – константа скорости реакции;
А – частотный фактор, отражающий число столкновений между реагирующими молекулами в единице объема в единицу времени;
R – универсальная газовая постоянная (8,31 Дж×моль-1×К-1);
T – температура по Кельвину (273 + t0С);
Ea – энергия активации, кДж/моль.
В. Энергия активации
Важным понятием в химической кинетике является энергия активации:
Энергия активации представляет тот избыток энергии, которым должны обладать молекулы взаимодействующих веществ по отношению к средней энергии молекул.
Химическое взаимодействие, как правило, начинается с разрыва или ослабления связи между атомами в молекулах реагирующих веществ. Этот процесс осуществляется путем столкновения молекул. Однако далеко не все столкновения заканчиваются химической реакцией. Так, в реакции разложения йодоводорода, протекающей при комнатной температуре, эффективным (т.е., приводящим к химической реакции) является лишь одно столкновение из 2×1017 столкновений молекул.
Такое соотношение между числом эффективных столкновений и общим числом столкновений объясняется тем, что в ходе взаимодействия частиц образуется неустойчивое промежуточное состояние, которое называется активированным комплексом. Для создания активированного комплекса молекулам необходимо преодолеть силы межъядерного отталкивания. Для преодоления этих сил молекулам требуется дополнительная энергия, т.е., энергия активации. Неустойчивый активированный комплекс существует очень короткое время и распадается с образованием продуктов реакции и выделением энергии.
Энергия активации зависит от природы реагирующих веществ и в некоторой степени от температуры.
Если энергия активации мала (меньше 40 кДж/моль), скорость реакции велика. Так, ионные реакции в растворах протекают практически мгновенно.
Если энергия активации реакции велика (больше 120 кДж/моль), скорость реакции мала. Например, синтез йодоводорода из I2 и H2 (Еа = 163 кДж/моль) при обычных условиях протекает за астрономический промежуток времени.
Реакции, энергия активации которых находится в пределах от 40 до 120 кДж/моль, протекают за время, которое можно зафиксировать в лабораторных условиях. Так, время протекания реакции разложения тиосульфата натрия серной кислотой, Еа = 86,5 кДж/моль:
Na2S2O3 + H2SO4 = Na2SO4 + S + SO2 + H2O
составляет несколько минут.
Соотношение констант скоростей при разных температурах определяется уравнением:
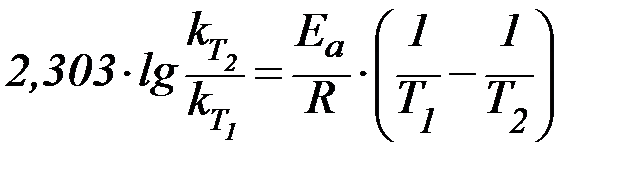 , , | (7) |
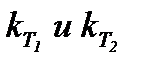 где – константы скорости реакции при температурах T1 и T2;
где – константы скорости реакции при температурах T1 и T2;
R – универсальная газовая постоянная, равная 8,31×10-3 кДж/моль×К;
Ea – энергия активации данной реакции в кДж/моль.
Данное уравнение позволяет рассчитать энергию активации системы.
Пример.
Для прямой элементарной реакции I2 + H2 = 2HI опытным путем определены константы скорости: при 443°С – 0,0067; при 508°С – 0,1059. Определить энергию активации данной реакции.
| T1 = 443 + 273 = 716 K | T2 = 508 + 273 = 781 K |
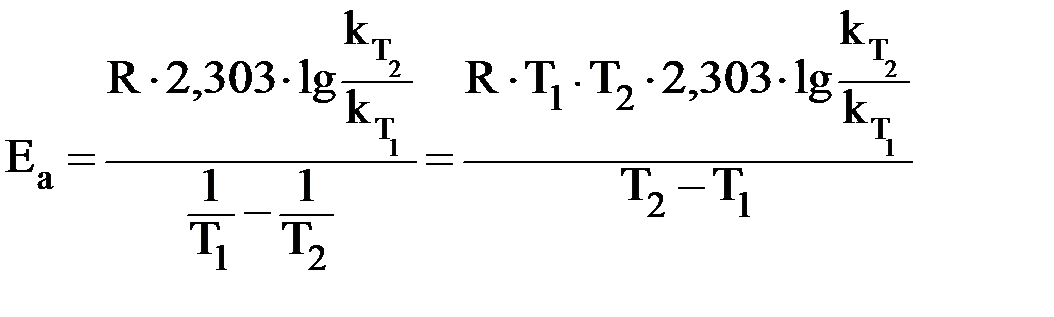
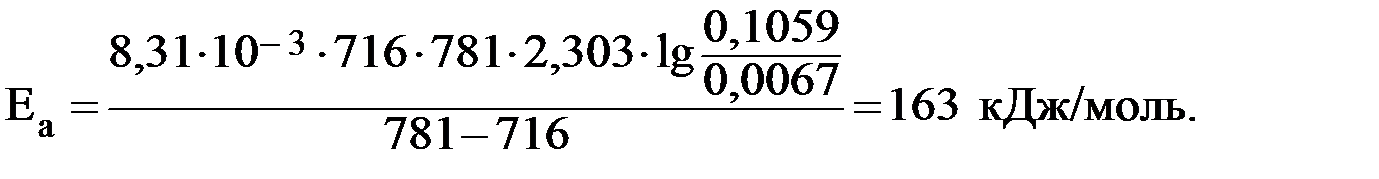
Вывод: скорость реакции очень мала, так как Еа > 120 кДж/моль.
Д. Реакции I порядка
Для реакций I порядка убыль концентрации реагента определяется уравнением:
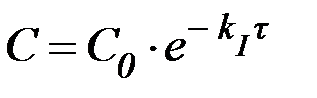 | (8) |
где С – концентрация вещества в данный момент времени;
С0 – начальная концентрация вещества;
kI – константа скорости реакции первого порядка;
t – время.
В логарифмической форме это выражение выглядит так:
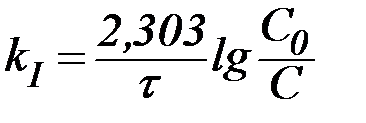 | (9) |
Из приведенных формул можно сделать ряд важных заключений:
1) константа скорости реакции первого порядка имеет размерность [время-1] и может быть выражена в обратных секундах, минутах, часах и т. д.;
2) величина kI не зависит от способа выражения концентрации реагента;
3) в реакциях первого порядка одинаковым промежуткам времени отвечают одинаковые доли прореагировавшего вещества.
Последнее утверждение позволяет ввести понятие период полупревращения.
Периодом полупревращения (t1/2) называют время, необходимое для превращения половины первоначального количества вещества.
Таким образом, в момент времени t = t1/2 количество непрореагировавшего вещества составляет 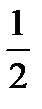 С0. В этом случае:
С0. В этом случае:
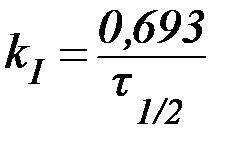 . . | (10) |
Из данной формулы следует, что в реакциях первого порядка период полупревращения не зависит от начальной концентрации реагента.
В некоторых случаях удобно использовать формулу:
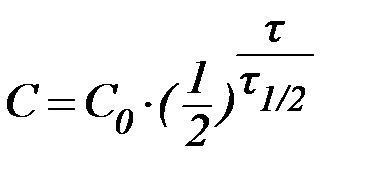 , , | (11) |
которая позволяет определить время, за которое превращению подвергнется определенное количество исходного вещества.
В организме человека процессы метаболизма лекарственных препаратов протекают, в основном, в соответствии с уравнением реакции первого порядка. Период, за который превращению подвергается половина действующего начала препарата называется периодом полувыведения или полуэлиминации. Зная величины kI и t1/2, можно рассчитать оптимальные промежутки времени между приемами лекарственного средства.
Кинетические уравнения реакций различного порядка представлены в табл. 2.
Табл. 2. Кинетические уравнения реакций различного порядка.
| Порядок реакции | Кинетическое уравнение | Решение кинетического уравнения* | Период полупревращения |
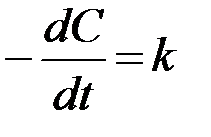 | 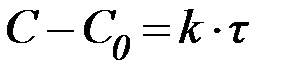 | 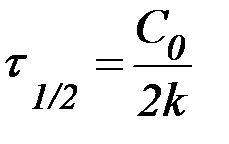 | |
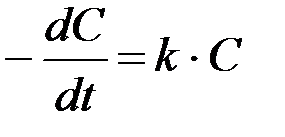 | 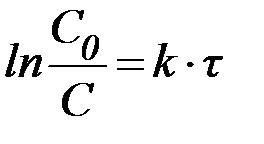 | 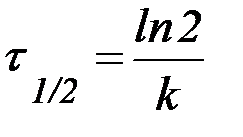 | |
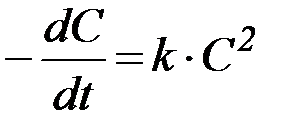 | 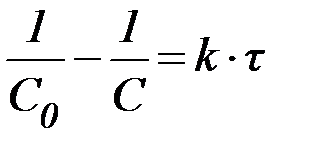 | 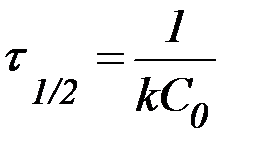 | |
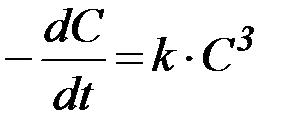 | 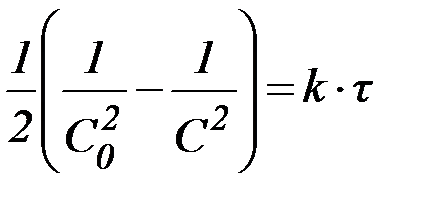 | 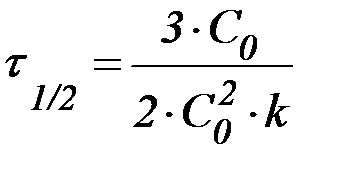 |
* при равных исходных концентрациях реагирующих веществ
Из приведенных уравнений следует, что для реакций различного порядка константы скорости имеют неодинаковые размерности. Действительно, константа скорости реакции второго порядка имеет размерность [л·моль-1·время-1)], третьего порядка - [л2·моль-2·время-1].
Таким образом, сравнивать значения констант скорости реакций различного порядка нельзя.
Фотосинтез
Фотосинтез - наиболее важный фотобиологический процесс, так как с его помощью растения и некоторые другие организмы сохраняют энергию солнечного света. Фотосинтез состоит из множества весьма сложных реакций, однако суммарный его результат выражается следующей простой реакцией:
6CO2 + 6H2O C6H12O6 + 6O2 DG0 = 2861,9 кДж/моль.
Более общая схема суммарного фотосинтетического процесса записывается следующим образом:
2H2D + CO2 CH2O + H2O + 2D,
где D – элемент, окисляющийся в ходе фотосинтеза.
Как видно из изменения стандартной энергии Гиббса, фотосинтез относится к эндэргоническим реакциям. Эти реакции могут осуществляться только за счет поступающей извне энергии света.
8. Зрение
Зрение включает в себя поглощение энергии излучения и превращение ее в нервный импульс. Видимый свет поглощается хромофором глаза, которым служит альдегидпроизводное витамина А-ретиналь. В сетчатке глаза находится около 100 млн. специализированных клеток, так называемых палочек, и 5 млн. других клеток, называемых колбочками. Между этими клетками и нервными волокнами, соединяющими их с мозгом, находятся соединительные участки, называемые синапсами.
Установлено, что в зрительном процессе поглощение энергии света не приводит ни к каким химическим реакциям, а сводится лишь к изомеризации 11-цис-ретиналя в транс-ретиналь. Ретиналь связывается с белком, называемым опсином. Опсин образует комплексы с хромофорами, формируя родопсин и йодопсин. Родопсин действует в условиях низкой интенсивности света, например, ночью. Он не различает цвета, так как содержит только один пигмент. Цветное зрение человека обусловлено йодопсином.
Ферментативный катализ
Катализаторомназывается вещество, которое ускоряет реакцию, но само в ходе реакции не расходуется. Хотя механизмы каталитических реакций могут сильно различаться, но общим является то, что в присутствии катализатора понижается энергия активации, т. е. в присутствии катализатора процесс идет по другому пути, отличающемуся от пути реакции в отсутствие катализатора.
Реакции, катализируемые ферментами, обычно характеризуются очень сильным ускорением (104 – 105 раз) и высокой специфичностью. Под специфичностью здесь понимают способность ферментов ускорять реакцию только между определенными веществами, называемыми субстратами.
Ферменты бывают двух типов: простые – это белковые молекулы, содержащие один /трипсин/ или несколько /уреаза-4/ активных центров; и сложные, состоящие из белка и небелкового компонента (витамины, атомы металлов, нуклеотиды и др.). Активные центры имеют жесткую структуру, на их поверхности и происходит превращение субстратов.
Ферментативный процесс можно представить следующим образом:

где E, S – фермент и субстрат;
P – продукт реакции;
ES – фермент-субстратный комплекс. 
Скорость ферментативного процесса можно рассчитать по уравнению Михаэлиса-Ментен:
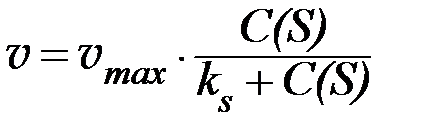 , , | (12) |
где С(S) – концентрация субстрата;
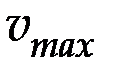 – максимальная скорость реакции, т. е. скорость, когда весь фермент находится в составе фермент-субстратного комплекса.
– максимальная скорость реакции, т. е. скорость, когда весь фермент находится в составе фермент-субстратного комплекса.
Из уравнения Михаэлиса-Ментен можно сделать следующие заключения:
а) при большой концентрации субстрата скорость реакции будет практически равна максимальной скорости, т. е. 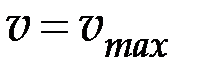 ;
;
б) при малой концентрации субстрата скорость реакции будет прямо пропорциональна его концентрации, т. е.:
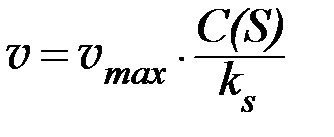
Уравнение Михаэлиса-Ментен довольно точно описывает только начальный период ферментативного процесса, так как в нем не учитывается влияние и взаимодействие с ферментом продуктов реакции.
Лекция № 2
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ
План лекции:
1. Введение
2. Основы химической кинетики. Факторы, влияющие на скорость химической реакции
3. Механизмы протекания химических реакций
4. Фотосинтез
5. Зрение
6. Ферментативный катализ
Цели изучения:познание кинетических закономерностей, определяющих протекание химических и биохимических процессов, изучение влияния различных факторов на скорость реакций.
Введение
Математический аппарат химической термодинамики позволяет определять тепловые эффекты химических реакций и прогнозировать направление протекания процессов, но при этом важнейшая для практики величина время, за которое протекает процесс, не рассматривается в рамках классической термодинамики.
Раздел химии, изучающий скорости и механизмы химических процессов, называется химической кинетикой.
Знание законов химической кинетики необходимо врачу, чтобы:
1) глубже понимать суть процессов, протекающих в организме;
2) определять оптимальные промежутки времени между приемами лекарственного средства;
3) оценивать остаточное количество токсиканта в организме.
2. Основы химической кинетики
Факторы, влияющие на скорость химической реакции
Основная величина в химической кинетике - скорость реакции. В общем случае, скорость химической реакции / 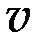 /определяется изменением количества реагирующего вещества в единицу времени:
/определяется изменением количества реагирующего вещества в единицу времени:
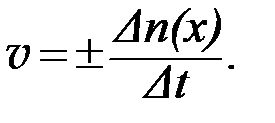 | (1) |
Для гомогенной (однородной) системы средняя скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образующихся в результате реакции за единицу времени в единице объема системы. Иными словами, в данном случае скорость реакции определяется изменением концентраций реагирующих веществ в единицу времени:
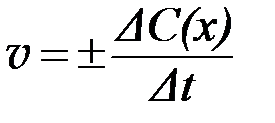 | (2) |
Истинная скорость гомогенной реакции, т.е., скорость реакции в данный момент времени, рассчитывается по уравнению:
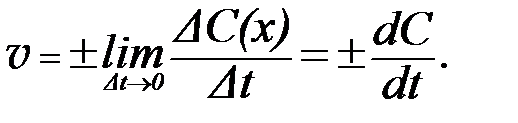 | (3) |
Концентрации реагирующих веществ принято выражать в моль/л, а время – в секундах, минутах или часах. Если время измерять в секундах, то размерность скорости гомогенной реакции: [моль∙л-1∙с-1].
Для гетерогенной (неоднородной) системы скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образующихся в результате реакции за единицу времени на единице поверхности раздела фаз:
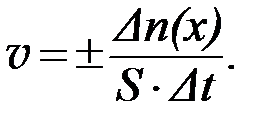 | (4) |
Размерность скорости гетерогенной реакции: [моль∙м–2∙с–1].
Скорость химической реакции зависит от природы реагирующих веществ, их концентрации, температуры и наличия катализатора. В некоторых случаях на скорость реакции оказывают влияние давление (если реакция протекает в газовой фазе), природа растворителя (если реакция протекает в растворе) и вид излучения (солнечная энергия, радиоактивное излучение). Скорость гетерогенных реакций зависит также от площади поверхности соприкосновения реагирующих веществ.
