Правила работы на фотоэлектроколориметре КФК-3
Фотоэлектроколориметр КФК-3 (рис. 1) предназначен для измерения коэффициентов пропускания (оптической проницаемости) или оптической плотности цветных растворов с целью определения по калибровочному графику концентрации вещества в растворах.
Спектральный диапазон работы КФК-3 от 315 до 990 нм.
Принцип действия фотоэлектроколориметра основан на сравнении светового потока, прошедшего через бесцветный растворитель (Фo), и светового потока, прошедшего через окрашенный раствор (Ф).
Световые потоки Фo и Ф фотоприемника преобразуются в электрические сигналы, которые обрабатываются микроЭВМ прибора и высвечиваются на цифровом табло в виде оптической проницаемости (П, %).
 |
 | |||||||||
 | |||||||||
 | |||||||||
 | |||||||||
| | |||||||||
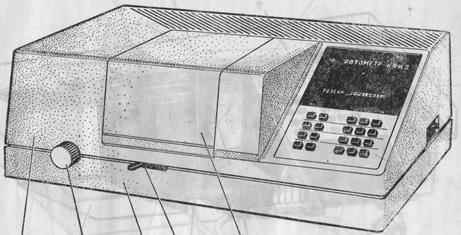
Рис. 1. Вид фотоэлектроколориметра:
1 – тумблер (сеть), 2 – ручка для установления длины волны, 3 – кюветное отделение с кюветодержателем, 4 – рукоятка для ввода светового пучка, 5 – микропроцессор системы, 6 – блок системы
При прохождении света через раствор свет или его компоненты поглощаются или отражаются. По величине поглощения или отражения лучей судят о природе и концентрации вещества.
В соответствии с законом Бугера-Ламберта-Бера зависимость изменения интенсивности потока света, прошедшего через раствор, от концентрации окрашенного вещества в растворе (С), выражается уравнением
lg(Io/I) = e × l× C, (2)
где Io и I – интенсивность потока света, падающего на раствор(Io) и прошедшего через раствор(I); e – коэффициент поглощения света, зависящий от природы растворенного вещества, называемый молярным коэффициентом поглощения; l – толщина слоя светопоглощающего раствора.
Измерив изменение интенсивности потока света, можно определить концентрацию анализируемого вещества. Определение проводят на фотоколориметре.
Таким образом, основным показателем для определения концентрации цветных растворов является оптическая плотность раствора (d) или противоположная ей величина – оптическая проницаемость раствора (П), она выражается в % и для оптически прозрачных растворов равна 100 %.
Порядок работы
Присоединить фотоэлектроколориметр (рис. 1) к сети 220 В и включить тумблер 1 СЕТЬ (с правой стороны фотоэлектроколориметра).
Нажать клавишу ПУСК на микропроцессорном блоке 5. На цифровом табло вверху появится значение длины волны. Ниже слева символ «Г» (оптическая плотность), справа – соответствующее ему значение.
Открыть крышку кюветного отделения и установить кювету с растворителем в дальнее гнездо кюветодержателя, а кювету с исследуемым раствором в ближнее гнездо кюветодержателя. Закрыть крышку кюветного отделения.
Установить ручкой (на передней панели слева внизу) длину волны (l), на которой проводится измерение (длина волны высвечивается на верхнем цифровом табло). Устанавливаемая длина волны зависит от цвета раствора.
В световой пучок установить кювету с растворителем, рукоятка перемещения кювет передвигается в крайнее левое положение (она находится на передней панели в центре внизу) (4, рис.1). Нажать клавишу «Г», а затем клавишу «П» (оптическая проницаемость). На нижнем цифровом табло высветится символ «П» и правее значение 100.0±0.2, означающие, что начальный отсчет светопропускания установился на фотометре правильно.
Затем рукоятку перемещения кювет установить вправо до упора, при этом в световой пучок вводится кювета с исследуемым раствором и на световом табло справа появляется значение оптической проницаемости (П, %) исследуемого раствора.
При построении калибровочного графика и определении концентрации растворов необходимо проводить измерения по методике, указанной выше, для каждого раствора в отдельности.
Опыт 1. Определение скорости химической реакции
Необходимо определить скорость реакции взаимодействия тиосульфата натрия (Na2 S2О3) с серной кислотой (Н2 SO4)
Na2 S2О3 + Н2 SO4 ® Na2 SO4 + Н2O+ SO2 + S ¯ .
В результате реакции выделяется сера в свободном виде, плотность раствора при этом меняется, что фиксируется по изменению оптической проницаемости раствора (до 3 %).
Группы студентов в количестве 2…3 человек получают от преподавателя раствор тиосульфата натрия определенной концентрации, наливают 2 мл этого раствора в кювету и добавляют в неё 2 мл раствора серной кислоты. Отмечают время начала реакции по секундомеру и следят за изменением значений проницаемости (П) или оптической плотности (d) на световом табло. Время протекания реакции записывают в табл. 1.
Таблица 1
Время протекания реакции и скорость химического процесса
при определенной концентрации тиосульфата натрия
| Концентрация раствора Na2 Ѕ2О3 С, моль/л | Время протекания реакции t, с | Скорость химической реакции v, моль/л×с |
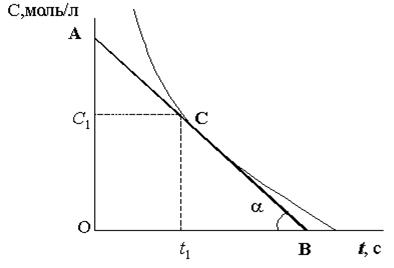
Данные, полученные всеми студентами, используют для построения графика, откладывая по оси ординат концентрации растворов (С, моль/л), а по оси абсцисс – время протекания реакции (t, с). Пример показан на рис. 2.
Итак, каждая группа студентов проводит касательную к точке на кривой, соответствующей исследуемой концентрации и определяет тангенс угла между касательной и абсциссой (tga ).Пример показан на рис. 2.
Например, ваша группа работала с концентрацией тиосульфата натрия С1 (моль/л). По данным, полученным всеми группами и занесенными в табл. 1, начерченную на доске, вы построите график С (моль/л) – t (с). К точке на графике, соответствующей концентрации С1, проводите касательную АВ (рис. 2) и находите тангенс угла наклона касательной к абсциссе (tga).
| |||
 | |||
 |
Эта величина в первом приближении равна скорости реакции (tga = v) как отношение отрезка АО : ОВ, что соответствует определению скорости реакции, которая равна отношению изменения концентрации реагирующего вещества (DС) к отрезку времени, за которое протекает реакция (v
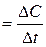 ). Определив скорость химической реакции, каждая группа студентов записывает полученные значения в табл. 1. Делаете общий вывод по результатам всей группы в опыте 1.
). Определив скорость химической реакции, каждая группа студентов записывает полученные значения в табл. 1. Делаете общий вывод по результатам всей группы в опыте 1.