Химическая переработка каменного угля
1) Низкотемпературная перегонка угля (швелевание, полукоксование). При этом способе уголь нагревают в специальных печах без доступа воздуха до температуры равной 500-600 °С. Цель – получение смолы и бензина. Смолы получают больше, чем при коксовании (до 10% к весу угля); так как отсутствуют вторичные пиролитические процессы, то в смоле содержится больше фенолов, нет бензола, конденсированных ароматических соединений. В ней содержатся алканы и алкены, циклические углеводороды. Отгоняемый бензин близок по составу к нефтяному крекинг-бензину. Кроме бензина, при разгонке смолы получают несколько сортов масел и пек. Выходы газа при этом процессе небольшие и его состав отличается от состава коксового газа (табл. 9)
Из 1 тонны угля получают 50-80 м³ швельгаза и до 10-15 грамм бензина. Первичная обработка швельгаза сходна с обработкой коксового газа. Твердый остаток – полукокс. Используется как топливо, содержит 7-11% летучих веществ.
Таблица 9
Состав швельгаза и коксового газа
| Составные части | Содержание (в объемных %) | |
| в швельгазе | В коксовом газе | |
| Водород | 15-20 | 50-60 |
| Метан | 55-65 | 25-35 |
| Прочие углеводороды | 5-8 | 2-3 |
| Аммиак | - | 1,2-1,5 |
2) Газификация углей. Газификацией твердого топлива называют искусственное превращение его органической части в горючие газы при помощи воздуха, водяного пара, других газов при высоких температурах. Газификация – удобный способ превращения в горючие газы низких сортов топлива. Газификация осуществляется в аппаратах, называющимися газогенераторами.
Смесь воздуха и водяного пара поступает через колосниковую решетку и слой шлака в зону горения, где уголь сгорает, выделяя тепло и давая CO2.
C + O2 → CO2
Затем газы поступают в зону восстановления, где контактируют с раскаленным углем:
C + H2O → CO + H2
C + CO2 → 2CO
Горячие газы далее поступают в зону сухой перегонки, где, соприкасаясь с углем, нагревают его, вызывая процессы термического разложения. Здесь газ обогащается высококалорийными веществами – углеводородами и кислородосодержащей органикой.
В самой верхней части газы подсушивают поступающее сверху топливо и выводятся наружу – на синтез (спиртов, горючего, аммиака и так далее). Таким образом, в промышленности получают в больших объемах «водяной газ».
Современные методы основаны на использовании газогенераторов с «кипящим» слоем частиц угля.
При подаче в газогенератор воды получают «Водяной газ», который обладает высокой калорийностью и является ценным сырьем для синтеза органических соединений.
Если в газогенератор подают воздух, получают так называемый «воздушный газ», содержащий примерно 65% азота, мало водорода, он обладает низкой калорийностью.
При подаче смеси воздуха и водяного пара получают так называемый «генераторный газ». Он содержит примерно 50% балласта (N2, CO2) обладает низкой теплотворной способностью (900-1500 ккал/м³) и используется на производстве как топливо. Разработан также способ получения высококалорийного газа из низкосортного твердого топлива – газификация угля под давлением. Процесс ведут под давлением 20-25 атмосфер, подается водяной пар с кислородом, образуется «водяной газ» (CO + H2), компоненты которого при таком давлении и температуре равной 700-800 ° вступают в реакцию между собой и углем:
2CO + 2H2  CH4 + CO2
CH4 + CO2
C + 2H2  CH4
CH4
Так получают высококалорийный газ из состава CH4 + CO + H2
3) Подземная газификация угля. Впервые эту идею высказал ещё Д.И. Менделеев. Принцип этого метода заключается в нагревании твердого топлива внутри земли, непосредственно на месте его залегания с подведением по трубам воздуха или кислорода. На другом конце обрабатываемого участка по трубам выводятся горючие газы, получившиеся в результате газификации. Преимущества этого способа очевидны – сокращение объема подземных работ, нет необходимости поднимать на поверхность огромные массы угля и особенно балластных пород, удобство передачи газа на большие расстояния.
4) Гидрогенизация угля. Гидрогенизация угля – это процесс получения из каменного угля жидкого топлива. В основу положен метод получения углеводородов по Бергиусу:

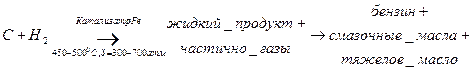
Паста, состоящая из мелких частиц угля, тяжелого масла и катализатора подается в реактор. Туда же подают водород, поддерживает нужное давление и температуру. Образуется жидкий и немного газообразного продукта. Жидкие продукты разделяют на ректификационной колонне, выделяя легкую фракцию – бензин, среднюю фракцию – смазочные масла и тяжелую фракцию «тяжелое» масло, которое идет на приготовление исходной реагентной пасты. В жидкие масла переходит 60-65% органической массы угля, а остальные 35% обычно превращаются в углеводородные газы, которые могут быть использованы для химических синтезов или в качестве моторного топлива. Промышленное оформление процесса гидрирования твердых топлив очень сложно, так как необходимо применение особых сталей и специальных аппаратов из-за высоких давлений и температур и наличие водорода.
Контрольные вопросы:
1. Рассчитайте объем воздуха (н.у.), необходимый для сжигания 100 кг каменного угля, содержащего 85 мас.% углерода.
2. Большее количество теплоты выделится при сжигании: а) бурого угля; б) антрацита; в) каменного угля; г) торфа.
3. Что представляет собой нефть?
4. Какие продукты можно получить при термическом и каталитическом крекинге нефти?
5. Для получения водорода из метана используют процесс конверсии. Укажите условия протекания этого процесса и запишите уравнение реакции.
6. Приведите уравнения реакций получения «водяного пара».
ПРОМЫШЛЕННАЯ СТЕХИОМЕТРИЯ
Стехиометрия – это раздел химии, исследующий количественные изменения, происходящие при химических реакциях. Термин «стехиометрия» введённый И. Рихтером, происходит от греческого слова «стехион» означающий «элементарный состав» и «метрей» (измерять). Основные усилия химиков XVIII и XIX веков были посвящены определению весовых соотношений элементов в веществах, что привело к накоплению современных знаний об атомных массах и к открытию новых элементов.
Стехиометрия имеет фундаментальное значение в современной химии. Она является основой количественного химического анализа. В химической промышленности знание стехиометрии необходимо для правильного ведения технологического процесса определения выхода химических продуктов и эффективности химических процессов. Стехиометрические методы также позволяют биохимикам прослеживать метаболические процессы, протекающие в живых организмах, например, процесс выделения энергии в их клетках.
Количественные законы химии
В химических реакциях одно или несколько веществ изменяют свой состав, давая новые вещества. Вещества, подвергающиеся превращению, называются реагентами, а вновь образующиеся вещества – продуктами. Тогда любая химическая реакция может быть записана в виде:
Реагенты → Продукты
В основе всех количественных химических расчетов лежат несколько основных законов химии.
1) Закон сохранения массы (материи) (Ломоносов-Лавуазье, 1756; 1785 гг). Современная формулировка этого закона такова: «Масса реагентов равна массе продуктов реакции». Общая масса участников реакции остается неизменной.
Масса вещества в системе СИ измеряется в килограммах, в химической практике – в мг, г, в химической технологии – в тоннах (т).
2) Закон постоянства состава (Пруст): «Химический состав вещества не зависит от способа его получения. Каким бы способом не было получено вещество, его качественный и количественный состав постоянен».
3) Закон кратных отношений (Дальтон): «Если два элемента образуют несколько соединений, то массы одного элемента, приходящиеся на одну и ту же массу атомов другого элемента, относятся между собой как небольшие целые числа»
Эти законы послужили основой для развития химии как количественной науки. В химических лабораториях, в химической промышленности обычно имеют дело с макроколичествами веществ, каждое из которых состоит из множества простых химических частиц (атомов, ионов, молекул).
Количественную связь между макро и микрообластью химии устанавливает понятие «количество вещества» - это физико-химическая величина, характеризующая макропорцию вещества. Единица количества вещества – моль.
Моль – это количество вещества, содержащее столько же структурных единиц, сколько их содержится в 12 г изотопа С12 .
Структурная единица – это атом, молекула, ион, электрон и т.д.
В 1 моле любого вещества содержится 6,02·1023 структурных единиц, например, 1 моль алюминия содержит 6,02·1023 атомов алюминия и в 1 моле серной кислоты содержится 6,02·1023 молекул H2SO4.
Молярная масса вещества – это отношение массы некоторой порции вещества к количеству вещества в этой порции:
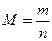 , где
, где
М – молярная масса вещества, г/моль;
m – масса вещества, г;
n – количество вещества, моль.
Численно молярная масса простого одноатомного вещества совпадает с относительной атомной массой элемента, а для соединения – с его относительной молекулярной массой.
Например,
| Наименование вещества | Атомная масса | Молярная масса |
| 1 моль Al | 27,00 | 27 г/моль |
| 1 моль H2SO4 | 98,00 | 98 г/моль |
В технических расчетах применяют укрупненные единицы измерения массы – это килограмм (кг), тонна (т); объема – кубический метр (м3). Количество вещества можно выразить в киломолях (кмоль), соответственно, молярная масса в кг/кмоль.
Состав гомогенной газовой смеси выражают в объемных процентах (об.%), а так же в мольных долях каждого компонента данной смеси. Мольная доля компонента А в смеси газов, состоящей из компонентов А и В определяется выражением XA = nA/nA+nB ,:
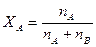 ,
,
где nA – число молей компонента А, nB – число молей компонента В, ХА – мольная доля компонентов А.
Для промышленных процессов очень важен выход реакции.
Масса продуктов, образующихся в ходе реакции, называется выходом.
Теоретический выход – выход продукта, вычисленный на основе уравнения реакции.
Фактический выход – действительный выход, полученный в эксперименте или в промышленном процессе.
Когда фактический выход равен теоретическому, говорят, что реакция имеет количественный выход. Реакцию, протекающую с количественным выходом, называют стехиометрическим процессов. К таким реакциям относятся многие ионные процессы (реакции нейтрализации, осаждения). Однако чаще всего реакции, особенно органические не имеют количественного выхода. Их принято характеризовать относительным выходом.
Относительный выход = Фактический выход/Теоретический выход * 100%
Относительный выход служит мерой эффективности реакции. Так, реакции, протекающие с количественным выходом имеют 100%-ную эффективность.
Для повышения относительного выхода обычно используют избыточное количество одного или нескольких реагентов. В этом случае теоретический выход вычисляют по количеству того реагента, который не используется в избытке. Такой реагент называют лимитирующим.
Пример: бромбензол можно получить по реакции бензола с избыточным количеством брома в присутствии FeCl3. В одном из экспериментов 23,0 г бромбензола было получено из 20,0 г бензола. Вычислим относительный выход этой реакции.
Решение:
C6H6 + Br2 → C6H5Br + HBR
mбензола = 20 г
MC6H6 = 78 г/моль, тогда
MC6H6 = m/M = 20/78 = 0,256 моль
при 100%-ной эффективности реакции из 1 моля C6H6 должно получиться 1 моль C6H5Br.
Значит, теоретический выход 0,256 моля C6H5Br т.к. M(C6H5Br) = 157 г моль, тогда
теоретический выход = (0,256 моль) * 157 = 40,2 г
Относительный выход = 23,0/40,2 * 100% = 57,2 %
Отправной пункт при рассмотрении эффективности любого химического процесса – его стехиометрия. Теоретически суммарная масса продуктов химического процесса должна быть равна суммарной массе реагентов, используемых в процессе, однако на практике это далеко не так. Указанное требование известно как баланс масс или материальный баланс. Оно вытекает непосредственно из закона сохранения материи.
На практике в любом процессе приходится использовать один или несколько реагентов в избыточном количестве, кроме того могут образовываться побочные продукты. Поэтому в промышленности термин «баланс масс» означает равенство количества реагентов суммарной массе всех образовавшихся целевых и побочных продуктов, а также неиспользованных реагентов и растворителей в конце процесса.
Следует различать теоретический баланс масс и фактический баланс масс.
Теоретический баланс масс включает предсказываемый выход целевого продукта, он основан на вычислениях или экспериментальных данных, полученных в лабораториях. Во многих процессах фактический баланс масс отличается от теоретического из-за неизбежных (или преодолимых) потерь материалов.
В промышленности вместо понятия «реагент» используют термин «сырье», «исходные материалы». Чтобы какой-либо процесс был экономически оправдан, необходимо достичь оптимального выхода продукта. Оптимальный выход не обязательно должен совпадать с теоретическим выходом, т.к. достижение последнего может, например, потребовать значительного расхода дорогостоящего компонента или же слишком длительного проведения процесс, что приводит к снижению экономической эффективности производства. Во многих технологических процессах оптимальный выход целевого продукта соответствует использованию лишь некоторой части исходных материалов.
Фактический выход каждого конкретного процесса может зависеть от целевого ряда факторов: температуры, давления, скорость перемешивания, наличие катализаторов, частота сырья, эффективность процедур извлечения продуктов.
Контрольные вопросы:
1. Определите количество Н2SO4 (кмоль), содержащееся в 100 кг.
2. Синтез аммиака описывают реакцией N2 + 3H2 = 2NH3. Определите объемы азота и водорода для получения 200 м3 аммиака (н.у.).
3. Рассчитайте относительный выход реакции N2 + 3H2 = 2NH3, проведенной в промышленных условиях, если из 100 м3 азота и 300 м3 водорода получено 160 м3 аммиака.
4. Рассчитайте массу железа, которую можно получить из 3 т руды, содержащей 92 мас.% Fe3O4.
5. Теоретический выход реакции составляет 100 г вещества А. В опыте получено 80 г этого вещества. Рассчитайте относительный выход реакции.
ТЕХНОЛОГИЧЕСКИЕ ОПЕРАЦИИ В ОРГАНИЧЕСКОМ СИНТЕЗЕ И ИХ АППАРАТУРНОЕ ОФОРМЛЕНИЕ
Подготовка сырья
Сырье поступает на производство в твердом, жидком и газообразном состояниях. Обычно оно освобождается от примесей, которые могут повлиять на выход продукта. Такими примесями являются: пустая порода в рудных и нерудных материалах, влага, пыль, посторонние включения механического характера, посторонние газы.
Приемы очистки твердых, жидких и газообразных веществ разнообразны.
Для очистки твердого сырья используют:
- разность удельных весов сырья и пустой породы (такая очистка проводится в токе воды или воздуха, в тяжелых жидкостях и суспензиях и т.д.);
- различие формы и размеров кусков сырья и пустой породы и коэффициента трения этих тел (грохочение, сита);
- флотацию – избирательное смачивание водой частиц сырья и пустой породы при помощи добавочных веществ, называемых флотореагентом;
- удаление влаги механическими способами (центрифугирование, прессование, отжим) или тепловыми способами (сушка в сушильных аппаратах горячим воздухом, газами). Процесс ускоряется при создании вакуума.
Для очистки жидкостей от твердых частиц используют отстаивание и фильтрацию (удаление твердых частиц) или центрифугирование.
- осушку жидкостей осуществляют:
- введением химических осушителей (KOH, CaCl2, MgSO4,P2O5,Al2O3, силикагель), взаимодействующих с водой;
- отгонкой воды в виде азеотропных смесей;
- использованием специальных ультрафильтрационных мембран.
Очистка от растворенных ионных соединений происходит при:
- пропускании через специальные ионные смеси (катионит, анионит);
- использовании специальных обратноосмотических фильтрующих мембран и электродиализных фильтрующих мембран.
При очистке газов необходимо удаление твердых частиц, которое осуществляют пропусканием газа через фильтрующую перегородку, через электрическое поле высокого напряжения, использованием центробежной силы, пропусканием газа через слой жидкости (барботаж).
Для осушки газов используют вымораживание или пропускание через твердые осушители (Al2O3, цеолиты – природные и синтетические и т.д.).
Очистка газов от вредных примесей (например, от H2S), осуществляется методом абсорбции, т.е. пропусканием газа через аппарат колонного типа (скруббер), заполненный инертной твердой насадкой или адсорбции, т.е. пропусканием через колонну с твердым адсорбентом (Al2O3, активированный уголь).
Очищенные таким образом сырьевые материалы в определенной дозировке направляются в реакционные аппараты и реакторы.
Дозировка твердых осушителей при помощи автоматических весов, жидкости дозируют по весу или, чаще, по объему (мерники). Газ дозируют с использованием различных приборов (ротаметры, трубки Вентури, газовые часы и т.д.).
