Основные стехиометрические законы
Лекция 1
Основные понятия и стехиометрические законы химии
Химия– наука о свойствах вещества и его превращениях, она включает в себя законы и принципы, описывающие эти превращения, а так же представления и теории, позволяющие дать им объяснение.
Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы.


Вещества подразделяют на простые и сложные (хим. соединения).
Простые вещества образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, напр. сера, железо, озон, алмаз.
Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся в некоторых пределах (нестехиометрические соединения или бертоллиды).
Молекула - наименьшая частица вещества, обладающая его химическими свойствами.
Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства.
Различным элементам соответствуют различные атомы, обозначаемые символом данного элемента (Ag, Fe, Mg).
Химический элемент - это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
В настоящее время известно 118 элементов: 89 из них найдены в природе (на Земле), остальные получены искусственным путем. Атомы существуют в свободном состоянии, в соединениях с атомами того же или других элементов, образуя молекулы. Способность атомов вступать во взаимодействие с другими атомами и образовывать химические соединения определяется его строением. Атомы состоят из положительно заряженного ядра и отрицательно заряженных электронов, движущихся вокруг него, образуя электронейтральную систему, которая подчиняется законам, характерным для микросистем.
Ионы (от греч. ion– идущий), одноатомные или многоатомные частицы, несущие электрический заряд.
Положительные ионы называют катионами (от греч. kation, буквально – идущий вниз),
отрицательные – анионами (от греч. anion, буквально идущий вверх). В свободном состоянии существуют в газовой фазе (в плазме).
Валентность (от лат. valentia– сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи.
В рамках электронной теории химической связи валентность атома определяется числом его неспаренных электронов в основном или возбужденном состоянии, участвующих в образовании общих электронных пар с электронами других атомов.
Реакции химические (от лат. re- – приставка, означающая обратное действие, и actio –действие), превращения одних веществ (исходных соединений) в другие (продукты реакции) при неизменяемости ядер атомов. Исходные вещества иногда называют реагентами, однако чаще (особенно в органической химии) термин "реагент" используют по отношению к одному, наиболее активному исходному соединению, определяющему направление химической реакции.
Атомное ядро - центральная часть атома, состоящая из Z протонов и N нейтронов, в которой сосредоточена основная масса атомов.
Заряд ядра - положительный, по величине равен количеству протонов в ядре или электронов в ней. Сумма протонов и нейтронов атомного ядра называется массовым числом A = Z + N.
Изотопы - химические элементы с одинаковыми зарядами ядер, но различными массовыми числами за счет разного числа нейтронов в ядре.
Так кислород имеет изотопы с массовыми числами 16,17, 18.
Атомная масса элемента равна среднему значению из масс всех его природных изотопов с учетом их распространенности. Например, природный хлор состоит из 75,4% изотопа с массовым числом 35 и из 24,6% изотопа с массовым числом 37; средняя атомная масса хлора 35, 453.
Изобары –атомы, имеющие одинаковую массу, но различные заряды ядра (атомные номера) и разные химические свойства. Они имеют одинаковое суммарное количество протонов и нейтронов в ядре, принадлежат к разным химическим элементам. Например: 40Ar, 40K, 40Ca;54Cr,54Fe; 112Cd, 112Sn и др.
Химическая формула - это условная запись состава вещества с помощью химических знаков (предложены в 1814 г. Й. Берцелиусом) и индексов (индекс - цифра, стоящая справа
внизу от символа, обозначает число атомов в молекуле).
Химическая формула показывает, атомы каких элементов и в каком соотношении соединены между собой в молекуле.
Молекулы простых веществ состоят из атомов одного и того же элемента.
Молекулы сложных веществ состоят из атомов различных химических элементов.
Международная единица атомных масс равна 1/12 массы изотопа 12C - основного изотопа природного углерода.
1 а.е.м = 1/12 • m (12C) = 1,66057 • 10-26 кг
Относительная атомная масса (Ar) - безразмерная величина, равная отношению средней массы атома элемента (с учетом процентного содержания изотопов в природе) к 1/12 массы атома 12C.
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода 12C. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов с учетом индексов.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а.е.м.
Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения - моль.
Количество вещества, моль (n). Означает количество вещества, содержащее столько структурных единиц (молекул, атомов, ионов, электронов и др.), сколько атомов содержится в 0,012 кг изотопа углерода 12С, например,
1 моль атомов 12С=6,02*10 атомов 12С
1 моль молекул Н2О=6,02*1023 молекул Н2О
1 моль ионов SO42-=6,02*1023 ионов SO42-
Число Авогадро(NA) означает, что количество частиц в 1 моль любого вещества одно и то же и равно 6,02 • 1023. моль-1 (зная массу одного атома углерода (1,993 *10 -26 кг),можно вычислить число атомов NA в 0.012 кг углерода : NA =0,012 кг/моль / 1.993 *10-26 = 6.02*10 23 моль-1).
Молярная масса (М) вещества равна отношению массы вещества к соответствующему количеству вещества и численно равна его относительной молекулярной массе, однако первая величина имеет размерность г/моль, а вторая - безразмерная. Масса (m) и количество вещества (n)понятия разные. Масса выражается в килограммах (граммах), а количество вещества – в молях, между ними существуют соотношения:
m = nM , n = m/M , M = m/n.
Пример 2
Определите выход реакции получения вольфрама методом алюминотермии, если из 33,14 г концентрата руды, содержащей WO3 и невосстанавливающиеся примеси (массовая доля примесей 0,3) было получено 12,72 г металла?
Пример 3.Сколько граммов осадка сульфата бария образуется при сливании растворов, содержащих 20,8 г хлорида бария и 18,0 г сульфата натрия?
Закон постоянства состава
Впервые сформулировал Ж.Пруст (1808 г): все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения.
Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных массовых соотношениях.
Пример.
CuS – сульфид меди. m(Cu) : m(S) = Ar(Cu) : Ar(S) = 64 : 32 = 2 : 1
Чтобы получить сульфид меди (CuS) необходимо смешать порошки меди и серы в массовых отношениях 2 : 1.
Если взятые количества исходных веществ не соответствуют их соотношению в химической формуле соединения, одно из них останется в избытке.
Например, если взять 3 г меди и 1 г серы, то после реакции останется 1 г меди, который не вступил в химическую реакцию. Вещества немолекулярного строения не обладают строго постоянным составом. Их состав зависит от условий получения.
Массовая доля элемента w(Э) показывает, какую часть составляет масса данного элемента от всей массы вещества: где n - число атомов; Ar(Э) - относительная атомная масса элемента; Mr - относительная молекулярная масса вещества.
w(Э) = (n • Ar(Э)) / Mr
Зная количественный элементный состав соединения можно установить его простейшую молекулярную формулу:
Задание:
Определите формулу оксида хрома, содержащего 68,4 %хрома.
Закон кратных отношении
(Д.Дальтон, 1803 г.): если два химических элемента дают несколько соединений, то весовые доли одного и того же элемента в этих соединениях, приходящиеся на одну и ту же весовую долю второго элемента, относятся между собой как небольшие целые числа. Например: N2O3 ; NO2; N2O5
число атомов кислорода в молекулах этих соединений, приходящиеся на два атома азота, относятся между собой как 3 : 4 : 5.
Закон объемных отношений
(Гей-Люссак, 1808 г.): Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа.
Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества.
Пример.
2CO+O2=2CO2.
При окислении двух объемов оксида углерода (II) одним объемом кислорода образуется 2 объема углекислого газа, т.е. объем исходной реакционной смеси уменьшается на 1 объем
.
Закон Авогадро(1811 г.):
Пример1.
Какой объем водорода при н.у. выделится при растворении 4,8 г магния в избытке соляной кислоты?
Пример 2.
3,17 г хлора занимают объем равный 1 л (при н.у.). Вычислите по этим данным молекулярную массу хлора.
Пример 3.
Газообразное соединение азота с водородом содержит 12,5% (масс.) водорода. Плотность соединения по водороду равна 16. Найти молекулярную формулу соединения.
Объединенный газовый закон - объединение трех независимых частных газовых законов: Гей-Люссака, Шарля, Бойля-Мариотта, уравнение, которое можно записать так:
(P•V)/T=(P0 • V0)/T0
М окс
Мэоксида =ƒэкв∙Мокс = ———
No ∙ noО.
где: Nо - число атомов кислорода
nоО – степень окисления кислорода в оксиде, которая равна всегда - 2.
Например:
Мэ (Mn2O7) = —— = 15,9 г/моль
7 ∙ 2
Молярная масса эквивалента кислоты равна произведению фактора эквивалентности на молярную массу кислоты
Мк
Мэкислоты =ƒэкв∙Мк= —
Nн+
где: Мк - молекулярная (формульная) масса кислоты
Nн+ - число атомов водорода, способных замещаться на металл.
Пример: Мэ (H2SO4) = 1/2 ∙ 98 = 49 г/моль
Молярная масса эквивалента основания равна произведению фактора эквивалентности на молярную массу основания
Мосн
Мэ основания =ƒэкв∙Мосн = ——
Nон-
ПримерМэ[Cr(OH)3 ] = 1/3 ∙ 103 = 34,3 г/моль
Молярная масса эквивалента соли равна произведению фактора эквивалентности на молярную массу соли
Мэ соли =ƒэкв соли ∙ Мс = 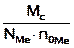

Nме – число атомов металла
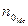 - степень окисления металла
- степень окисления металла
МэAl2(SO4)3= ——— = 57 г/моль
2* 3
В ОВР для определения ƒэкв необходимо единицу разделить на число отданных или присоединенных электронов. Например, в реакции:Na2SO3+KMnO4+H2SO4→Na2SO4+MnSO4+K2SO4+H2O
ƒэкв(KMnO4)=1/5, так как:MnO4- + 8H+ + 5ē = Mn2+ + 4H2O
В 1792 г. немецким физиком Рихтером был сформулирован закон эквивалентов: массы реагирующих друг с другом веществ (m1,m2) пропорциональны молярным массам их эквивалентов (МЭ1,МЭ2)
m1 Mэ1
—— = ———
m2 МЭ2
Из математической записи закона эквивалентов следует, что количество моль - эквивалентов веществ в реакции равны между собой.
nэкв1 = nэкв2
Для реакций с участием газов используют молярный объем эквивалента – это объем, занимаемый 1 моль-эквивалентом газа.
Так, МЭ(Н) = 1г/моль, если моль газа 2г/моль занимают V=22,4л, то 1 эквивалент – в два раза меньший объем, равный 11,2 л.
VЭКВ (Н2) = 22,4 : 2 = 11,2л.
Аналогично МЭКВ(О)= ¼ М(О2) = 32 : 4 = 8г/моль, отсюда
Vэ(О2) = 22,4 : 4 = 5,6л.
Тогда математическая запись закона через эквивалентный объем:
mв-ва Vгаза mв-ва МЭв-ва
—— = —— <=> —— = ——
MЭв Vэгаза Vгаза VЭг
Пример 1: Молярная масса эквивалента некоторого металла равна 12 г/моль. Какая масса этого металла прореагировала с кислотой, если при этом выделилось 1150 мл водорода (н.у.)?
Решение: По закону эквивалентов число моль эквивалентов прореагировавшего металла и водорода одинаково:
nэкв(1/z Ме) = nэкв(1/z Н2).
Выразим число моль эквивалентов металла через отношение масс, а для водорода – через отношение объемов :
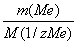 =
= 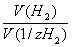 .
.
Ответ: 1.23 г.
Пример 2: При нагревании в кислороде 3.60 г некоторого металла его масса увеличилась до 5.04 г. Рассчитайте молярную массу эквивалента металла и его оксида.
Ответ: 20 г/моль; 28 г/моль.
Пример 3: В оксиде некоторого элемента массовая доля кислорода составляет 20 %. Рассчитайте молярную массу эквивалента элемента и его оксида.
Ответ: 32 г/моль; 40 г/моль.
Лекция 1
Основные понятия и стехиометрические законы химии
Химия– наука о свойствах вещества и его превращениях, она включает в себя законы и принципы, описывающие эти превращения, а так же представления и теории, позволяющие дать им объяснение.
Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы.


Вещества подразделяют на простые и сложные (хим. соединения).
Простые вещества образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, напр. сера, железо, озон, алмаз.
Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся в некоторых пределах (нестехиометрические соединения или бертоллиды).
Молекула - наименьшая частица вещества, обладающая его химическими свойствами.
Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства.
Различным элементам соответствуют различные атомы, обозначаемые символом данного элемента (Ag, Fe, Mg).
Химический элемент - это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
В настоящее время известно 118 элементов: 89 из них найдены в природе (на Земле), остальные получены искусственным путем. Атомы существуют в свободном состоянии, в соединениях с атомами того же или других элементов, образуя молекулы. Способность атомов вступать во взаимодействие с другими атомами и образовывать химические соединения определяется его строением. Атомы состоят из положительно заряженного ядра и отрицательно заряженных электронов, движущихся вокруг него, образуя электронейтральную систему, которая подчиняется законам, характерным для микросистем.
Ионы (от греч. ion– идущий), одноатомные или многоатомные частицы, несущие электрический заряд.
Положительные ионы называют катионами (от греч. kation, буквально – идущий вниз),
отрицательные – анионами (от греч. anion, буквально идущий вверх). В свободном состоянии существуют в газовой фазе (в плазме).
Валентность (от лат. valentia– сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи.
В рамках электронной теории химической связи валентность атома определяется числом его неспаренных электронов в основном или возбужденном состоянии, участвующих в образовании общих электронных пар с электронами других атомов.
Реакции химические (от лат. re- – приставка, означающая обратное действие, и actio –действие), превращения одних веществ (исходных соединений) в другие (продукты реакции) при неизменяемости ядер атомов. Исходные вещества иногда называют реагентами, однако чаще (особенно в органической химии) термин "реагент" используют по отношению к одному, наиболее активному исходному соединению, определяющему направление химической реакции.
Атомное ядро - центральная часть атома, состоящая из Z протонов и N нейтронов, в которой сосредоточена основная масса атомов.
Заряд ядра - положительный, по величине равен количеству протонов в ядре или электронов в ней. Сумма протонов и нейтронов атомного ядра называется массовым числом A = Z + N.
Изотопы - химические элементы с одинаковыми зарядами ядер, но различными массовыми числами за счет разного числа нейтронов в ядре.
Так кислород имеет изотопы с массовыми числами 16,17, 18.
Атомная масса элемента равна среднему значению из масс всех его природных изотопов с учетом их распространенности. Например, природный хлор состоит из 75,4% изотопа с массовым числом 35 и из 24,6% изотопа с массовым числом 37; средняя атомная масса хлора 35, 453.
Изобары –атомы, имеющие одинаковую массу, но различные заряды ядра (атомные номера) и разные химические свойства. Они имеют одинаковое суммарное количество протонов и нейтронов в ядре, принадлежат к разным химическим элементам. Например: 40Ar, 40K, 40Ca;54Cr,54Fe; 112Cd, 112Sn и др.
Химическая формула - это условная запись состава вещества с помощью химических знаков (предложены в 1814 г. Й. Берцелиусом) и индексов (индекс - цифра, стоящая справа
внизу от символа, обозначает число атомов в молекуле).
Химическая формула показывает, атомы каких элементов и в каком соотношении соединены между собой в молекуле.
Молекулы простых веществ состоят из атомов одного и того же элемента.
Молекулы сложных веществ состоят из атомов различных химических элементов.
Международная единица атомных масс равна 1/12 массы изотопа 12C - основного изотопа природного углерода.
1 а.е.м = 1/12 • m (12C) = 1,66057 • 10-26 кг
Относительная атомная масса (Ar) - безразмерная величина, равная отношению средней массы атома элемента (с учетом процентного содержания изотопов в природе) к 1/12 массы атома 12C.
Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода 12C. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов с учетом индексов.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а.е.м.
Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения - моль.
Количество вещества, моль (n). Означает количество вещества, содержащее столько структурных единиц (молекул, атомов, ионов, электронов и др.), сколько атомов содержится в 0,012 кг изотопа углерода 12С, например,
1 моль атомов 12С=6,02*10 атомов 12С
1 моль молекул Н2О=6,02*1023 молекул Н2О
1 моль ионов SO42-=6,02*1023 ионов SO42-
Число Авогадро(NA) означает, что количество частиц в 1 моль любого вещества одно и то же и равно 6,02 • 1023. моль-1 (зная массу одного атома углерода (1,993 *10 -26 кг),можно вычислить число атомов NA в 0.012 кг углерода : NA =0,012 кг/моль / 1.993 *10-26 = 6.02*10 23 моль-1).
Молярная масса (М) вещества равна отношению массы вещества к соответствующему количеству вещества и численно равна его относительной молекулярной массе, однако первая величина имеет размерность г/моль, а вторая - безразмерная. Масса (m) и количество вещества (n)понятия разные. Масса выражается в килограммах (граммах), а количество вещества – в молях, между ними существуют соотношения:
m = nM , n = m/M , M = m/n.
Основные стехиометрические законы
Закон сохранения массы веществ (М.В.Ломоносов, 1748 г.; А.Лавуазье, 1789 г.):
