V1: 01. основные законы и понятия химии
V1: 01. ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ
V2: 01. Основные классы неорганических соединений
I: 01.01;
S: Степень окисления марганца в следующих соединениях: KMnO4, MnO2, H2MnO4, MnSO4 равна соответственно ###
+: +7, +4, +6, +2
-: +6, +4, +7, +2
-: +4, +4, +6, +7
-: +2, +6, +4, +7
I: 01.02;
S: Степень окисления хрома в следующих соединениях: KCrO2, Na2Cr2O7, BaCrO4, CrF3 равна соответственно ###
+: +3, +6, +6, +3
-: +6, +4, +7, +2
-: +4, +4, +6, +7
-: +2, +6, +4, +7
I: 01.03;
S: Степень окисления азота в следующих соединениях: AgNO2, NO2, NaNO2, NH3 равна соответственно ###
+: +3, +4, +3, –3
-: +3, +4, +3, +3
-: +5, +4, +5, +3
-: +4, +4, +6, +7
I: 01.04;
S: Степень окисления серы в следующих соединениях: H2S, CaSO4, Na2SO3, H2SO4
равна соответственно ###
+: –2, +6, +4, +6
-: +6, +4, +7, +2
-: +4, +4, +6, +7
-: +2, +6, +4, +6
I: 01.05;
S: В избытке щелочи не растворяется ###
-: А1(ОН)3
+: Mg(OH)2
-: Сr(ОН)3
-: Zn(OH)2
I: 01.06;
S: Со щелочами взаимодействуют оксиды ### (не менее двух вариантов)
-: железа (II)
+: хрома (III)
+: серы (IV)
-: азота (II)
I: 01.07;
S: Кислотный характер имеет оксид, формула которого ###
-: Al2O3
-: СО
-: СаО
+: Р2О5
I: 01.08;
S: Основный характер имеет оксид, формула которого ###
-: Mn2O7
-: Al2O3
+: BaO
-: Cr2О3
I: 01.09;
S: Оксид цинка не реагирует с ###
+: NO
-: SO2
-: СО2
-: NaOH
I: 01.10;
S: Амфотерными являются оксиды ### (не менее двух вариантов)
-: марганца (VII)
+: алюминия
-: кальция
+: бериллия
I: 01.11;
S: В ряду оксидов Na2О → MgO → Al2O3 происходит переход от ###
-: амфотерного оксида к кислотному
-: кислотного оксида к основному
-: основного оксида к кислотному
+: основного оксида к амфотерному
I: 01.12;
S: Кислотными являются гидроксиды ### (не менее двух вариантов)
-: олова (IV)
-: железа (III)
+: азота (III)
+: серы (VI)
I: 01.13;
S: Кислотный характер имеют оксиды, образованные металлами ###
-: со степенью окисления ниже +4
-: главных подгрупп
+: со степенью окисления равной или выше +4
-: с любой степенью окисления
I: 01.14;
S: К кислотным оксидам относится ###
+: N2O5
-: NO
-: N2O
-: N2O2
I: 01.15;
S: Кислота образуется при растворении в воде оксида ###
-: N2O
-: SiO2
+: Р2О5
-: К2О
I: 01.16;
S: Между собой взаимодействуют соединения ### (не менее двух вариантов)
-: К2О, СаО
+: Na2O, N2O5
+: ВаО, СгОз
-: СО2, SO3
I: 01.17;
S: Все вещества реагируют между собой в группе ###
-: HC, НВг, HI
-: BaO, MgO, CuO
-: КОН. Са(ОН)2, Fe(OH)3
+: SO3, CaO, Al2O3
I: 01.18;
S: Соль образуется при ###
-: обугливании сахара в серной кислоте
-: растворении негашеной извести в воде
-: разложении перекиси водорода
+: горении железа в хлоре
I: 01.19;
S: Выделение газа при добавлении сильной кислоты в исследуемый раствор указывает на наличие ионов ###
-: PO43–
-: Cl–
+: CO32–
-: NO3–
I: 01.20;
S: При взаимодействии 2 моль гидроксида натрия и 1 моль серной кислоты образуется ### соль и вода
+: средняя
-: двойная
-: основная
-: кислая
I: 01.21;
S: При взаимодействии 1 моль гидроксида кальция и 1 моль углекислого газа образуется ### соль и вода
-: двойная
+: средняя
-: кислая
-: основная
I: 01.22;
S: Основные соли образуют гидроксиды ### (не менее двух вариантов)
+: меди (II)
-: натрия
+: цинка
-: калия
I: 01.23;
S: Кислые соли образуют гидроксиды ### (не менее двух вариантов)
+: H2S
+: H2SO4
-: HCl
-: HNO3
I: 01.24;
S: При взаимодействии 3 моль гидроксида натрия и 1 моль фосфорной кислоты образуется ### соль и вода
-: основная
-: двойная
+: средняя
-: кислая
I: 01.25;
S: При взаимодействии избытка раствора NаОН с H3PO4 образуется ###
-: Na2HPO4
-: Na2НРО3
+: Na3PO4
-: NaH2PO4
I: 01.26;
S: При взаимодействии 1 моль гидроксида натрия и 1 моль серной кислоты образуется ### соль и вода
-: двойная
-: основная
+: кислая
-: средняя
V1: 02. Основные закономерности протекания химической реакции
V2: 02. Химическая кинетика
I: 02.01;
S: При уменьшении объема системы в 3 раза скорость прямой реакции,
N2(г)+3Н2(г) 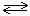 2NН3(г) ###
2NН3(г) ###
-: уменьшится в 27 раз
+: возрастет в 81 раз
-: уменьшится в 81 раз
-: возрастет в 27 раз
I: 02.02;
S: При повышении температуры на 300 (g=3) скорость реакции увеличится###
-: в 9 раз
+: в 27 раз
-: в 81 раз
-: в 3 раза
I: 02.03;
S: Равновесие реакции 2H2(г)+O2(г) 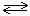 2H2O(г) ; DH<0 смещается влево при:
2H2O(г) ; DH<0 смещается влево при:
-: понижении температуры
-: увеличении давления
-: уменьшении концентрации H2O
+: повышении температуры
I: 02.04;
S: Добавление катализатора смещает равновесие химической реакции ###
-: в сторону продуктов
-: в сторону исходных веществ
+: не влияет на положение равновесия
-: влияет неоднозначно
I: 02.05;
S: Равновесие реакции CaCO3(т) 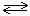 CaO(т)+CO2(г) при повышении давления сместится###
CaO(т)+CO2(г) при повышении давления сместится###
+:влево
I: 02.06;
S: При увеличении давления в системе в 2 раза скорость прямой реакции (при условии ее элементарности) CO(г)+2Н2(г) 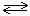 CH3OH(ж) ###
CH3OH(ж) ###
-: уменьшится в 4 раза
-: увеличится в 4 раза
+: увеличится в 8 раз.
-: уменьшится в 8 раз
I: 02.07;
S: При увеличении концентрации водорода в 2 раза скорость реакции С(т)+2H2(г) 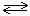 СH4(г) возрастет в ### раза
СH4(г) возрастет в ### раза
+: 4
I: 02.08;
S: Добавление катализатора ### энергию активации химической реакции
-: увеличивает
+: уменьшает
-: не влияет
-: делает равной нулю
I: 02.09;
S:Математическое выражение для константы равновесия гетерогенной химической реакции 2NaHCO3 (кр.) = Na2CO3 (кр.) + H2O (г.) + CO2 (г.) имеет вид
-: 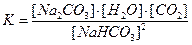
-: 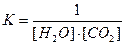
-: 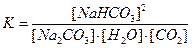
+: 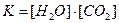
I:02.10;
S: При увеличении давления в системе H2 (г) + I2 (г) Û 2HI (г), DH°<0 равновесие смещается###
-: в сторону продуктов
-: в сторону исходных веществ
-: не достаточно данных для ответа
+: положение равновесия не изменяется
I: 02.11;
S: При повышении температуры на ### скорость реакции возросла в 8 раз (g=2)
+: 300
I: 02.12;
S: При понижении температуры на ###, скорость химической реакции уменьшается в 125 раз, g=5
+: 300
I: 02.13;
S:При увеличении давления в системе 3H2 (г) + N2 (г) Û 2NH3 (г) равновесие смещается
+: в сторону продуктов
-: в сторону исходных веществ
-: не достаточно данных для ответа
-: положение равновесия не изменяется
I: 02.14;
S: Скорость реакции СО2(г)+C(т) 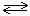 2CO(г) возрастает в 3 раза при увеличении концентрации углекислого газа###
2CO(г) возрастает в 3 раза при увеличении концентрации углекислого газа###
+: в 3 раза
I: 02.15;
S: Равновесие реакции 2NO(г)+O2(г) 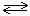 2NO2(г) ; DH<0
2NO2(г) ; DH<0
смещается влево при:
-: увеличении давления
+: повышении температуры
-: понижении температуры
-: увеличении концентрации NO
I: 02.16;
S: При увеличении температуры в системе 3H2 (г) + N2 (г) Û 2NH3 (г), DH°<0 равновесие смещается:
-: в сторону продуктов
+: в сторону исходных веществ
-: не достаточно данных для ответа
-: положение равновесия не изменяется
I: 02.17;
S:При повышении температуры равновесие смещается в сторону###
-: экзотермической реакции
+: эндотермической реакции
-: увеличения объема
-: уменьшения объема
I: 02.18;
S: При понижении температуры равновесие смещается в сторону###
+: экзотермической реакции
-: эндотермической реакции
-: увеличения объема
-: уменьшения объема
I: 02.19;
S:При понижении давления равновесие смещается в сторону…
-: экзотермической реакции
-: эндотермической реакции
+: увеличения объема
-: уменьшения объема
I: 02.20;
S: При повышении давления равновесие смещается в сторону…
-: экзотермической реакции
-: эндотермической реакции
-: увеличения объема
+: уменьшения объема
I: 02.21;
S: При добавлении в реакционную смесь продуктов реакции равновесие смещается…
-: в сторону продуктов
+:в сторону исходных веществ
-: не достаточно данных для ответа
-: положение равновесия не изменяется
I: 02.22;
S: При добавлении в реакционную смесь исходных веществ равновесие смещается…
+: в сторону продуктов
-: в сторону исходных веществ
-: не достаточно данных для ответа
-: положение равновесия не изменяется
I: 02.23;
S: Равновесие реакции 2H2(г)+O2(г) 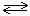 2H2O(г) ; DH<0 смещается влево при:
2H2O(г) ; DH<0 смещается влево при:
-: понижении температуры
+: увеличении давления
-: уменьшении давления
-:увеличении концентрации O2
I: 02.24;
S:Математическое выражение для константы равновесия химической реакции
2H2 (г) + CO (г.) Û CH3OH (г.) имеет вид:
-: 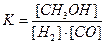
-: 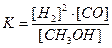
+: 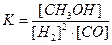
-: 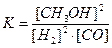
I: 02.25;
S: Математическое выражение для константы равновесия химической реакции
3H2 (г) + N2 (г.) Û 2NH3 (г.) имеет вид:
-: 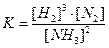
+: 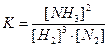
-: 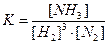
-: 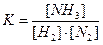
I: 02.26;
S: В какую сторону сместится равновесие реакции CaCO3(т) 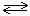 CaO(т)+CO2(г) при повышении давления?
CaO(т)+CO2(г) при повышении давления?
-: вправо
+: влево
-:не сместится
-: недостаточно данных для ответа
I: 02.27;
S: Равновесие реакции 4HCl(г)+O2(г) 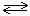 2H2O(г)+2Cl2(г) ; DH>0 смещается вправо при:
2H2O(г)+2Cl2(г) ; DH>0 смещается вправо при:
-: увеличении объема
+: уменьшении объема
-: понижении температуры
-: увеличении концентрации H2O
I: 02.28;
S: Равновесие реакции Fe3O4(т)+4CO(г) 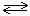 3Fe(т) +4CO2(г) ; DH<0 смещается влево при:
3Fe(т) +4CO2(г) ; DH<0 смещается влево при:
-: понижении температуры
+: повышении температуры
-: уменьшении давления
-: увеличении давления
I: 02.29;
S: При увеличении концентрации водорода в ###раз скорость реакции
N2(г)+3Н2(г) 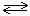 2NН3(г) возросла в 216 раз
2NН3(г) возросла в 216 раз
+: 6
I: 02.30;
S: При увеличении температуры от 270 до 470 скорость реакции возрастет в ### раз (g=3)
+: 9
-: 27
-: 81
-: 16
I: 02.31;
S Равновесие реакции H2(г)+S(т) 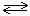 H2S(г) ; DH>0 смещается влево при:
H2S(г) ; DH>0 смещается влево при:
-: увеличении температуры
-: уменьшении давления
+: увеличении концентрации H2S
-: увеличении концентрации H2
I: 02.32;
S: Cкорость прямой реакции N2(г)+3Н2(г) 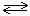 2NН3(г) возросла в 256 раз при увеличении давления в###раза
2NН3(г) возросла в 256 раз при увеличении давления в###раза
+: 4
I: 02.33;
S: Cкорость реакции 2SO2(г)+O2(г) 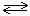 2SO3(г) возросла в 100 раз при увеличении концентрацию диоксида серы в### раз
2SO3(г) возросла в 100 раз при увеличении концентрацию диоксида серы в### раз
+: 10
V2: 01. Дисперсные системы
I: 01. 01;
S: Туман представляет собой распределение мельчайших частиц:
-: твердого вещества в газе
+: жидкости в газе
-: газа в газе
-: жидкости в жидкости
I: 01.02;
S: Суспензиями называются такие дисперсные системы, в которых:
-: газообразные частицы распределены в жидкости
-: газообразные частицы распределены в газе
-: одна жидкость раздроблена в другой не растворяющей ее жидкости
+: твердые частицы распределены в жидкости
I:01.03;
S: Эмульсиями называются дисперсные системы, в которых:
-: газообразные частицы распределены в жидкости
-: газообразные частицы распределены в газе
+: одна жидкость раздроблена в другой не растворяющей ее жидкости
-: твердые частицы распределены в жидкости
I: 01.04;
S: В лабораторных условиях растворитель можно отделить от растворенного вещества:
-: декантацией
+: перегонкой
-: фильтрованием
-: отстаиванием
I: 01.05;
S: В лабораторных условиях смесь мела и воды можно разделить:
-: экстракцией
-: перегонкой
+: фильтрованием
-: перекристаллизацией
I: 01.06;
S: В истинных растворах размер растворенных частиц колеблется в пределах (см):
-: 1 – 10-2
-: 10-2 – 10-5
-: 10-5 – 10-7
+: 10-7 – 10-8
I: 01.07;
S: В коллоидных системах размер растворенных частиц колеблется в пределах (см):
-: 1 – 10-2
-: 10-2 – 10-5
+: 10-5 – 10-7
-: 10-7 – 10-8
I: 01.08;
S; Температуру кипения жидкости можно повысить, если:
+: добавить поваренной соли в воду
-: накрыть стакан с водой крышкой
-: увеличить пламя газовой горелки
-: уменьшить пламя газовой горелки
I: 01.09;
S: При посыпании обледенелой дороги хлоридом натрия, лед тает потому что:
-: образуется раствор, температура замерзания которого выше, чем у растворителя
+: образуется раствор, температура замерзания которого ниже, чем у растворителя
-: происходит выделение теплоты
-: происходит поглощение теплоты
I: 01.10;
S: Раствор над осадком, полученным через несколько недель после того как KCl оставили в склянке, является:
-: разбавленным
+: насыщенным
-: перенасыщенным
-: ненасыщенным
V2: 04. Гидролиз солей
I: 04.01;
S: Концентрация (моль/л) ионов водорода [Н+] в 0,01М растворе HCl при полной ее диссоциации равна:
-: 2
-: 1·10-1
+: 1·10-2
-: 2·10-2
I: 04.02;
S: Концентрация (моль/л) ионов водорода [Н+] в 0,1М растворе HNO3 при полной ее диссоциации равна:
-: 1
+: 1·10-1
-: 1·10-2
-: 2·10-2
I: 04.03;
S: Значение рН раствора полностью ионизированой 0,01М азотной кислоты равно:
-: 1
+: 2
-: 10
-: 12
I: 04.04
S: Значение рН раствора полностью ионизированого 0,01М гидроксида натрия равно:
-: 1
-: 2
-: 10
+: 12
I: 04.05;
S: Концентрация (моль/л) ионов водорода в растворе, имеющем значение рН = 5,0 равна:
-: 1·10-14
-: 5
+: 1·10-5
-: 9
I: 04.06
S: Концентрация (моль/л) ионов водорода в растворе, имеющем значение рН = 9,0 равна:
+: 1·10-9
-: 5
-: 1·10-14
-: 9
I: 04.07;
S: В растворе нитрата алюминия среда будет:
-: щелочной
-: нейтральной
+: кислой
-: близкой к нейтральной
I: 04.08;
S: В растворе карбоната калия среда будет:
+: щелочной
-: нейтральной
-: кислой
-: близкой к нейтральной
I: 04.09;
S: В растворе нитрата натрия среда будет:
-: щелочной
+: нейтральной
-: кислой
-: близкой к нейтральной
I: 04.10;
S: Щелочную реакцию среды будет показывать следующий раствор:
-: хлорид натрия, NaCl
-: хлороводород, HCl
+: карбонат натрия, Na2CO3
-: хлорид аммония, NH4Cl
I: 04.11;
S: Кислую реакцию среды будет показывать следующий раствор:
-: хлорид натрия, NaCl
+: хлороводород, HCl
-: карбонат натрия, Na2CO3
-: хлорид аммония, NH4ОН
I: 04.12;
S: Нейтральную реакцию среды будет показывать следующий раствор:
+: хлорид натрия, NaCl
-: хлороводород, HCl
-: карбонат натрия, Na2CO3
-: хлорид аммония, NH4Cl
I: 04.13;
S: В водном растворе кислую реакцию дает:
-: CH3COONa
+: NH4Cl
-: Na2CO3
-: Na2HPO4
I: 04.14;
S: Чтобы ослабить или прекратить гидролиз раствора хлорида железа (III), необходимо немного добавить:
+: соляной кислоты
-: гидроксида кальция
-: твердой соли NaCl
-: дистиллированной воды
I: 04.15;
S: Усилить гидролиз хлорида алюминия можно добавлением к его раствору:
-: HCl
-: NaCl
+: NaOН
-: NH4Cl
I: 04.16;
S: В результате гидролиза в водном растворе полностью разлагается соль:
-: Na2CO3
+: Al2S3
-: Na2S
-: (NH4)2SO4
I: 04.17;
S: Временная жесткость воды обусловлена присутствием:
+: Ca(HCO3)2, Mg(HCO3)2
-: Na2SO4, K2SO4
-: Na2CO3, Na3PO4
-: CaCl2, MgCl2
I: 04.18;
S: Постоянная жесткость воды обусловлена присутствием:
-: Ca(HCO3)2, Mg(HCO3)2
-: Na2SO4, K2SO4
-: Na2CO3, Na3PO4
+: CaCl2, MgCl2
I: 04.19;
S: Индикатор фенолфталеин в щелочной среде имеет окраску:
-: оранжевую
-: желтую
+: малиновую
-: синюю
I: 04.20;
S: Индикатор лакмус в щелочной среде имеет окраску:
+: синюю
-: фиолетовую
-: желтую
-: красную
V1: 04. СТРОЕНИЕ ВЕЩЕСТВА
V1: 05. ЭЛЕКТРОХИМИЯ
V2: 03. Электролиз
I: 03.01;
S: Металлом, который нельзя получить электролизом водного раствора его соли, является ###
+: Na
-: Ag
-: Сu
-: Ni
I: 03.02;
S: Продуктами, выделяющимися на инертных электродах (катоде и аноде) при электролизе водного раствора сульфата меди, являются ###
-: Cu и SO3
-: Н2 и О2
-: Сu и H2S
+: Сu и О2
I: 03.03;
S: Продуктами, выделяющимися на инертных электродах (катоде и аноде) при электролизе водного раствора хлорида никеля, являются ###
-: Ni и Cl2
+: Ni, H2 и Cl2
-: Ni и О2
-: Ni, H2 и O2
I: 03.04;
S: Продуктами, выделяющимися на инертных электродах (катоде и аноде) при электролизе водного раствора сульфата никеля, являются ###
-: Ni и SO3
-: Ni, H2 и SO3
-: Ni и О2
+: Ni, H2 и O2
I: 03.05;
S: Продуктами, выделяющимися на инертных электродах (катоде и аноде) при электролизе водного раствора сульфата натрия, являются ###
-: Na и SO2
-: H2 и S
-: Na и О2
+: Н2 и О2
I: 03.06;
S: При электролизе водного раствора сульфата натрия на катоде протекает реакция ###
-: Na+ + e– = Na
+: 2Н2О + 2e– = Н2 + 2ОН–
-: 4ОН– – 4e– = О2 + 2Н2О
-: 2Н+ + 2e– = Н2
I: 03.07;
S: При электролизе водного раствора сульфата натрия на инертном аноде протекает реакция ###
-: Na+ + e– = Na
-: 2Н2О + 2e– = Н2 + 2ОН–
-: 4ОН– – 4e– = О2 + 2Н2О
+: 2Н2О – 4e– = О2 + 4H+
I: 03.08;
S: Уравнение процесса, протекающего на катоде при электролизе водного раствора йодида калия, имеет вид ###
-: 2Н2О – 4e– = О2 + 4H+
-: К+ + e– = К0
-: О2 + 2Н2О + 4e– = 4ОН–
+: 2Н2О + 2e– = Н2+2ОН–
I: 03.09;
S: Уравнение процесса, протекающего на катоде при электролизе расплава йодида калия, имеет вид ###
-: 2Н2О – 4e– = О2 + 4H+
+: К+ + e– = К0
-: О2 + 2Н2О + 4e– = 4ОН–
-: 2Н2О + 2e– = Н2+2ОН–
I: 03.10;
S: Уравнение процесса, протекающего на катоде при электролизе водного раствора нитрата серебра, имеет вид ###
-: 2NO3– – 2e– = 2NO2 + O2
-: 2Н2О + 2e– = Н2 + 2ОН–
+: Ag+ + e– = Ag
-: 2Н+ + 2e– = Н2
I: 03.11;
S: Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора нитрата серебра, имеет вид ###
-: 2NO3– – 2e– = 2NO2 + O2
+: 2H2O – 4e – = O2 + 4H+
-: Ag+ + e– = Ag
-: 2Н+ + 2e– = Н2
I: 03.12;
S: Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора йодида калия, имеет вид ###
+: 2I – – 2e – = I2
-: 2H2O – 4e – = O2 + 4H+
-: O2 + 2H2O + 4e – = 4OH–
-: 4OH – – 4e – = 4OH –
I: 03.13;
S: Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора хлорида натрия, имеет вид ###
-: O2 + 2H2O + 4e – = 4OH–
-: 2H2O – 4e – = O2 + 4H+
-: 4OH – – 4e – = 4OH –
+: 2Cl – – 2e – = Cl2
I: 03.14;
S: Уравнение процесса, протекающего на катоде при электролизе водного раствора хлорида натрия, имеет вид ###
+: 2Н2О + 2e– = Н2 + 2ОН–
-: 2H2O – 4e – = O2 + 4H+
-: Na+ + e– = Na
-: 2Cl – – 2e – = Cl2
I: 03.15;
S: Уравнение процесса, протекающего на катоде при электролизе расплава хлорида натрия, имеет вид ###
-: Н2О + 2e– = Н2 + 2ОН–
+: Na+ + e– = Na
-: O2 + 2H2O + 4e – = 4OH–
-: 2Cl – – 2e – = Cl2
I: 03.16;
S: Для получения 54 г серебра электролизом водного раствора нитрата серебра (выход по току 100%) необходимо, чтобы в растворе содержалось ### граммов чистой соли
42,5
+: 85
I: 03.17;
S: При электролизе раствора сульфата меди в течение одного часа при силе тока 4 А на катоде выделилось ### граммов меди (с точностью до 0,1)
+: 4,7
I: 03.18;
S: При электролизе раствора нитрата серебра в течение четырех часов при силе тока 2 А на катоде выделилось ### граммов серебра (с точностью до 0,1)
+: 32,2
I: 03.19;
S: При электролизе раствора сульфата калия в течение трех часов при силе тока 5 А разложилось ### воды (с точностью до 0,01)
+: 5,03
I: 03.20;
S: При электролизе раствора сульфата натрия в течение пяти часов при силе тока 7 А разложилось ### воды (с точностью до 0,01)
+: 11,75
V2: 04. Коррозия
I: 04.01;
S: Для защиты железных изделий от коррозии в качестве анодного покрытия используют ###
+: цинк
-: серебро
-: медь
-: олово
I: 04.02;
S: Дня защиты медных изделий от коррозии в качестве анодного покрытия можно использовать ###
-: Аu
-: Pt
+: А1
-: Ag
I: 04.03;
S: Для защиты медных изделий от коррозии в качестве катодного покрытия можно использовать ###
-: Ni
-: Сг
-: Sn
+: Ag
I: 04.04;
S: Для защиты от коррозии стального изделия в качестве анодного покрытия может быть использован ###
-: никель
+: хром
-: медь
-: свинец
I: 04.05;
S: При нарушении оловянного покрытия на железном изделии, находящемся в кислой среде, на аноде будет протекать реакция ###
-: Sn0 – 2e- = Sn2+
+: Fe0 – 2e- = Fe2+
-: Sn2+ + 2e- = Sn0
-: 2Н+ + 2e- = Н2
I: 04.06;
S: При нарушении оловянного покрытия на железном изделии, находящемся в кислой среде, на катоде будет протекать реакция ###
-: Sn0 – 2e- = Sn2+
-: Fe0 – 2e- = Fe2+
-: Sn2+ + 2e- = Sn0
+: 2Н+ + 2e- = Н2
I: 04.07;
S: При нарушении оловянного покрытия на железном изделии, находящемся в нейтральной среде, на аноде будет протекать реакция ###
-: Sn0 – 2e- = Sn2+
+: Fe0 – 2e- = Fe2+
-: Sn2+ + 2e- = Sn0
-: 2Н2O + O2 + 4e- = 4OH–
I: 04.08;
S: При нарушении оловянного покрытия на железном изделии, находящемся в кислой среде, на катоде будет протекать реакция ###
-: Sn0 – 2e- = Sn2+
-: Fe0 – 2e- = Fe2+
-: Sn2+ + 2e- = Sn0
+: 2Н2O + O2 + 4e- = 4OH–
I: 04.09;
S: При нарушении цинкового покрытия на железном изделии, находящемся в кислой среде, на аноде будет протекать реакция ###
+: Zn0 – 2e- = Zn2+
-: Fe0 – 2e- = Fe2+
-: Zn2+ + 2e- = Zn0
-: 2Н+ + 2e- = Н2
I: 04.10;
S: При нарушении цинкового покрытия на железном изделии, находящемся в кислой среде, на катоде будет протекать реакция ###
-: Zn0 – 2e- = Zn2+
-: Fe0 – 2e- = Fe2+
-: Zn2+ + 2e- = Zn0
+: 2Н+ + 2e- = Н2
I: 04.11;
S: При нарушении цинкового покрытия на железном изделии, находящемся в нейтральной среде, на аноде будет протекать реакция ###
+: Zn0 – 2e- = Zn2+
-: Fe0 – 2e- = Fe2+
-: Zn2+ + 2e- = Zn0
-: 2Н2O + O2 + 4e- = 4OH–
I: 04.12;
S: При нарушении цинкового покрытия на железном изделии, находящемся в нейтральной среде, на катоде будет протекать реакция ###
-: Zn0 – 2e- = Zn2+
-: Fe0 – 2e- = Fe2+
-: Zn2+ + 2e- = Zn0
+: 2Н2O + O2 + 4e- = 4OH–
I: 04.13;
S: При нарушении никелевого покрытия на железном изделии, находящемся в нейтральной среде, на аноде будет протекать реакция ###
-: Ni0 – 2e- = Ni2+
+: Fe0 – 2e- = Fe2+
-: Ni2+ + 2e- = Ni0
-: 2Н2O + O2 + 4e- = 4OH–
I: 04.14;
S: При нарушении никелевого покрытия на железном изделии, находящемся в нейтральной среде, на катоде будет протекать реакция ###
-: Ni0 – 2e- = Ni2+
-: Fe0 – 2e- = Fe2+
-: Ni2+ + 2e- = Ni0
+: 2Н2O + O2 + 4e- = 4OH–
I: 04.15;
S: При нарушении никелевого покрытия на железном изделии, находящемся в кислой среде, на аноде будет протекать реакция ###
-: Ni0 – 2e- = Ni2+
+: Fe0 – 2e- = Fe2+
-: Ni2+ + 2e- = Ni0
-: 2Н+ + 2e- = Н2
I: 04.16;
S: При нарушении никелевого покрытия на железном изделии, находящемся в кислой среде, на катоде будет протекать реакция ###
-: Ni0 – 2e- = Ni2+
-: Fe0 – 2e- = Fe2+
-: Ni2+ + 2e- = Ni0
+: 2Н+ + 2e- = Н2
V2:01. Органическая химия
I: 01.01;
S: Из указанных соединений к классу спиртов относится:
+: С2H5OH
-: С2H5Cl
-: СН4
-: С2H5NO2
I:01.02;
S: Из указанных соединений к классу карбоновых кислот относится:
-: С2H5NH2
+: CH3COOH
-: СН4
-: С2H5NO2
I:01.03;
S: Из указанных соединений к классу алканов относится:
+: С2H6
-: С2H5Br
-: CH3COOH
-: С2H5NO2
I:01.04;
S: Из указанных соединений к классу нитросоединений относится:
+: С2H5NO2
-: С2H6
-: С2H5Br,
-: СН3Cl
I:01.05;
S: Из указанных соединений к ароматическим относится:
-: вода
+: бензол
-: сероводород
-: метан
I:01.06;
S: Из указанных соединений к классу кетонов относится:
-: диоксан
+: диоктилкетон
-: метан
-: толуол
I:01.07;
S: Соединение С2H5OH относится к классу:
+: спиртов
-: предельных углеводородов
-: аминов
-: галогенпроизводных
I: 01.08;
S: Соединение С5H10 относится к классу:
+: алкенов
-: аминов
-: спиртов
-: альдегидов
I:01.09;
S: Соединение С6H5OH относится к классу:
+: фенолов
-: алкинов
-: алканов
-: алкенов
I:01.10;
S: Соединение СH2=СH–СН=СН2 относится к классу:
-: карбоновых кислот
+: диеновых углеводородов
-: спиртов
-: нитросоединений
I:01.11;
S: Соединение СH2=СH2 относится к классу:
+: алкенов
-: ароматических соединений,
-: полимеров
-: галогенопроизводных
I:01.12;
S: Соединение СH≡СH относится к классу:
-: галогенпроизводных
+: алкинов
-: карбоновых кислот
-: аминокислот
I:01.13;
S: Соединение СH3–СH3 относится к классу:
-: аминокислот
-: полимеров
+: алканов
-: галогенпроизводных
I:01.14;
S: Этаноламин относится к классу
-: галогенпроизводных
+: аминопроизводных
-: полимеров
-: алкенов
I:01.15;
S: Уксусная кислота относится к классу:
-: галогенпроизводных
-: спиртов
+: карбоновых кислот
-: алкенов
I: 01.16;
S: Хлорметан относится к классу:
-: аминопроизводных
-: полимеров
+: галогенпроизводных
-: спиртов
I:01.17;
S: Соединение С2Н5Сl относится к классу
+: галогенпроизводных
-: нитросоединений
-: аминокислот
-: альдегидов
I:01.18;
S: Качественная реакция на альдегиды
+: серебряного зеркала
-: гидрирования
-: галогенирования
-: гидрогалогенирования
I:01.19;
S: В виде цис-транс-изомеров может существовать соединение
-: этан
-: нитроэтан,
+: бутен-2
-: этанол
I:01.20;
S: В виде цис-транс-изомеров может существовать соединение
-: метан
-: этан
-: пропан
+: бутен-2
I:01.21;
S: В виде цис-транс-изомеров может существовать соединение
+: СHCl=СHCl
-: СH2Cl–СH2Cl
-: СH3–СH2–СН3
-: СHСl2–СHCl2
I:01.22;
S: Углерод в предельных углеводородах находится в состоянии
+: sp3-гибризизации
-: sp2-гибризизации
-: sp-гибридизации
-: d2sp3-гибризизации
I:01.23;
S: Валентный угол в молекуле метана СН4 равен
+: 109°
-: 90°
-: 180°
-: 120°
I:01.24;
S: В молекуле ацетилена СH≡СH атом углерода находится в состоянии
-: sp3-гибризизации
-: sp2-гибризизации
+: sp-гибридизации
-: d2sp3-гибризизации
I:01.25;
S: В молекуле этилена СH2=СH2 атом углерода находится в состоянии
-: sp3-гибризизации
+: sp2-гибризизации
-: sp-гибридизации
-: d2sp3-гибризизации
I:01.26;
S: Радикал –СН3 называется
-: бутил
-: октил
-: винил
+: метил
I:01.27;
S: В состав аминов входит функциональная группа
-: –OH
+: –NH2
-: –Cl
-: –SO3
I:01.28;
S: В состав спиртов входит функциональная группа
+: –OH
-: –NH2
-: –Cl
-: –SO3
I:01.29;
S: В состав карбоновых кислот входит функциональная группа
-: –OH
-: –NH2
+: –СООН
-: –SO3
I:01.30;
S: В молекуле бензола атом углерода находится в состоянии
-: d2sp3-гибризизации
-: sp3-гибризизации;
+: sp2-гибризизации
-: sp-гибридизации
I:01.31;
S: Гомологами являются
+: пропан и пентан
-: пропан и циклопропан
-: пентан и пентен
-: циклопропан и пропен
I: 01.32;
S: Две π - связи имеются в молекуле
-: СН4
-: СН2=СН2
-: СН3 – СН 2– СН3
+: СН≡С–СН3
I:01.33;
S: Гомологами являются
-: бутан и циклобутан
+: бутен и пропен
-: бензол и этанол
-: этан и этен
I:01.34;
S: К одноатомным предельным спиртам относится
-: фенол
-: стирол
+: этанол
-: бензол
I:01.35;
S: Молекула метана СН4 имеет форму
+: тетраэдра
-: угловую
-: линейную
-: октаэдра
I:01.36;
S: Степень окисления углерода в хлорметане СН3Сl равна:
-: +2
-: +4
+: –2
-:–4
I:01.37;
S: Степень окисления углерода в бромметане СН3Br равна:
-: +2
-: +4
+: –2
-: –4
I:01.38;
S: Ацетилен может быть получен реакцией воды с
-:этиленом
+: карбидом
-: этаном
-: бензолом
I: 01.39;
S: Бромная вода обесцвечивается при действии
-: этана
+: этилена
-: этанола
-: уксусной кислоты
V1: 01. ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ
