Второе и третье начала термодинамики
Второе начало термодинамики: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает (закон возрастания энтропии).
Если первое начало термодинамики выражает закон сохранения и превращения энергии применительно к термодинамическим процессам безотносительно их направления, то второе начало термодинамики определяет направление протекания термодинамических процессов, указывая, какие процессы в природе возможны, а какие - нет.
Существуют ещё две формулировки второго начала термодинамики:
1) по Кельвину:невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к телу более нагретому.
Третье начало термодинамики - теорема Нернста-Планка - постулирует поведение термодинамических систем при нуле Кельвина: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина:
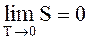 .
.
Тепловые двигатели и холодильные машины
Тепловой двигатель - это периодически действующий двигатель, совершающий работу за счет полученной извне теплоты.
Термостатом называется термодинамическая система, которая может обмениваться теплотой с телами практически без изменения собственной температуры.
Рабочее тело - это тело (газ или пар), совершающее круговой процесс и обменивающееся энергией с другими телами.
Принцип работы теплового двигателя: от термостата с более высокой температурой 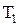 , называемого нагревателем, за цикл отнимается количество теплоты
, называемого нагревателем, за цикл отнимается количество теплоты 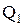 , а термостату с более низкой температурой
, а термостату с более низкой температурой 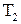 , называемому холодильником, за цикл передается количество теплоты
, называемому холодильником, за цикл передается количество теплоты 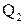 . При этом рабочее тело расширяется и совершает работу
. При этом рабочее тело расширяется и совершает работу 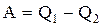 (рис.18).
(рис.18).
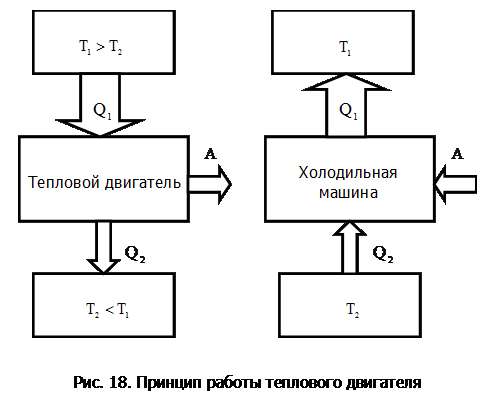
Термический КПД двигателя:
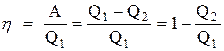
Чтобы КПД был равен 1, необходимо, чтобы 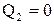 , а это запрещено
, а это запрещено
вторым началом термодинамики.
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине: от термостата с более низкой температурой 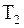 за цикл отнимается количество теплоты
за цикл отнимается количество теплоты 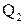 и отдается термостату с более высокой температурой
и отдается термостату с более высокой температурой 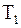 . При этом
. При этом 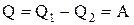 или
или 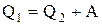 .
.
Количество теплоты 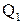 , отданное системой термостату
, отданное системой термостату 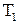 , больше количества теплоты
, больше количества теплоты 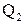 , полученного от термостата
, полученного от термостата 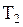 , на величину работы, совершенной над системой.
, на величину работы, совершенной над системой.
Эффективность холодильной машины характеризует холодильный коэффициент 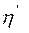 - отношение отнятой от термостата с более низкой температурой количества теплоты
- отношение отнятой от термостата с более низкой температурой количества теплоты 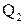 к работе
к работе 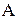 , которая затрачивается на приведение холодильной машины в действие:
, которая затрачивается на приведение холодильной машины в действие:
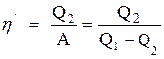 .
.
Теорема Карно
Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей  и холодильников
и холодильников  , наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
, наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
|
 Для построения рабочего цикла использует обратимые процессы. Например, цикл Карно состоит из двух изотерм (1–2, 2-4), в которых теплота полностью превращается в работу, и двух адиабат (2-3, 4–1), в которых изменение внутренней энергии полностью превращаются в работу (рис. 19).
Для построения рабочего цикла использует обратимые процессы. Например, цикл Карно состоит из двух изотерм (1–2, 2-4), в которых теплота полностью превращается в работу, и двух адиабат (2-3, 4–1), в которых изменение внутренней энергии полностью превращаются в работу (рис. 19). Рассмотрим изменение энтропии рабочего тела. Общее изменение энтропии в цикле: 
Так как мы рассматриваем только обратимые процессы, общее изменение энтропии  .
.
Последовательные термодинамические процессы в цикле Карно:
| Процесс | Работа | Изменение энтропии | Наблюдается |
Изотермическое расширение 1—2  |  |  | тело принимает теплоту |
Адиабатическое расширение 2—3  ; ;  |  |  | охлаждение до  |
изотермическое сжатие 3-4  |  |  | тело отдает теплоту |
адиабатическое сжатие  ; ;  |  |  | восстановление начального состояния  |
Общее изменение энтропии в равновесном цикле:  , поэтому:
, поэтому:  -максимальный КПД теплового двигателя.
-максимальный КПД теплового двигателя.
Следствия:
1. КПД цикла Карно не зависит от рода рабочего тела.
2. КПД определяется только разницей температур нагревателя и холодильника.
3. КПД не может быть 100% даже у идеальной тепловой машины, так как при этом температура холодильника должна быть  , что запрещено законами квантовой механики и третьим законом термодинамики.
, что запрещено законами квантовой механики и третьим законом термодинамики.
4. Невозможно создать вечный двигатель второго рода, работающий в тепловом равновесии без перепада температур, т.е. при  , так как в этом случае
, так как в этом случае  .
.
Тепловые двигатели повышают энтропию замкнутой системы.
РЕАЛЬНЫЕ ГАЗЫ
Уравнение Ван-дер-Ваальса
Как показывают эксперименты, модель идеального газа позволяет описывать поведение разреженных реальных газов лишь при «нормальных» условиях, т.е. при достаточно низком давлении и высокой температуре. При высоких давлениях, или низких температурах уравнение состояния дает большие расхождения с результатами экспериментов.
При выводе уравнения состояния идеального газа не учитывались размеры молекул и потенциальная энергия их взаимодействия. Поэтому физическая природа газа не играла никакой роли и уравнение состояния универсально и применимо ко всем газам. Повышение давления приводит к уменьшению среднего расстояния между молекулами, значит, необходимо учитывать объем молекул и взаимодействие между ними.
Учитывая собственный объем молекул и силы межмолекулярного взаимодействия, Ван-дер-Ваальс вывел уравнение состояния реального газа, введя в уравнение Клапейрона-Менделеева две поправки.
1. Учет собственного объема молекул.
Для движения молекул предоставлен не весь объем  , занимаемый газом, а меньший на величину объема всех молекул газа ‑
, занимаемый газом, а меньший на величину объема всех молекул газа ‑  , где
, где  ‑ суммарный объем молекул газа,
‑ суммарный объем молекул газа,  - молярный объем. Расчеты показывают, что константа
- молярный объем. Расчеты показывают, что константа  численно равна учетверенному объему молекул, содержащихся в моле газа. Размерность поправки
численно равна учетверенному объему молекул, содержащихся в моле газа. Размерность поправки  .
.
2.Учет притяжения молекул.
Действие сил притяжения молекул газа приводит к появлению дополнительного давления на газ, называемого внутренним давлением. Внутреннее давление  равно
равно
 ,
,
где  – постоянная Ван-дер-Ваальса, характеризующая силы притяжения молекул. Размерность коэффициента:
– постоянная Ван-дер-Ваальса, характеризующая силы притяжения молекул. Размерность коэффициента:  .
.
Вводя эти поправки, получим уравнение Ван-дер-Ваальса для моля газа (уравнение состояния реальных газов):
 (23)
(23)
Для произвольного количества вещества  газа с учетом того, что
газа с учетом того, что  , уравнение (23) имеет вид:
, уравнение (23) имеет вид:

где поправки  и
и  - постоянные для каждого газа величины, определяемые опытным путем.
- постоянные для каждого газа величины, определяемые опытным путем.

