Замещение гидроксильных групп спиртов
При кипячении спиртов с концентрированными галогенводородными кислотами получают галогенпроизводные по обратимому процессу.
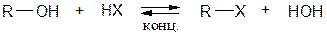
Легче идет реакция с HI, труднее с HCl.
Из спиртов наиболее реакционоспособны третичные.
В лабораторных условиях вместо концентрированных кислот используют галоген-ангидриды фосфорной или серной кислот и карбоновых кислот.
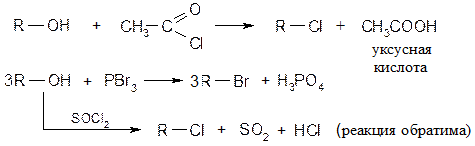
Закономерности реакций нуклеофильного замещения
у насыщенного атома водорода
| № п/п | SN1 мономолекулярный | SN2 бимолекулярный | SNi |
| 1. Механизм |  | 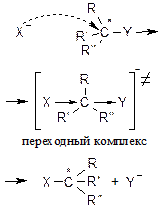 |  |
| 2. Кинетика | 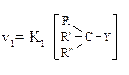 Мономолекулярное замещение (скорость реакции зависит от концентрации одного компонента - субстрата) Мономолекулярное замещение (скорость реакции зависит от концентрации одного компонента - субстрата) | 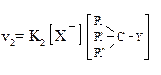 Бимолекулярное замещение (в кинетическом уравнении – концентрации и реагента и субстрата) Бимолекулярное замещение (в кинетическом уравнении – концентрации и реагента и субстрата) | 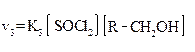 Реакция характерна только для замещения гидроксильных групп спиртов. Реакция характерна только для замещения гидроксильных групп спиртов. |
| 3. Стереохимия | SN1 - правило: рацемизация (или частичное обращение конфигурации) | SN2 - правило: обращение конфигурации (подход реагента с противоположной стороны по отношению к уходящей группе) | SNi - правило: полное сохранение конфигурации (атака со стороны уходящей группы) |
| 4. Влияние растворителя | Реакция облегчается полярными растворителями, как нуклеофильного (вода, спирты), так и электрофильного характера: бензол с акцепторными группами 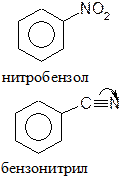 | Умеренное влияние растворителя; реакции способствуют растворители, связывающие электрофильную часть молекулы (облегчают подход и уход заряженной частицы - апротонные, нуклеофильные растворители). Например, простые эфиры, нитрилы, амины. | Растворители не влияют на скорость и стереохимию процесса. |
| 5. Влияние эффектов заместителей | Относительно слабое влияние пространственных эффектов, но сильное влияние эффектов сопряжения C2H5 v=1 CH3-Br v=0,8 (CH3)2CH-Br v=11,6 (CH3)3C-Br v=1,2·106 | Преобладающее влияние пространственных эффектов C2H5 v=1 CH3-Br v=145 (CH3)2CH-Br v=0,078 (CH3)3CH-Br v=0,00051 | Слабое влияние пространственных эффектов, значительное влияние полярных эффектов |
| Относительная скорость реакции | При прочих равных условиях скорости реакций нуклеофильного замещения, как правило, уменьшаются в ряду: третичные > вторичные > первичные. | ||
| 6. Влияние характера замещающих групп | Скорость реакции тем быстрее, чем беднее энергией уходящая группа (чем стабильнее уходящая группа). Это обусловлено энергией связи C-Y в первую очередь и C-X во вторую очередь. Для галогенов самая богатая энергией группа Clˉ, самая бедная - Iˉ. | ||
| 7. Влияние характера реагентов | Предпочтительнее реакция с более электроотрицательным реагентом, имеющим значительное сродство к электрону. | Предпочтительнее реакция с более нуклеофильным реагентом (способность образовывать связи с атомом углерода - нуклеофильность). | Нет влияния |
| 8. Побочные реакции | Отщепления по механизму E1, перегруппировки углеродного скелета | Отщепления по механизму E2 | Нет |
Примечания:
Как следует из графы 8 таблицы, реакции SN и E являются конкурирующими. Например, после образования карбокатиона [SN1] возможны два пути дальнейшего процесса – образование продукта замещения (Х- нуклеофил), или продукта отщепления (Х- основание):
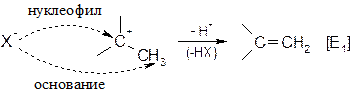
Подобная реакция возможна и по бимолекулярному механизму [SN2]:
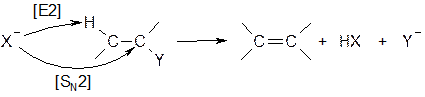
Для перегруппировки необходимо образование первичного или вторичного карбокатиона:

Практически нет реакций, которые бы протекали исключительно по одному из представленных механизмов SN1, SN2. Поэтому можно говорить лишь о преимущественном протекании реакции по тому или иному механизму. Так, первичные производные реагируют в основном по механизму SN2, третичные - по механизму SN1, вторичные - либо по SN1, либо по SN2 (в зависимости от строения молекулы).
