Биологическая очистка сточных вод.
Этот метод является наиболее распространенным и относительно недорогим способом очистки СВ от большинства органических примесей. Очистные сооружения стационарного типа применяются для очистки стоков городов, крупных предприятий. Локальные установки применяются на судах (в основном пассажирских).
Метод основан на способности микроорганизмов потреблять органические вещества из СВ в качестве пищи. При этом происходит окисление и восстановление органических соединений с образованием безвредных оксидов азота, углерода и др. Чаще применяют аэробные бактерии, окисляющие органику, поэтому для осуществления процесса требуется подача воздуха или кислорода.
Процесс биоокисления можно разделить на две стадии:
1. масса – передача органических веществ и кислорода из
объема СВ к поверхности клеток микробов.
2. диффузия кислорода и органических соединений через клеточную мембрану, их окисление и синтез клеточного вещества. Например, окисление нитросоединений протекает по реакции:
фермент
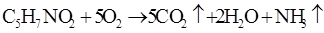
Сообщества микроорганизмов, применяемых в биоочистке, образуют так называемый «активный ил». Этот ил имеет очень развитую поверхность, около 100 н 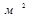 а 1г сухого вещества. Интенсивность жизнедеятельности организмов, а, следовательно, и процесс окисления зависит от концентрации кислорода, рН среды, температуры, величины окислительно-восстановительного потенциала и ряда других факторов. Для биоочистки наибольшее распространение получили аэроционные сооружения (аэротанки) и биофильтры. В последнее время начали применятся малогабаритные установки.
а 1г сухого вещества. Интенсивность жизнедеятельности организмов, а, следовательно, и процесс окисления зависит от концентрации кислорода, рН среды, температуры, величины окислительно-восстановительного потенциала и ряда других факторов. Для биоочистки наибольшее распространение получили аэроционные сооружения (аэротанки) и биофильтры. В последнее время начали применятся малогабаритные установки.
Список литературы
1. Глинка Н. А. Общая химия под редакцией А. Н. Ерамкова. – М.: Интеграл Пресс, 2000-2007гг. – 728с
2. Коровин Н. В. Общая химия. – М.: Высшая школа, 2004г. – 558с
3. Фролов В. В. Химия. – М.: Высшая школа, 1996г. – 545с
4. Угай Я. А. Общая и неорганическая химия. – М.: Высшая школа, 2004г. – 527с
Содержание
Тема 1. Введение
1.1. Химическое производство и проблемы окружающей среды………........................…3
Тема 2. Химическая термодинамика и кинетика……………………………………….….15
2.1. Внутренняя энергия и энтальпия. Первый закон термодинамики. Закон Гесса. Понятие об энтальпии. Второй закон термодинамики. Энергия Гиббса…………………………………………………………….…………………..15
2.2. Классификация химических реакций в химической кинетике. Гомо- и гетерогенные реакции. Скорость химической реакции. Факторы влияющие на скорость химической реакции. Закон действия масс. Правило Вант –Гоффа…………...………..….…..27
2.3. Обратимые и необратимые реакции. Химическое равновесие. Константа химического равновесия. Принцип Ле Шателье. Гетерогенное равновесие. Фазовые равновесия…………………………………………..……………………….………32
2.4. Механизм химической реакции. Ценные реакции. Фотохимические процессы. Гетерогенный и гомогенный катализ. Каталитические яды.________________35
Тема 3. Растворы………………………………………………………………………..…..40
3.1. Дисперсные системы. Классификация дисперсных систем. Коллоидные растворы. Общие свойство растворов. Способы выражения концентрации. Растворы не электролитов, закон Рауля…………………………………………...…..………...40
3.2. Два вида электролитов: сильные и слабые электролиты. Электролитическая диссоциация в водных растворах. Ионное произведение воды. Водородный показатель……………….……………………………………………………….….48
Тема 4. Окислительно – восстановительные и электрохимические процессы……........51
4.1. Электрохимические процессы. Уравнение Нернста. Водородный электрод. Ряд напряжений. Гальванический элемент……….………………………………...…51
4.2. Электрохимические источники тока………………………………………….…..60
Тема 5. Реакционная способность веществ…………………………………………...….65
5.1. Электронное строение атома квантово-механическая модель атома. Строение многоэлектронных атомов………………………………………………………..65
Тема 6. Химическая идентификация и анализ веществ………………………………...73
6.1. Идентификация катионов и анионов. Количественный анализ:……………......73
6.2. Инструментальные методы анализа……………………………………...……...78
Тема 7. Металлы и неметаллические материалы, применяемые в промышленности………………………………………………………………………..… .83
7.1.Физические и химические свойства металлов. Получение металлов…..................83
7.2. Методы получения полимеров…………………………………………...… …...90
Тема 8. Заключительная лекция…………………………………………………..….… 94
Список литературы…………………………………………………………….….…101
