Генетическая связь между углеводородами и кислородсодержащими органическими веществами
Цель работы – научиться составлять уравнения реакций, отражающих генетическую связь веществ; научиться решать задачи на основе этих уравнений.
Пояснения к работе:
Генетическая связь между углеводородами

Генетическая связь между углеводородами и кислородсодержащими органическими веществами
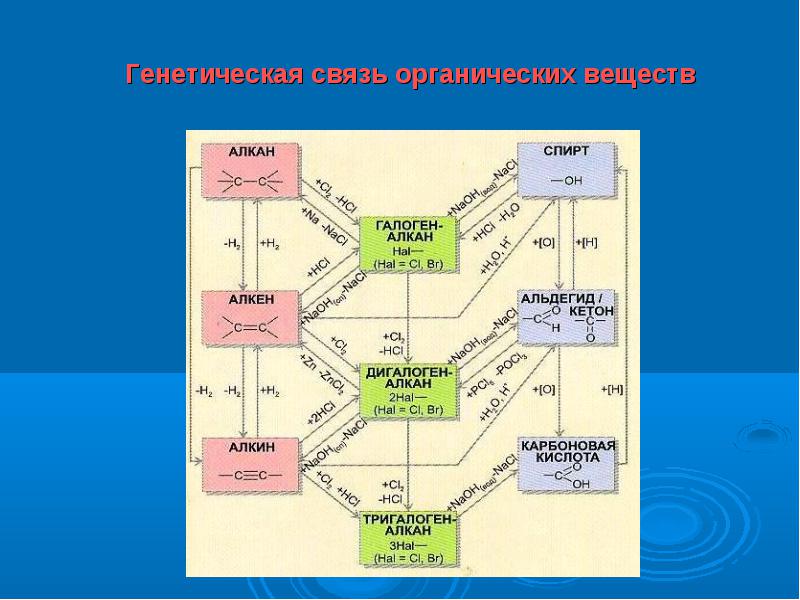
Пояснения к решению задач по химическим уравнениям
1. Определение массы, объема или количества одного вещества по известной величине массы, объема или количества другого вещества.
Задача 1 Определить количество вещества кислорода, необходимое для полного окисления 6 моль диоксида серы (SO2) в триоксид серы(SO3).
Рассуждаем: По условию дано количество диоксида серы (v(SO2) = 6 моль). Запишем уравнение указанной в условии реакции:
2SO2 + О2 = 2SO3
По уравнению мы видим, что в реакции участвуют 2 моль SO2 и 1моль О2.
То есть для взаимодействия с 2моль SO2 необходимо 1моль О2., а по условию для взаимодействия с 6 моль SO2 необходимо неизвестное количество вещества О2. запишем наши рассуждения в форме пропорции:
по условию: 6 моль SO2 – х моль О2
по уравнению: 2 моль SO2 – 1 моль О2
Или:
2/6 = x/1;
Далее определяем х по пропорции.
x = (6∙1)/2 = 3моль
Задача 2 Определить объем кислорода, необходимый для полного окисления 6 моль диоксида серы (SO2) в триоксид серы(SO3).
Рассуждаем так же, как в задаче 1. Отличие в том, что определить нужно объем вещества. Чтобы перейти к количеству вещества, воспользуемся ۟расчетной формулой 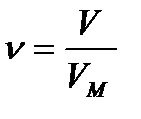 , где VM = 22,4л/моль
, где VM = 22,4л/моль
Задача 3. Определить массу кислорода, необходимую для полного окисления 6 моль диоксида серы (SO2) в триоксид серы (SO3).
Рассуждаем так же, как в задаче 1. Отличие в том, что определить нужно массу вещества. Чтобы перейти к количеству вещества, воспользуемся расчетной формулой: 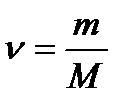 , где М – молярная масса вещества, величину которой определяем при помощи периодической системы.
, где М – молярная масса вещества, величину которой определяем при помощи периодической системы.
Вариант 1
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Карбид алюминия→метан→хлорметан→этан→этен→этин→этаналь
2. Задача определить объем хлора, необходимый для получения 11,2л хлорметана.
Вариант 2
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Оксид кальция→карбид кальция→ацетилен→этилен→полиэтилен
↓ ↓
Бензол этанол
2. Задача. Какая масса 92% этилового спирта необходима для получения 1,12л этилена?
Вариант 3
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Этанол→этилен→ацетилен→бензол→хлорбензол→фенол
↓
Хлорэтан
2. Задача. Определить массу бензола, которую можно получить из 56л ацетилена, если доля выхода продукта составляет 60% от теоретически возможного?
Вариант 4
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
метан→хлорметан→этан→этилен→этанол→этаналь
↓
Ацетилен
2. Задача. Какую массу этилового спирта можно получить гидратацией 112л этилена, если доля выхода продукта составляет 80% от теоретически возможного?
Вариант 5
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Метан→ацетилен→бензол→хлорбензол→фенол(C6H5OH)
↓
Диоксид углерода.
2. Задача. При действии избытка воды на 32 грамма технического карбида кальция образовалось 8,96 литра ацетилена (н.у.). Определить массовую долю примесей в техническом карбиде кальция.
Вариант 6
1. Составить уравнение реакций с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Карбид алюминия→метан→хлорметан→этан→этилен→ацетилен→этаналь
2. Задача. Определить объем хлора, необходимый для получения 33,6л хлорметана.
Вариант 7
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Этиловый спирт→этилен→ацетилен→этилен→этанол
↓
хлорэтан→этанол.
2. Задача. Какую массу этилового спирта можно получить гидратацией 112 литров этилена, если доля выхода продукта реакция составляет 80% от теоретически возможного.
Вариант 8
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Оксид кальция→карбид кальция→ацетилен→этилен→этанол
↓ ↓
Бензол этановая кислота
2. Задача. При действии избытка воды на 40г карбида кальция образовалось 8,96 литра ацетилена (н.у.). Определить объемную долю выхода продукта по сравнению с теоретически возможным.
Вариант 9
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Карбид алюминия→метан→хлорметан→этан→этен→этин
↓
Этаналь
2. Задача определить объем хлора, необходимый для получения 11,2л хлорметана
Вариант 10
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Этиловый спирт→этилен→ацетилен→бензол→циклогексан
↓
этаналь→этановая кислота.
2. Задача. Определить массу воды, необходимую для взаимодействия с 10 литрами этилена (н.у.), содержащего 20% примесей.
Вариант 11
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
метан→хлорметан→этан→этилен→этанол→этаналь
↓
Ацетилен
2. Задача. Какую массу этаналя можно получить гидратацией 11,2л ацетилена, если доля выхода продукта составляет 80% от теоретически возможного?
Вариант 12
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Оксид кальция→карбид кальция→ацетилен→этилен→полиэтилен
↓ ↓
Бензол этанол
2. Задача. Какую массу этилового спирта можно получить гидратацией 112 литров этилена, если доля выхода продукта реакция составляет 80% от теоретически возможного.
Вариант 13
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Метан→ацетилен→бензол→хлорбензол→фенол
↓
Диоксид углерода.
2. Задача. При действии избытка воды на 50г карбида кальция образовалось 9л ацетилена (н.у.). Определить долю выхода ацетилена в % от теоретически возможного.
Вариант 14
1. Составить уравнения реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Карбид алюминия→метан→хлорметан→этан→этен→этин→этаналь
2. Задача определить объем хлора, необходимый для получения 11,2л хлорметана
Вариант 15
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
Этиловый спирт→этилен→ацетилен→этаналь→этановая кислота
↓
хлорэтан→этанол.
2. Задача. Определить массу уксусной кислоты, которую можно получить окислением 92г этилового спирта, если доля выхода продукта составляет 75% от теоретически возможного
Генетическая связь между углеводородами и кислородсодержащими органическими веществами
Отчет по практическаой работе 3.
Студент_________________________________________________________
Группа_____
Цельработы: ______________________________________________________________________________________________________________________________________________________________________________________________________
1. Составить уравнение реакций, с помощью которых можно осуществить превращения. Указать условия протекания и тип реакций.
1)
2)
3)
4)
5)
2. Задача
Урок 15
