Углеводы, строение и свойства
Углеводы — важный класс природных веществ — встречаются повсеместно в растительных, животных и бактериальных организмах.
В биосфере на долю углеводов приходится больше, чем всех других органических соединений вместе взятых. В растениях они составляют 80—90% из расчета на сухое вещество; в животном организме на их долю приходится 2-3 % массы тела.
Для большинства организмов природные углеводы выполняют множество функции:
¾ углеводы являются источником углерода, который необходим для синтеза белков, нуклеиновых кислот, липидов и др.;
¾ энергетическая. Углеводы обеспечивают до 70% потребности организма в энергии. При окислении 1 г углеводов выделяется 16,9 кДж энергии;
¾ резервная. Некорые углеводы (крахмал и гликоген) представляют собой форму хранения питательных веществ (в основном в виде глюкозы).
¾ строительная. Целлюлоза и другие полисахариды образуют прочный каркас клеточных стенок; в комплексе с белками и липидами они входят в состав биомембран всех клеток.
¾ защитная. Кислые гетерополисахариды выполняют роль биологического смазочного материала, выстилая трущиеся поверхности суставов, слизистой пищеварительных путей, носа, бронхов, трахеи и др.
¾ углеводы участвуют в образовании комплексных молекул, а именно гликопротеинов и гликолипидов. Гликопротеины служат маркерами в процессах узнавания молекулами и клетками друг друга, определяют антигенную специфичность, обуславливают различия групп крови, выполняют рецепторную, каталитическую и другие функции.
Углеводы включают соединения, начиная от низкомолекулярных, содержащих всего несколько атомов углерода, до веществ, молекулярная масса которых достигает нескольких сот тысяч и даже миллионов. Все углеводы делят на три класса в зависимости от числа остатков сахаров: моносахариды, олигосахариды и полисахариды.
Моносахариды, или простые сахара, содержат только одну структурную единицу и при гидролизе не распадаются. Моносахариды — это полигидроксиальдегиды или полигидроксикетоны.
Олигосахариды состоят из нескольких (от 2 до 10) остатков моносахаридов, соединенных О-гликозидными связями. Наиболее распрастраненными являются дисахариды («di» - от греческого «два»), состоящие из двух остатков моносахаров.
Полисахариды являются высокомолекулярными веществами, состоящими из остатков моносахаридов, соединенных О-гликозидными связями, со степенью полимеризации выше 10.
Моносахариды.
Существует несколько принципов классификации моносахаридов:
1. по числу углеродных атомов, входящих в состав молекулы (С3 – триозы, C4 – тетрозы, C5 – пентозы, C6 – гексозы, C7 – гептозы, C8 – октозы и т. д.);
2. по характеру карбонильной группы: альдегидной – альдозы или кетонной групп – кетозы;
3. по наличию других групп, кроме карбонильной и гидроксильной:
— нейтральные сахара, содержащие только карбонильную и гидроксильную группы;
— аминосахара (основные), содержащие вместо гидроксигруппы аминогруппу;
— кислые сахара, содержащие помимо карбонильных и гидроксильных групп еще и карбоксильную.
Формулы некотоых из моносазаридов приведены на рисунках 2.10 и 2.11.
В основу номенклатуры сахаров положены тривиальные названия моносахаридов состава СnН2nОn с прямой цепью углеродных атомов: ксилоза, рибоза, глюкоза, фруктоза и др. Наименованиям кетоз придается окончание -улоза, например кетоза С5 - пентулоза. Всем моносахарам присуща конфигурационная (оптическая) изомерия, т. е. они существуют в двух энантиомерных формах – D и L. Принадлежность моносахаридов к D- или L-ряду определяется по расположению ОН-группы у последнего (считая от альдегидной или кетогруппы) хирального (ассимметричного) атома углерода. В качестве стандарта сравнения конфигурации асимметрического атома углерода предложено использовать изомер глицеринового альдегида. Названный D-глицериновым альдегидом изомер вращает плоскость поляризованного света вправо, а его зеркальное отражение антипод — L-глицериновый альдегид — влево.
Некоторые моносахариды, например фруктоза, отнесенные к D-ряду, являются левовращающими, а представители L-ряда — правовращающими. Чтобы указать и принадлежность сахара к D- или L-ряду, и направление вращения плоскости поляризации, после символов D или L перед названием моносахарида в скобках ставят знак (+) или (—), обозначающий соответственно правое или левое вращение.
В живых организмах моносахариды присутствуют преимущественно в D-конфигурации, которую называют природной. Исключение составляет L-арабиноза бактерий, L-рамноза и L-сорбоза растений.
У альдоз, начиная с n = 4, и кетоз — с n = 5 имеется несколько хиральных центров, т. е. существует ряд диастереомеров, представляющих собой разные по химическим свойствам соединения, причем каждый из диастереомеров может существовать в L- и D- конфигурации.
Карбонильные группы моносахаридов с длиной цепи n = 5 и более могут вступать во взаимодействие со спиртовыми группами с образованием циклической полуацетали,илиполукетали, которые называются соответственно фуранознымиилипиранозными по аналогии с известными соединениями — фураном или пираном:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
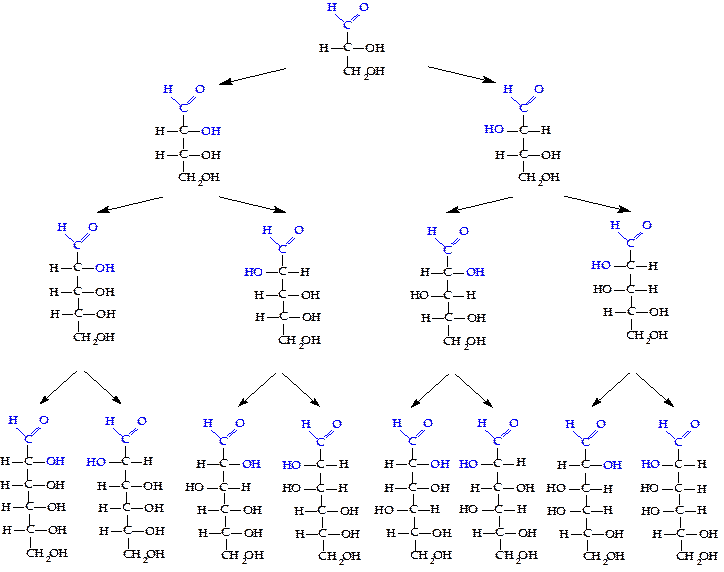
Рисунок 2.10 - Стереохимические соотношения D-альдоз с разным числом атомов углерода в цепи
|
|
|
|
|
|
|
|

 Рисунок 2.11 - Стереохимические соотношения D-кетоз с разным числом атомов углерода в цепи
Рисунок 2.11 - Стереохимические соотношения D-кетоз с разным числом атомов углерода в цепи
|
|
|
|
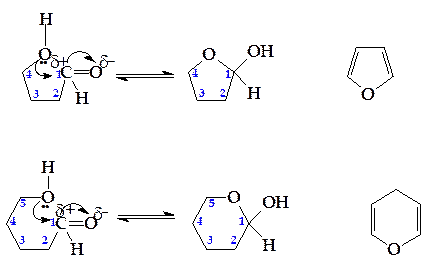
При этом в молекуле пентоз или гексоз появляется еще один хиральный центр и новая пара изомеров — a - и b-аномеры, отличающиеся расположением гидроксильной группы при полуацетальном атоме углерода относительно плоскости кольца: у a-аномера гидроксильная и СН2ОН-группы находятся по разные плоскости кольца, а у b-аномера — по одну его сторону. Таким образом, гексоза образует четыре циклические формы (a- и b-фуранозную и a- и b-пиранозную), находящиеся в растворе в динамическом равновесии с ациклической формой. В водном растворе все эти формы способны взаимно превращаться друг в друга через оксоформу (нециклическую форму) глюкозы, количество которой составляет менее 1%.
|
|
|
|
|
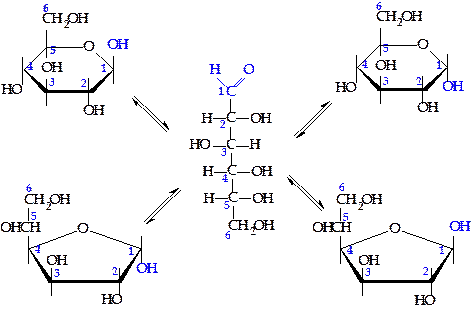
Пиранозные формы гексоз и пентоз значительно более устойчивы, чем фуранозные, поэтому в растворе всегда существенно преобладают первые. a- и b-Формы моносахаридов, обладающие разной величиной оптического вращения, в процессе растворения в воде взаимно переходят друг в друга, поэтому удельное вращение [a]D в свежеприготовленных растворах моносахаридов изменяется в течение времени до определенной величины. Это явление получило название мутаротации (от лат. «multirotatia» — много вращений).
Олигосахариды.
Как и для моносахаридов, в классификацию олигосахаридов положено несколько принципов. Их классифицируют:
1. в зависимости от числа моносахаридных фрагментов, входящих в состав олигосахаридов: ди-, три-, тетрасахариды и т. д.;
2. по составу моносахаридных остатков:
— гомоолигосахариды, состоящие из остатков одного вида моносахарида;
— гетероолигосахариды, состоящие из остатков разных сахаров;
3. в зависимости от порядка соединения мономеров:
— линейные сахара;
— разветвленные сахара;
4. восстанавливающие и невосстанавливающие сахара.
У восстанавливающих олигосахаридов связь между мономерами осуществляется за счет спиртового и полуацетального гидроксилов. Потому, одно из моносахаридных звеньев сохраняет свободный полуацетальный гидроксил, который определяет восстанавливающие свойства (способность сахара окисляться) и все реакции, свойственные моносахаридам.
У невосстанавливающих олигосахаридов гликозидная связь образована за счет полуацетальных гидроксилов моносахаридов. Они не содержат свободного полуацетального гидроксила и не проявляют характерных реакций альдегидной группы. Примеры восстанавливающих и невосстанавливающих дисахаридов, а также характер положения связи между моносахарами приведены в таблице 2.3.
Из дисахаридов наибольшее распростаранение в природе получили мальтоза, лактоза и сахароза.
Мальтоза состоит из двух остатков a-D-глюкозы, соединенных 1®4 О-гликозидной связью. Целлобиоза также состоит из двух остатков глюкозы, однако уже b-формы, соединенных также связью 1®4.
Таблица 2.3 - Восстанавливающие и невосстанавливающие дисахариды
| Восстанавливающие сахара | |
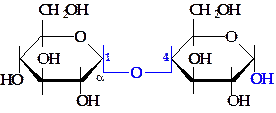 мальтоза мальтоза | 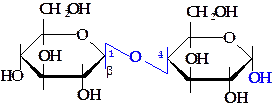 целлобиоза целлобиоза |
Окончание таблицы 2.3.
| Невосстанавливающие сахара | |
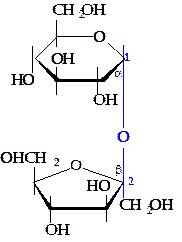 сахароза сахароза | 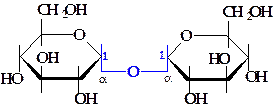 трегалоза трегалоза |
Сахарозу, или обычный сахар, синтезируют многие растения. У высших животных она не образуется. В состав сахарозы входят a-D-глюкоза и b-D-фруктоза.
Среди природных трисахаридов важное значение имеют рафиноза, состоящая из остатков D-фруктозы, D-галактозы и D-глюкозы, а также ген-цианоза, состоящая из двух остатков D-глюкозы и одного остатка D-фруктозы.
Полисахариды (гликаны).
Основная масса всех углеводов, встречающихся в природе, существует в виде полисахаридов. С точки зрения их функционального назначения полисахариды можно разделить на две основные группы. Первая группа, в которую входит, например, целлюлоза, несет главным образом структурную функцию. Вторая группа, представителем которой является, в частности, гликоген, выполняет функции, связанные с питанием. Эти молекулы играют в основном роль депо и могут быть легко мобилизованы путем превращения в моносахариды.
С точки зрения общих принципов строения полисахариды харктеризуются тремя особенностями:
¾ природой составляющих их мономеров;
¾ природой гликозидной связи между мономерами;
¾ последовательностью расположения моносахаридных остатков в цепи.
В зависимости от природы мономеров полисахариды делятся на гомополисахариды, если все входящие в состав мономеры одинаковы, и гетерополисахариды, если мономеры различны.
Названия гомополисахаридов слагаются из названий входящих в их состав редуцирующих моносахаридов, в которых суффикс -оза меняется на суффикс -ан (глюкан или аубазидан, декстран, маннан или родэксман, арабан и т. д.). Разветвленный гетерополисахарид, в основной цепи которого находятся остатки глюкозы, а в боковой — остатки маннозы, называют манноглюканом, а в случае обратного распределения моноз — глюкоманнаном. Иногда полисахариды называют по продуценту, сохраняя суффикс -ан, например ксанбан (продуцент — Xanthomonas campestris).
Гомополисахариды. Самым распространенным на Земле органическим соединением и важнейшим гомополисахаридом является целлюлоза. Она входит в состав клеточных стенок практически всех растений, тем самым служит основным строительным элементом. Целлюлоза - совокупность очень длинных неразветвленных цепей, состоящих из b-глюкозы, молекулы которой соединены связями 1®4, а повторяющимся звеном является дисахарид целлобиоза (рисунок 2.12).
Основная биологическая функция целлюлозы – структурная. Питательная ценность целлюлозы для высших животных и человека ограничена, поскольку в их организме нет ферментов (целлюлаз), способных разорвать b-(1®4)-гликозидные связи глюкозы.
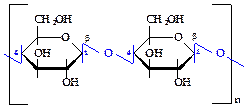 в скобках указан мономерный участок - целлобиоза Рисунок 2.12 - Строение молекулы целлюлозы в скобках указан мономерный участок - целлобиоза Рисунок 2.12 - Строение молекулы целлюлозы |
Другим ярким представителем гомополисахаридов является основной резервный полисахарид растений ‑ крахмал.
Крахмал представляет собой смесь полисахаридов — амилозы и амилопектина.
Амилоза — линейный полимер с a-(1®4)-гликозидными связями между остатками D-глюкопиранозы.
Амилопектин отличается от амилозы высокоразветвленным строением. Остатки D-глюкозы в линейных участках полисахарида связаны a-(1®4)-гликозидными связями, а в точках ветвления имеются дополнительные a-(1®6)-связи (рисунок 2.13).
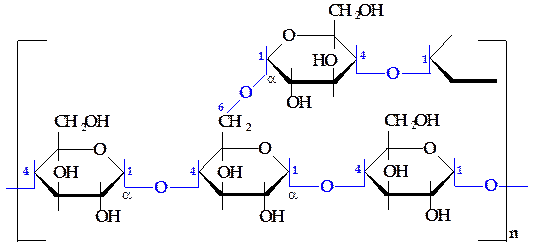
Рисунок 2.13 - Строение амилопектина растительного крахмала
Биологическая роль крахмала состоит в том, что он является запасным питательнм веществом в растениях, и когда возникает потребность в энергии и источнике углерода, крахмал гидролизуется ферментами - амилазами. Последние расщепляют a-(1®4)-гликозидные связи, что приводит к образованию смеси глюкозы и мальтозы. В результате действия амилаз происходит полное расщепление амилозы, однако амилопектин расщепляется лишь частично, и для разрыва 1®6 гликозидных связей необходимо действие еще одних ферментов – мальтаз, разрывающих связи в точках ветвления.
Гликоген (животный крахмал) — разветвленный полисахарид животных организмов, а также некоторых бактерий и дрожжей. Структура гликогена подобна амилопектину — a-(1®4)-глюкан с a-(1®6)-связями в точках ветвления.
Гликоген отличается от амилопектина лишь большей разветвленностью и более жесткой упаковкой молекулы. Если в амилопектине крахмала точки ветвления встречаются через каждые 25-30 остатков глюкозы, то в молекуле гликогена – через 8-10 остатков вдоль a-(1®4)-цепи (рисунок 2.14).
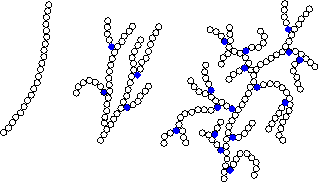 кружочками обозначены остатки a-глюкозы, синие кружочки – точки ветвления |
Рисунок 2.14 - Структура молекул
амилозы (а), амилопектина (б)
и гликогена (в)
Молекулярная масса гликогена колеблется от 102 до 105 кДa. Как и крахмал, гликоген является запасающим веществ в организме животных, который накапливается в печени и расходуется в мышцах во время интенсивной физической нагрузки.
Среди представителей гомополисахаридов можно отметить: инулин (полимер фруктозы), дектраны (полимер a-D-глюкозы, соединенной связями 1®6, но цепи соединены между собой связями 1®4), пектины (полимеры галактуроновой кислоты с преобладающей связью 1®4), хитин (полимер b-(1®4)-ацетил-глюкозамина) и многие другие.
Гетерополисахариды.
К ярко выраженным гетерополисахаридам относятся гиалуроновая кислота, хондроитинсульфаты, кератосульфаты. Поскольку водные растворы этих соединений гелеобразны, их называют мукополисахаридами (от лат. «mucos» — слизь).
Гиалуроновая кислота состоит из эквимолярных количеств D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, которые чередуются друг с другом в молекуле полисахарида. Аминосахар соединен с кислотой b-(1®4)-связью, а кислота — с аминосахаром b-(1®3) гликозидной связью (рисунок 2.15).
Этот полисахарид присутствует в соединительных тканях животных, а также в стекловидном теле глаза и в синовиальной жидкости. Кроме того, он синтезируется также различными штаммами бактерий.
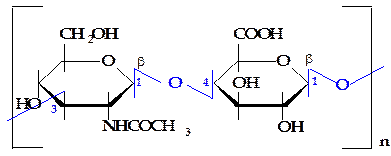 Рисунок 2.15 - Фрагмент молекулы гиалуроновой кислоты Рисунок 2.15 - Фрагмент молекулы гиалуроновой кислоты |
Предполагают, что функция гиалуроновой кислоты заключается в том, чтобы связывать воду в интерстициальных пространствах и удерживать клетки вместе в желеподобном матриксе. Кроме того, она придает синовиальной жидкости смазочные свойства и способность смягчать удары.
Хондроитинсульфаты. К ним относится, в частности, хондроитин — полисахарид, сходный с гиалуровой кислотой, в котором D-глюкозамин замещен D-галактозамином.
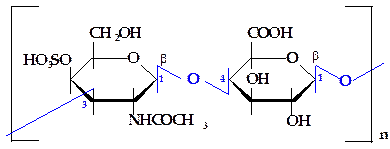 Рисунок 2.16 - Фрагмент молекулы хондроитинсульфата Рисунок 2.16 - Фрагмент молекулы хондроитинсульфата |
Хондроитинсульфаты состоят из эквимолярных количеств D-глюкуроновой кислоты, N-ацетил-D-галактозами-на и сульфата (рисунок 2.16). Их структуры различаются только по положению сульфатных остатков. В хондроитинсульфате находитсяL-идуроновая кислота. Во всех случаях находятся b-(1®3)- и b-(1®4)-гликозидные связи.
Кератосульфаты. Они сходны с хондроитинсульфатами как в структурном отношении, так и по своему распространению. Кератосульфат является одним из главных полисахаридов соединительной ткани.
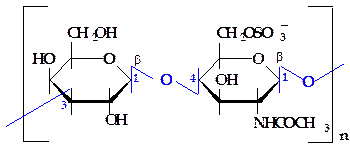 Рисунок 2.17 - Фрагмент молекулы кератосульфата Рисунок 2.17 - Фрагмент молекулы кератосульфата |
Кератосульфат состоит из чередующихся остатков D-галактозы и N-ацетил-D-глюкозаминсульфата, соединенных между собой чередующимися связями b-(1®4)- и b-(1®3)-типа (рисунок 2.17).
Среди других природных образований, содержащих гетерополисахариды, стоит назвать: гепарин – полимер сульфатированных глюкозамина и идуроновой кислоты, соединенных a-(1®4)-гликозидной связью; камеди (вишневый клей, гуммиарабик) - смесь солей гексуроновых кислот и пентоз; лигнин – смесь, содержащая неорганические кислоты, фенольные соединения, вещества ароматического ряда. В состав этих гетерополисахаридов входят остатки маннозы, галактозы, ксилозы, глюкуроновой кислоты.
