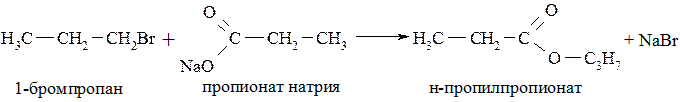Глава 11. Галогенопроизводные углеводородов
Галогенопроизводные — это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на атомы галогенов.
По числу атомов галогена различают моно-, ди-, три-и т.д. полигалогенопроизводные:
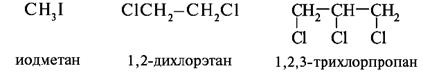
По строению углеводородного радикала различают галогенопроизводные алифатического, карбоциклического и гетероциклического рядов. Внутри каждой группы можно выделить подгруппы: например, алкилгалогениды, алкенилгалогениды, арилгалогениды и т.д.
Всё же для удобства рассмотрения реакционной способности, более целесообразно учитывать тип гибридизации атома углерода, с которым связан галоген.
В алкилгалогенидах (галогеналканах) атом галогена связан с sp3-гибридизованным атомом углерода. В галогеналкенах галоген может быть непосредственно связан с sp2-гибридизованным атомом углерода, например, R–CH=CHCl или же с Сsp3 в молекуле СН2=СН–СН2–Cl. Для ароматических галогенопроизводных выделяют соединения с галогеном в ядре, т.е. галоген связан с Сsp2-атомом бензольного ядра, и с галогеном в боковой цепи, например, Ar–CH2Cl.
Способы получения
Галогенирование предельных углеводородов
Фторирование алканов (SR-механизм) протекает очень бурно с выделением большого количества тепловой энергии, что часто сопровождается взрывом. Поэтому процесс требует особых условий и конструкции реакторов. Хлорирование алканов проходит по SR-механизму под влиянием УФ-облучения и/или температуры. Во избежание взрыва процесс осуществляется в избытке алкана, так как эквимолярная смесь метана с хлором под влиянием УФ-облучения взрывается.
Легче всего замещается водород у третичного атома углерода, труднее у вторичного. Подробно механизм и особенности хлорирования алканов см. разд. 5.3.
Галогенирование алканов иначе называют реакцией металепсии.
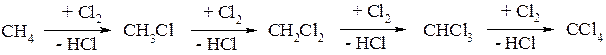
Бромирование низших алканов (метан, этан) не очень характерно, хотя введение брома при нагревании и интенсивном УФ-облучении возможно (гексан, гептан и т.д.).
Прямое галогенирование алкенов и алкинов
Из алкенов образуются виц-дигалогенпроизводные:
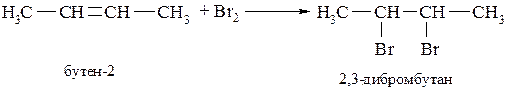
Из алкинов получают тетрагалогенопроизводные:
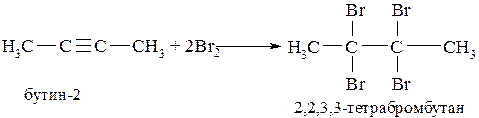
Гидрогалогенирование алкенов и алкинов
Присоединение галогеноводородов происходит по механизму электрофильного присоединения – АdЕ и в соответствии с правилом Марковникова. Из алкенов образуются моногалогенопроизводные:
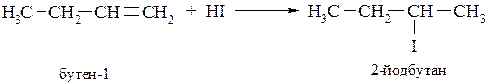
При гидрогалогенировании алкинов присоединение происходит также в соответствии с правилом Марковникова: в соотношении алкин - галогеноводород 1:1 образуется соответствующий винилгалогенид, а в избытке галогеноводорода образуется гем-дигалогенопроизводное:
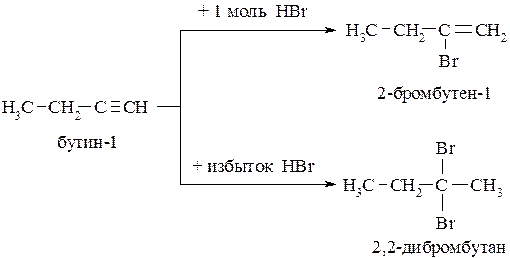
Фтороводород к алкенам не присоединяется, а стимулирует их полимеризацию.
Получение из спиртов.
При взаимодействии спиртов с галогеноводородом происходит замещение гидроксигруппы на галоген, и данная реакция протекает по SN-механизму (подробно смотри разд. 3.1.2).
Следует обратить внимание на следующие особенности.
Реакция спирта с галогеноводородом обратима, поэтому для смещения равновесия вправо необходимо безводный спирт насыщать сухим газообразным галогеноводородом, либо процесс вести в присутствии сухой соли – галогенида щелочного металла и концентрированной серной кислоты. Это позволяет связывать выделяющуюся воду и предотвратить гидролиз целевого продукта.
Гидроксигруппа относится к трудно уходящим (трудно замещаемым) группам, поскольку является более сильным основанием, чем вода. Следовательно, вода является лучшей уходящей группой, чем гидроксид-анион. В кислой среде спиртовый гидроксил присоединяет протон с образованием ониевого катиона R–O+H2.
Из такого катиона атакующий галогенид-анион вытесняет уже не гидроксид-анион, а воду.
Далее галогенид-анион атакует α-углеродный атом, поскольку на нем сосредоточен высокий положительный заряд.. Атака происходит со стороны, наиболее удалённой от замещаемой группы, т.е. с тыла. В переходном состоянии происходит формирование новой связи С–Hal и одновременный разрыв связи С–О+Н2:
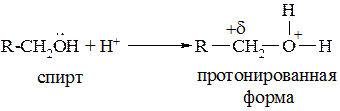

Поскольку образование связи C–Hal и разрыв связи С–О+Н2 происходит одновременно, то подобные процессы принято называть согласованными.
Рассмотренный механизм представляет собой пример одностадийного нуклеофильного замещения. Первичные спирты и метанол реагируют с галогеноводородами по SN2-механизму с высокими выходами (до 90%). С третичными спиртами реакция протекает по SN1- механизму. Стадией, лимитирующей кинетику процесса, является образование третичного карбокатиона:
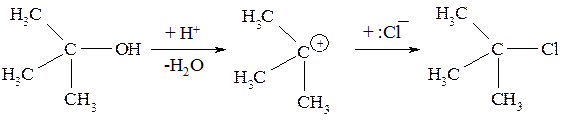
Что касается вторичных спиртов, то с ними реакции протекают по смешанному механизму.
Реакционная способность спиртов по отношению к галогеноводородам убывает в следующей последовательности:
аллил, бензил > третичный > вторичный > первичный
Из спиртов галогенопроизводные можно получить, используя галогениды фосфора – PHal3; PHal5; хлорокись фосфора (V) – POCl3, а также тионилхлорид – SOCl2:
R–CH2OH + PCl5 → R–CH2Cl + POCl3 + HCl
R–CH2OH + SOCl2 → R–CH2Cl + SO2 + HCl
Из оксосоединений
Из альдегидов и кетонов действием пентагалогенидами фосфора можно получить гем-дигалогенопроизводные:
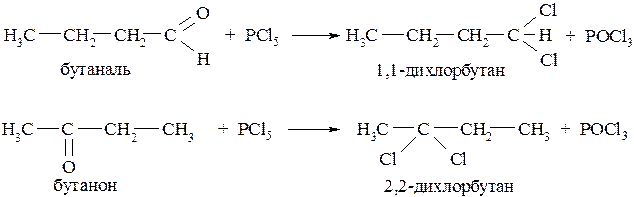
Галоформы
К ним относятся CHCl3 – хлороформ, CHBr3 – бромоформ и CHI3 – йодоформ. Их получают взаимодействием соответствующего галогена с ацетальдегидом:
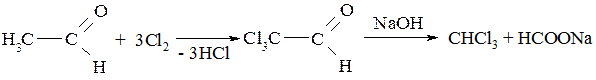
Подробно галоформная реакция будет рассмотрена в главе 16.
Из карбоновых кислот.
При взаимодействии PCl5 с карбоновыми кислотами образуются соответствующие хлорангидриды, которые под влиянием высокой температуры и давлении переходят в соответствующие трихлорпроизводные:
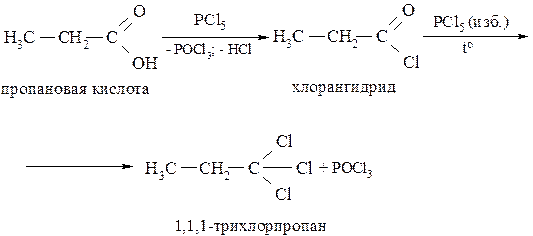
Из солей карбоновых кислот под действием брома можно получить бромпроизводное, в котором на один атом углерода меньше, чем в исходной кислоте. Причиной тому является декарбоксилирование:

Ароматические галогенопроизводные можно получить галогенированием в ядро и в боковую цепь, о чём подробно изложено в разделе 10.3.1.
Физические свойства
Такие параметры, как температура плавления и кипения зависят в большей степени от природы галогена. Низшие и средние галогеналканы являются газообразными веществами и жидкостями. Число атомов галогена также влияет на температуры кипения и плавления, что можно проследить на примере йодметанов.
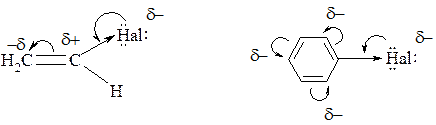
В галогенопроизводных типа Csp3–Х энергия связи в значительной степени зависит от природы галогена: наиболее прочной является связь C–F, наиболее слабой – связь C–I. Связь С–Hal полярна из-за большей электроотрицательности атома галогена, поэтому на атоме галогена появляется избыток электронной плотности, а на углероде-дефицит. В соединениях типа Csp2–Х связь менее полярна по двум причинам:
- во-первых, Csp2 более электроотрицателен, чем Csp3;
- во-вторых, имеет место р,π-сопряжение за счёт взаимодействия р-орбитали галогена с парой электронов с π-электронами двойной связи алкена или π-секстетом ароматического ядра, т.е. атом галогена характеризуется выраженным –I и слабым +М-эффектами:
Длина связи C–Hal в этом случае короче:
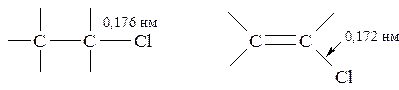
В галогенопроизводных типа Сsp-x полярность связи намного ниже, чем у галогеналкенов.
Химические свойства
Высокая полярность связи Csp3–Hal является результатом перераспределения электронной плотности, в связи с чем в молекуле формируется электрофильный центр. Таковым становится атом углерода, непосредственно связанный с галогеном. Результатом отрицательного индуктивного эффекта, проявляемого галогеном (-I–эффект), является полярность молекулы. Следует также учитывать, что связь C–Hal характеризуется высокой поляризуемостью, т.е. становится ещё более полярной под воздействием реакционной среды.
Поляризуемость связи C–Hal увеличивается от C–F к C–I, что и подтверждается в реакциях нуклеофильного замещения.
Подвижность атома галогена в аллильном положении гораздо выше. Это объясняется тем, что образующийся при диссоциации аллильный катион стабилизируется за счёт сопряжения свободной р-орбитали катионного атома углерода с соседней π-связью, что способствует делокализации положительного заряда:
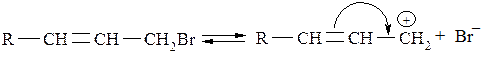
В предельных галогенопроизводных вследствие индуктивного эффекта формируется ещё один реакционный центр – СН-кислотный центр с участием β-углеродного атома.
Галогенопроизводные Сsp3–Hal характеризуются высокой реакционной способностью. Для них наиболее характерны реакции нуклеофильного замещения, при которых галоген замещается на нуклеофил, а также реакции β-элиминирования, в которой участвует СН-кислотный центр (β-углеродный атом).
11.3.1. Реакции нуклеофильного замещения у галогенопроизводных типа Csp3–Hal
Высокая полярность и поляризуемость связи C–Hal являются причиной лёгкого разрыва этой связи по гетеролитическому механизму при нуклеофильной атаке молекулы:

Данная реакция представляет собой пример типичного нуклеофильного замещения по SN2-механизму:
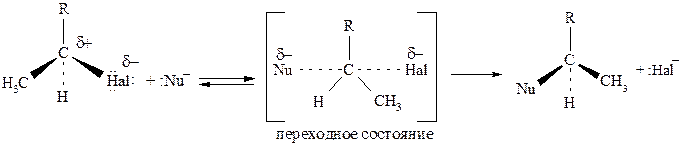
Важно отметить, что если в исходной молекуле α-углеродный атом является асимметрическим, то в результате SN2-реакции происходит изменение конфигурации: S-конфигурация переходит в R и наоборот. Таким образом реакция по SN2 мехпнизму является стереоспецифической.
Из схемы реакции видно, что уходящей частицей является галогенид-анион, который представляет собой слабое основание: чем слабее выражены основные свойства галогенид-аниона, тем он более стабилен и тем легче происходит замещение.
В ряду галогенид-анионов наиболее слабым основанием и, следовательно, самой легко уходящей частицей является I-, затем Br-, Cl- и F-.
При переходе от первичных галогенопроизводных к третичным, реакция нуклеофильного замещения протекает по SN1-механизму (см. разд. 11.1).
В качестве нуклеофилов могут быть использованы анионные нуклеофилы - ОН-; О- Alk-; CN-; нейтральные нуклеофилы – Н2О; NH3; NH2R; NHRR1; NR1R2R3; спирты, тиолы.
Используя перечисленные нуклеофилы, можно на основе галогенопроизводных получить соединения, относящиеся к разным классам.
Говоря о нуклеофилах, следует учитывать, что они являются основаниями по Брёнстеду и Льюису, хотя при этом необходимо помнить разницу в понятиях «основность» и «нуклеофильность».
Под основностью подразумевают реакционную способность основания, т.е. способность предоставлять электронную пару протону, который является кислотой.
Нуклеофильность – это способность предоставлять электронную пару карбкатиону, или другой положительно заряженной частице (кроме Н+).
Таким образом, основность – это понятие, относящееся к кислотно-основному взаимодействию, а нуклеофильность – это понятие, подразумевающее влияние основания Льюиса на реакции нуклеофильного замещения.
Гидролиз. Под действием свежеприготовленного гидроксида серебра или водного раствора щёлочи образуются спирты:
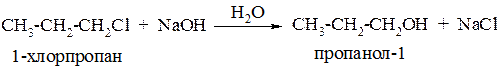
Образование простых эфиров. При взаимодействии с алкоголятами щелочных металлов можно получить простые эфиры:
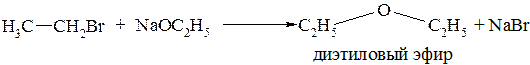
Получение сложных эфиров. В этом случае используют соли карбоновых кислот и соответствующий галогеналкан. Более эффективно процесс протекает при использовании первичных или вторичных бром- или йодалканов: