Окислительное дезаминирование
Наиболее активно в тканях происходит дезаминирование глутаминовой кислоты. Реакцию катализирует фермент глутаматдегидрогеназа,коферментом глутаматдегидрогеназы является NAD+. Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование а-иминоглутарата, затем - неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется а-кетоглутарат (см. схему ниже).
Окислительное дезаминирование глутамата -
обратимая реакция и при повышении концентрации аммиака в клетке может протекать в обратном направлении, как восстановительное шинирование α-кетоглутарата.
Глутаматдегидрогеназа очень активна в митохондриях клеток практически всех органов, кроме мышц. Глутаматдегидрогеназа играет важную роль, так как является регуляторным ферментом аминокислотного обмена. Аллостерические ингибиторы глутаматдегидрогеназы (АТФ, ГТФ, NADH) вызывают диссоциацию фермента и потерю глутаматдегидрогеназной активности. Высокие концентрации АДф активируют фермент. Таким образом, низкий энергетический уровень в клетках стимулирует разрушение аминокислот и образованиеα-кетоглутарата, поступающего в ЦТК как энергетический субстрат. Глутаматдегидрогеназа может индуцироваться стероидными гормонами (кортизолом).
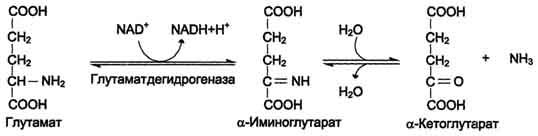
Схема
В организме человека и животных в основном происходит окислительное дезаминирование аминокислот. Этот процесс катализируется оксидазами L - и D-аминокислот с простетиче-скими группами соответственно ФМН и ФАД.
Оксидаза L-аминокислот
В печени и почках обнаружен фермент оксидаза L-аминокислот,способный дезаминировать некоторые L-аминокислоты (см. схему в конце стр.).
Коферментом в данной реакции выступает FMN. Однако вклад оксидазы L-аминокислот в дезаминирование, очевидно, незначителен, так как оптимум её действия лежит в щелочной среде (рН 10,0). В клетках, где рН среды близок к нейтральному, активность фермента очень низка.
Оксидаза D-аминокислоттакже обнаружена в почках и печени. Это FAD-зависимый фермент. Оптимум рН этой оксидазы лежит в нейтральной среде, поэтому фермент более активен, чем оксидаза L-аминокислот. Роль оксидазы D-аминокислот невелика, так как количество D-изомеров в организме крайне мало, потому что в белки пищи и белки тканей человека и животных входят только природные L-аминокислоты. Вероятно, оксидаза D-аминокислот способствует их превращению в соответствующие L-изомеры (рис. 9-8).
2. Непрямое дезаминирование
(трансдезаминирование)
Большинство аминокислот не способно дезаминироваться в одну стадию, подобно Глу. Аминогруппы таких аминокислот в результате трансаминирования переносятся на α-кетоглутарат с образованием глутаминовой кислоты, которая затем подвергается прямому окислительному дезаминированию. Такой механизм дезаминирования аминокислот в 2 стадии получил название трансдезаминирования, или непрямого дезаминирования:
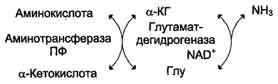
Непрямое дезаминирование аминокислот происходит при участии 2 ферментов: аминотрансферазы (кофермент ПФ) и глутаматдегидрогеназы (кофермент NAD+).
Значение этих реакций в обмене аминокислот очень велико, так как непрямое дезаминирование - основной способ дезаминирования большинства аминокислот.Обе стадии непрямого дезаминирования обратимы (рис. 9-9), что обеспечивает как катаболизм аминокислот (рис. 9-9, А), так и возможность образования практически любой аминокислоты из соответствующей α-кетокислоты (рис. 9-9, Б).
В мышечной ткани активность глутаматдегидрогеназы низка, поэтому в этих клетках при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ. Вначале происходит перенос аминогруппы аминокислот на аспартат, затем на инозиновую кислоту (ИМФ) и в завершение - дезаминирование АМФ. Представленная схема отражает последовательность реакций непрямого неокислительного дезаминирования:
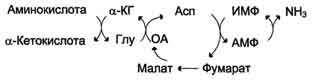
Можно выделить 4 стадии процесса:
- трансаминирование с α-кетоглутаратом, образование глутамата;
- трансаминирование глутамата с оксалоацета-том (фермент ACT), образование аспартата;
- реакция переноса аминогруппы от аспартата на ИМФ (инозинмонофосфат), образование АМФ и фумарата;
- гидролитическое дезаминирование АМФ.
Перенос аминогруппы от аспартата и синтез АМФ происходят следующим образом (см. схему А на с. 476).
Реакция дезаминирования адениловой кислоты происходит под действием фермента АМФ дезаминазы (см. схему Б на с. 476).
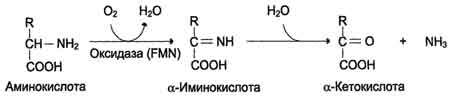
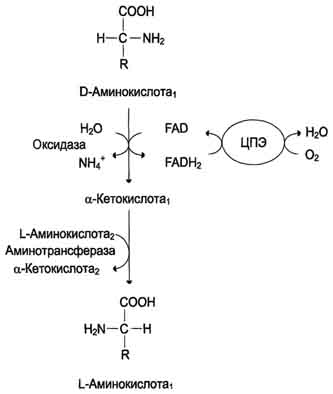
Рис. 9-8. Биологическая роль оксидазы D-аминокислот.
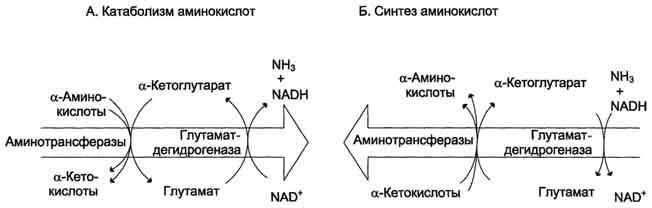
Рис. 9-9. Биологическая роль непрямого дезаминирования. А - при катаболизме почти все природные аминокислоты сначала передают аминогруппу на а-кетоглутарат в реакции трансаминирования с образованием глутамата и соответствующей кетокислоты. Затем глутамат подвергается прямому окислительному дезаминированию под действием глутаматдегидрогена-зы, в результате чего получаются а-кетоглутарат и аммиак; Б - при необходимости синтеза аминокислот и наличии необходимых а-кетокислот обе стадии непрямого дезаминирования протекают в обратном направлении. В результате восстановительного аминирования а-кетоглутарата образуется глутамат, который вступает в трансаминирование с соответствующей а-кетокислотой, что приводит к синтезу новой аминокислоты.
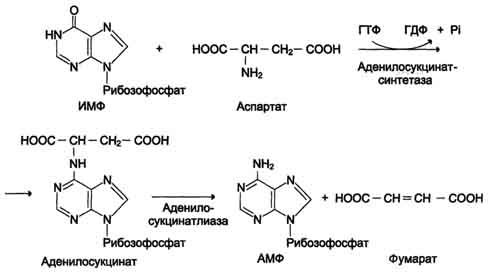
Схема А
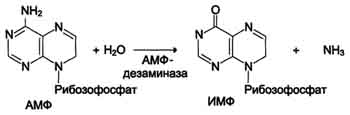
Схема Б.
Этот путь дезаминирования преобладает в мышцах при интенсивной работе, в результате которой накапливается молочная кислота. Выделяющийся аммиак предотвращает закисление среды в клетках, вызванное образованием лактата.
Билет 52-другой вариант
У человека основным способом дезаминирования является окислительное дезаминирование. Выделяют два варианта окислительного дезаминирования: прямоеи непрямое.
Прямое окислительное дезаминирование
Прямое дезаминирование катализируется одним ферментом, в результате образуется NH3 и кетокислота. Прямое окислительное дезаминирование может идти в присутствии кислорода (аэробное) и не нуждаться в кислороде (анаэробное).
1. Аэробное прямое окислительное дезаминирование катализируется оксидазами D-аминокислот (D-оксидазы) в качестве кофермента использующими ФАД, и оксидазами L-аминокислот (L-оксидазы) с коферментом ФМН. В организме человека эти ферменты присутствуют, но практически неактивны.
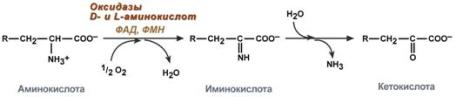
Реакция, катализируемая оксидазами D- и L-аминокислот
2. Анаэробное прямое окислительное дезаминирование существует только для глутаминовой кислоты, катализируется толькоглутаматдегидрогеназой, превращающей глутамат в α-кетоглутарат. Фермент глутаматдегидрогеназа имеется в митохондриях всех клеток организма (кроме мышечных). Этот тип дезаминирования теснейшим образом связан с трансаминированиемаминокислот и формирует с ним процесс трансдезаминирования (см ниже).
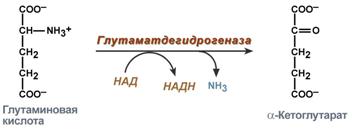
Реакция прямого окислительного дезаминирования
глутаминовой кислоты
Непрямое окислительное дезаминирование (трансдезаминирование)
Непрямое окислительное дезаминирование включает 2 этапа и активно идет во всех клетках организма.
Первый этап заключается в обратимом переносе NH2-группы с аминокислоты на кетокислоту с образованием новой аминокислоты и новой кетокислоты – этот перенос называется трансаминированиеи его механизм довольно сложен.
В качестве кетокислоты-акцептора ("кетокислота 2") в организме обычно используется α-кетоглутаровая кислота, которая превращается в глутамат("аминокислота 2").
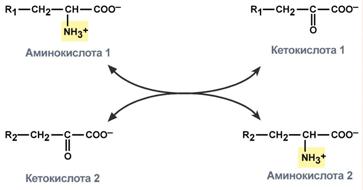
Схема реакции трансаминирования
В результате трансаминирования свободные аминокислоты теряют α-NH2-группы и превращаются в соответствующие кетокислоты. Далее их кетоскелет катаболизирует специфическими путями и вовлекается в цикл трикарбоновых кислот и тканевое дыхание, где сгорает до СО2 и Н2О. При необходимости (например, голодание) углеродный скелет глюкогенных аминокислот может использоваться для синтеза глюкозы в глюконеогенезе.
Второй этап состоит в отщеплении аминогруппы от аминокислоты 2 – дезаминирование. В организме человека дезаминированию подвергается только глутаминовая кислота. Второй этап осуществляется глутаматдегидрогеназой (перейти вверх).
В организме коллектором всех аминокислотных аминогрупп является глутаминовая кислота, и только она подвергается окислительному дезаминированию с образованием аммиака и α-кетоглутаровой кислоты. Фермент глутаматдегидрогеназаимеется в митохондриях всех клеток организма, кроме мышечных.
Учитывая тесную связь обоих этапов, непрямое окислительное дезаминирование называют трансдезаминирование.
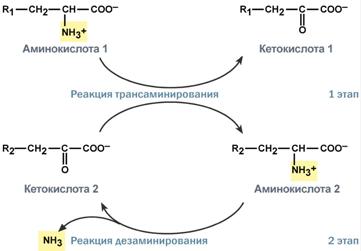
Схема обоих этапов трансдезаминирования
Если реакция идет в митохондриях печени, аммиак используется для синтеза мочевины, которая в дальнейшем удаляется с мочой. В эпителии канальцев почек реакция необходима для удаления аммиака в процессе аммониегенеза.
Так как НАДН используется в дыхательной цепи и α-кетоглутарат вовлекается в реакции ЦТК, то реакция активируется при дефиците энергии и ингибируется избытком АТФ и НАДН.
Процесс трансдезаминирования идет в организме непрерывно, потому что:
- сопряженные реакции трансаминирования и дезаминирования создают поток лишнего аминного азота из периферических клеток в печень для синтеза мочевины и в почки для синтеза аммонийных солей.
Билет 53
Для удаления аммиака есть два способа
Практически весь аммиак удаляется из организма через почки в виде мочевины, которая синтезируется в печени, и в виде образующися в эпителии канальцев почек солей иона аммония.
В клетки печени и почек аммиак попадает в составе глутаминаи аспарагина, глутаминовой кислоты, аланинаи в свободномвиде. Кроме этого, при метаболизме он образуется в большом количестве и в самих гепатоцитах.
В клетке глутамини аспарагиндезаминируются соответственно глутаминазойи аспарагиназойс образованием аммиака (точнее, иона аммония).
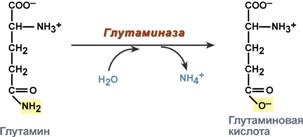
Реакция дезаминирования глутамина
Аланинвступает в реакцию трансаминирования. Образованный в результате реакции пируват идет в глюконеогенез или энергетический обмен. Параллельно образуется глутаминовая кислота.
В целом глутаминовая кислота в гепатоците может появляться тремя путями: 1) из крови, 2) при дезаминировании глутамина, 3) при трансаминировании α-кетоглутарата с аспартатом или аланином. Происхождение и дальнейшая ее судьба зависит от конкретных концентраций всех задействованных веществ. Обычно далее глутамат дезаминируется глутаматдегидрогеназой с образованиемаммиака.
Синтез мочевины
В печени весь удаляемый аммиак используется для синтеза мочевины. Увеличение синтеза мочевины наблюдается при распаде тканевых белков и азотистых соединений (голодание, воспалительные процессы, сахарный диабет) или при избыточном белковом питании. У младенцев и детей синтез мочевины может быть снижен по двум причинам: незрелость печени и активный синтез белков и нуклеиновых кислот при росте организма.
Реакции синтеза мочевины являются циклическим процессом и получили название орнитиновый цикл. Синтез мочевины начинается в митохондриях (первая и вторая реакции), оставшиеся три реакции идут в цитозоле. Для переноса цитруллина и орнитина через митохондриальную мембрану существуют специальные переносчики.
Как побочный продукт орнитинового цикла образуется фумаровая кислота, переносимая обратно в митохондрии. Здесь в реакциях ЦТК из нее образуется оксалоацетат, который трансаминируется с глутаматом до аспартата, выходит в цитозоль и вновь реагирует с цитруллином.
В образовании одной молекулы мочевины участвует 1 молекула NH4+, 1 молекула CO2, аминогруппа 1 молекулы аспарагиновой кислоты, затрачивается 4 макроэргических связи трех молекул АТФ.
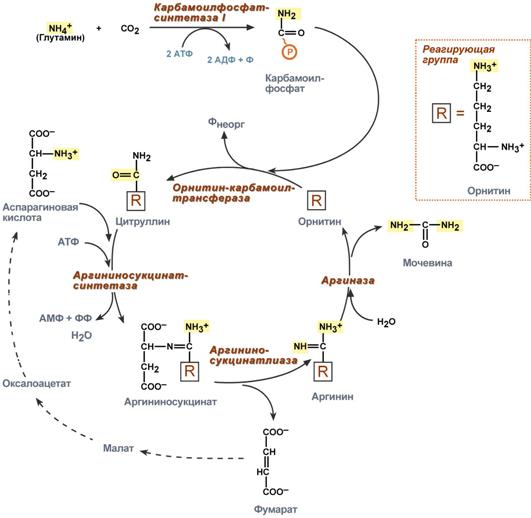
Реакция синтеза карбамоилфосфата и орнитиновый цикл
Синтез аммонийных солей
Непосредственный синтез аммонийных солей или аммониегенезпроисходит в просвете канальцев почек из секретируемых сюда аммиака и ионов водорода и фильтрующихся органических и неорганических анионов первичной мочи. Около 10% всего аммиака выводится почками в виде аммонийных солей.
Часть глутамина крови, не задержавшаяся в печени, достигает почек. В эпителиальных клетках почечных канальцев, в основном в дистальных канальцах, имеется фермент глутаминаза, гидролизующая амидную группу с образованием глутамата. Глутамат, в свою очередь, дезаминируется глутаматдегидрогеназой.
Параллельно в эпителии происходят процессы клеточного дыхания, сопросождающиеся образованием угольной кислоты, которая диссоциирует на ион Н+ и карбонат-ион НСО3−. Ионы водорода секретируются в первичную мочу, карбонат-ионы – в кровь.
Выделяемый аммиак диффундирует в просвет канальца, где соединяется с ионом Н+, образуя ионы аммония NH4+. Они связываются с неорганическими (фосфаты, хлориды, сульфаты) или с органическими анионами (уксусной, щавелевой, молочной кислот).
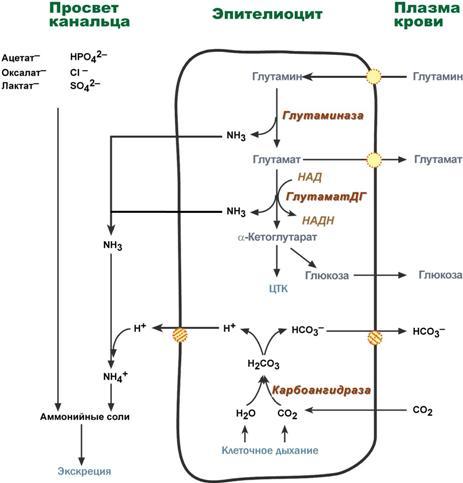
Реакции синтеза аммонийных солей
Билет 53-другой вариант
Аммиак образуется в ходе следующих процессов:
1) дезаминирования аминокислот;
2) дезаминирования биогенных аминов (гистамина, серотонина, цисте-амина и т. д.);
3) дезаминирования пуриновых оснований (гуанина и аденина);
4) дезаминирования амидов аминокислот (аспарагина к глутамина);
5) распада пиримидиновых оснований (урацила, тимина, Цнтозина). Аммиак — очень токсичное соединение, особенно для нервных клеток.
При накоплении его возникает возбуждение нервной системы. Поэтому в тканях Существуют механизмы его обезвреживания. К ним относятся: 1) образование мочевины; 2) восстановительное аминирование, или трансреамини-робание; 3) образование амидов аминокислот — аспарагина и глутамина; 4) образование аммонийных солей.
Основной путь обезвреживания аммиака — синтез мочевины. Еще в прошлом веке русские ученые М. В. Ненцкий и С. С. Салаз-кин показали, что в печени происходит образование мочевины из аммиака и углекислоты. Кребс и Гензенлейт установили, что синтез мочевины представляет собой циклический процесс, в котором каталитическую роль играет орнитин. Коген и Ратнер выяснили, что начальной реакцией этого цикла является синтез карбамоил фосфата. На рис. 58 приведен цикл образования мочевины. На образование одной молекулы мочевины расходуется три молекулы АТФ. Мочевина — безвредное для организма соединение. Главным местом ее образования в организме является печень, где есть все ферменты мочевниообразовання. В головном мозгу имеются все ферменты синтеза мочевины, кроме карбамоилфосфатсинтетазы, поэтому в нем мочевина не -образуется. Нарушение функции печени ведет к снижению мочевинообразования, и содержание мочевины в крови и выделение ее с мочой падает.
Восстановительное аминнрование — малоэффективный процесс связывания аммиака, так как необходимы значительные количества 2-оксоглута-рата.
Образование аспарагина н гяутамниа является важным вспомогательным путем связывания аммиака. Оно протекает с участием аспарагинсин-тетазы и глутаминсинтетазы по уравнениям:
Этот процесс активен в нервной и мышечной тканях, в почках.
Образование аммонийных солей. Глутамин и в меньшей степени аспа-рагии считают своеобразной транспортной формой аммиака, так как, образуясь в тканях, они с кровью попадают в почки, где подвергаются гидролизу под действием специфических ферментов — глутаминазы и аспарагиназы:
Освободившийся в канальцах почек аммиак нейтрализуется с образованием солей аммония
NH3 + H+ + CI-—+NH4C1 которые выделяются с мочой.
Билет 54
Образование н распад медиаторов. Медиаторы образуются в нервной ткани и ряде других клеток. Нейромедиаторы* образующиеся в нервных окончаниях, участвуют в передаче нервного импульса на другие нервные клетки или периферические органы и ткани Тканевые медиаторы участвуют в межтканевой регуляции обмена веществ.
В образовании ряда медиаторов существенное значение имеет реакция декарбоксилирования аминокислот, которая катализируется специфическими ферментами декарбокснлазачи, содержащими в качестве кофермента пиридоксальфосфат:
Продуктом декарбоксилироиания являются амины, обладающие высокой биологической активностью, поэтому их называют биогенными аминами. Большинство медиаторов принадлежат к этой группе соединений.
Почти все ткани и органы содержат гистамин. Особенно много его в тканях легких и в коже, имеется он в спинном мозге и подкорковых образованиях головного мозга. Большое количество гистамина образуется и депонируется в тучных клетках соединительной ткани, в которых он связан в виде белково-гепаринового комплекса. Освобождается он нз тучных клеток под действием веществ, .которые называются либераторами гистамина. Большое количество гистамина образуется в слизистой желудка, где он действует на секрецию пепсина и соляной кислоты. В крови гистамин связан с гранулами базофилов и эозинофнлов. Небольшие количества его всегда имеются в плазме крови и других биологических жидкостях.
В больших количествах гистамин освобождается при патологических Процессах, являясь медиатором аллергических реакций
Образование серотонина. Серотонин образуется из триптофана:
Примерно 90% серотонина взрослого человека содержится в «энтерохромаффинных клетках кишечника. Остальная часть его находится в тучных клетках кожи, селезенке, печени, почках, легких. Много серотонина в тромбоцитах крови и в центральной нервной системе. В частности, он образуется в сером веществе коры головного мозга, в гипоталамусе. Серотонин играет роль медиатора в нервной системе и местного регулятора функций периферических органов и тканей.
Образование у-аминомасляной кислоты (ГАМК). ГАМК образуется из глутаминовой кислоты под действием глутаматдекарбоксилазы:
Синтез протекает в тормозных синапсах нервной системы, являясь их медиатором. Наибольшие количества ГАМК содержатся в подкорковых образованиях головного мозга (в черной субстанции, бледном шаре, гипоталамусе). В периферических органах она встречается в виде следов.играет роль нейрогуморального ингибитора.
Тирамин, b-(n-оксифенил)-этиламин, HO-C6H4-CH2-CH2-NH2, органическое вещество из группы биогенных аминов. Тирамин найден в спорынье, гниющих тканях, сыре. Отсюда и его название (от греч. tyros – сыр). Физиологически активен (в связи с сосудосуживающим действием повышает кровяное давление, влияет на процессы возбуждения и торможения в нервной системе) и токсичен. Образуется из аминокислоты тирозина под действием бактериальных декарбоксилаз, в частности при гнилостных процессах в кишечнике млекопитающих животных и человека. Обезвреживание избыточного тирамина в живом организме осуществляется в результате его окисленияферментом моноаминоксидазой (МАО).[1]
Билет 54 –другой вариант
