Определение содержания кислоты в растворе
Приборы и материалы
2. Кондуктометр
3. Магнитная мешалка
4. Бюретка на 50 мл
5. Воронка
6. Стакан для титрования емкостью 100 мл
7. Мерный цилиндр на 100 мл
8. Стандартный раствор 0,1 м NaOH
Выполнение работы
1. Подготовка прибора к работе.
Нажатием кнопки на передней панели включают кондуктометр, при этом зажигается сетевая контрольная лампа. Прибор прогревают в течение 2-3 минут. Чтобы прибор давал точные показания, необходимо убедиться в чистоте его электрода (удельная электропроводность в чистой дистиллированной воде должна находиться в интервале 5-6 микросименсов по шкале прибора).
Для этого шкалу прибора необходимо отградуировать в выбранном интервале измерений. Поворотом рукоятки пределов измерения устанавливают диапазон измерения до 15 μς (микросименсов), находящийся на нижней стороне шкалы. Нажимают кнопку калибровки и, если измерительная стрелка не совпадает точно с красной меткой шкалы, ее корректируют поворотом рукоятки калибровки, удерживая все время кнопку в нажатом состоянии. После установки стрелки освобождают кнопку калибровки. Электрод погружают в стаканчик с чистой дистиллированной водой так, чтобы жидкость полностью покрывала платиновые кольца электрода. Если показания стрелки соответствуют 6-7 μς , электрод чист и прибор готов к работе.
Одновременно этим контролируют и чистоту дистиллированной воды (загрязненная вода имела бы удельную электропроводность 200-500 микросименсов).
Измеряя таким способом электропроводность водных смывов с поверхности пищевых емкостей можно просто проверять их чистоту, что имеет важное значение в пищевой технологии.
Техника определения
Полученный от лаборанта в мерной колбе емкостью 100 см3 раствор неизвестной концентрации доводят водой до метки и тщательно перемешивают.
Бюретку заполняют до верхней метки стандартным раствором щелочи точной концентрации и, убрав воронку, устанавливают уровень титранта на нулевом делении.
Мерным цилиндром отмеривают 60 см3 анализируемого раствора в стакан для титрования, ставят его на магнитную мешалку для перемешивания раствора во время титрования и погружают глубоко в раствор электроды кондуктометра. Поворачивая рукоятку пределов измерения, устанавливают предполагаемый диапазон измерения от 50 до 150 микросименсов.
Затем вновь калибруют шкалу в этом диапазоне, устанавливая стрелку на красной метке (как указано выше). Затем освобождают кнопку и отсчитывают по шкале значения удельной электропроводности раствора до начала титрования. Результаты заносят в лабораторный журнал.
Затем, включив мешалку, начинают титрование, приливая в стаканчик щелочь из бюретки по 0,5 см3; при этом записывают показания прибора. Сделав еще три замера после точки эквивалентности, титрование прекращают.
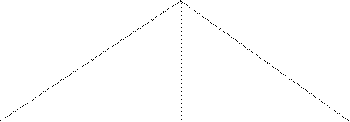
По полученным данным строят кривую титрования и находят ТЭ. Для этого на оси абсцисс откладывают объемы стандартного раствора щелочи, идущей на титрование (отсчет по шкале бюретки), на оси ординат – соответствующие им значения удельной электропроводности (отсчет по шкале кондуктометра). Из точки пересечения двух ветвей на ось абсцисс опускают перпендикуляр; полученное значение (см3) подставляют в формулу:
Нкисл. = 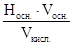 ,
,
где Vкисл., Нкисл. – объем (см3) и нормальность раствора кислоты,
Носн. – нормальность раствора щелочи (0,1 н. стандартный раствор),
Vосн. – объем щелочи, пошедшей на титрование, см3
х(μS)

 |
 |
0 т.э.
 1 2 3 4 5 6 7 8 9 10 V
1 2 3 4 5 6 7 8 9 10 V
(титранта)
см3
Рис. 11. Кривая титрования сильной кислоты
неизвестной концентрации сильным основанием
Вопросы для самопроверки
1. От таких факторов зависит величина окислительно-восстановительного потенциала
2. Какие электроды используются при измерении потенциала (Э.Д.С.).
3. Почему потенциал хингидронного электрода является обратной химической функцией рН раствора.
4. Объясните почему потенциал электродов сравнения (каломельный хингидронный при постоянной, температуре есть величина постоянная.)
5. Как определяют активную и общую кислотность пищевых систем.
6. От чего зависит ход кондуктометрических кривых.
7. Как рассчитывают величины удельной, эквивалентной и мольной электропроводности. В каких единицах они измеряются.
8. С помощью каких электродов измеряют концентрацию ионов ионометрическим методом анализа. Какие электроды являются при этом индикаторными.
9. Сущность ионометрического метода определения нитратов.
10. Вольт – амперометрические методы анализа. Классификация.
11. Сущность полярографического метода анализа. Система электродов.
12. Какие характеристики можно рассчитать с помощью уравнения Ильковича.
13. Что такое остаточный, диффузионный и кинетические токи в полярографии.
14. Приведите характерную зависимость величины тока от напряжения. Какую качественную характеристику несет эта зависимость.
Как определяют катионы металлов полярографическим методом.
ОПТИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Спектральный анализ
Спектральный анализ основан на взаимодействии светового электромагнитного излучения с веществом. Первичное излучение источника света, складываясь с колебаниями атомов и молекул, преобразуется во вторичные световые волны определенной длины. Такое взаимодействие может иметь формы поглощения, отражения или испускания света, образуя атомные и молекулярные спектры.
Различные типы электромагнитных излучений показаны на схеме 1.
