Вычисление рН водных растворов
сильных кислот:рН = – lga(H+) = – lg (c(H+) / f(Н+))
сильных оснований:рН = 14 + lga(OH¯) = 14 + lg (c(OH¯) f(OH¯))
слабых кислот:рН = – ½(рKкислоты – lgc) = – ½Kкислоты – ½lgc
слабых оснований:рН = 14 – ½рKоснования + ½lgc
солей, образованных сильным основанием и слабой кислотой:рН = 7 + ½pKкислоты + ½lgcсоли
солей, образованных слабым основанием и сильной кислотой:рН = 7 – ½Kоснования – lgcсоли
солей, образованных слабым основанием и слабой кислотой:рН = 7 + ½pKкислоты + ½pKоснования
кислого буферного раствора:
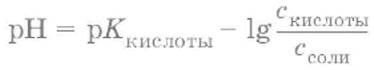
щелочного буферного раствора:
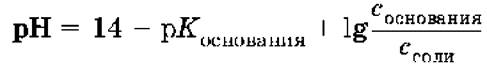
Вычисление буферной емкости.Емкость буферного раствора определяется количеством сильной кислоты или сильного основания, которое необходимо добавить к 1 л буферного раствора, чтобы изменить его значение рН на единицу.
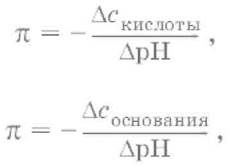
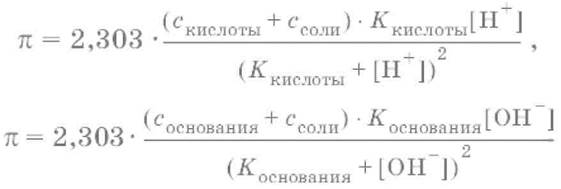
Гетерогенное равновесие: осадок – насыщенный раствор малорастворимого соединения.Гетерогенное равновесие между осадком малорастворимого соединения и его ионами в насыщенном водном растворе может быть представлено следующим уравнением:
KtmAnn↓ ↔ mKtn++ nAnm‑
[Ktn+] = m s; [Anm‑] = n • s
Константа равновесия обратимой реакции осаждения‑растворенияназывается произведением растворимости Ks(или ПР) и выражается следующим образом:
Ks = a(Ktn+)ma(Anm‑)n= (f(Ktn+) x [Ktn+])m • (f(Anm‑)[Anm‑])n= (ms)m(ns)n• f(Ktn+)m• f(Ann‑)n= nnmmsm+n • f(Ktn+)m• f(Anm‑)n, или Ks = nn• mm• sm+n
Растворимость – это свойство вещества образовывать гомогенные системы с растворителем. Молярная растворимость малорастворимого вещества (s), моль/л, выражается следующим образом:
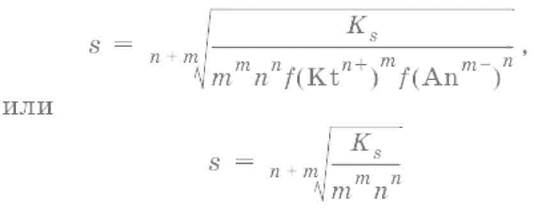
Зная молярную растворимость соединения KtmAnn, легко вычислить его растворимость в г/л ρ по формуле:
ρ = s •M(KtmAnn)
Массу малорастворимого вещества в любом объемеможно рассчитать по формуле:
m(KtmAnn) = s(KtmAnn) • M(KtmAnn) x Vр‑ра
Условие образования и растворения осадка.Осадок не образуется или растворяется, если произведение концентраций ионов осадка в растворе меньше величины произведения растворимости.
[Ktn+]m[Anm‑]n< Ks(KtmAnn)
Осадок образуется или выпадает, если произведение концентраций ионов осадка в растворе больше величины произведения растворимости.
[Ktn+]m[Anm‑]n> Ks(KtmAnn).
Равновесия в окислительно‑восстановительных системах.Для обратимой окислительно‑восстановительной реакции
Oх + nē ↔ Red
Равновесный потенциал Eox/red со стандартным потенциалом редокс‑пары Eox/red и активностью окисленной и восстановленной формы связан уравнением Нернста:
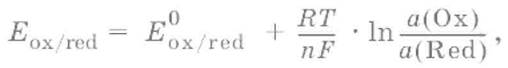
где R – универсальная газовая постоянная, равная 8,314 Дж/моль К, Т – температура по шкале Кельвина, К, T – число Фарадея, равное 96485 Кл/моль, а(Ох) – активность окисленной формы, a(Red) – активность восстановленной формы.
При подстановке в уравнение значений универсальной газовой постоянной, числа Фарадея, температуры Т =298 К и замены натурального логарифма на десятичный получается уравнение для расчета значения равновесного электродного потенциала редокс‑пары при 25°C:
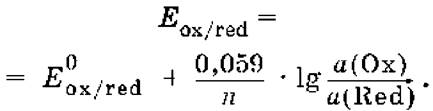
Если в окислительно‑восстановительных реакциях принимают участие ионы водорода, то уравнение Нернста выглядит следующим образом:
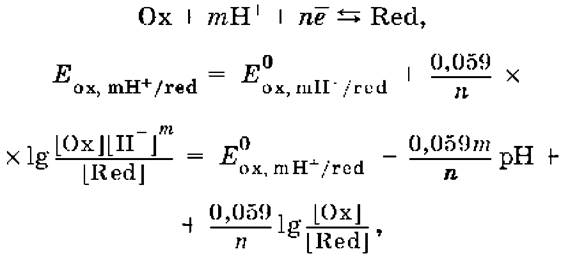
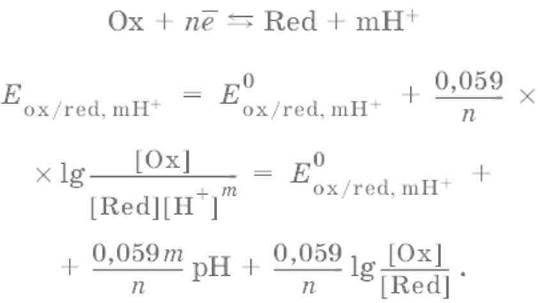
Если окисленная или восстановленная форма окислительно‑восстановительной полуреакции является малорастворимым соединением, то в формулу для вычисления равновесного потенциала такой системы входит величина произведения растворимости этого соединения.
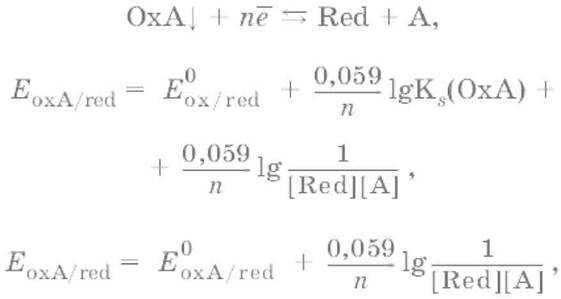
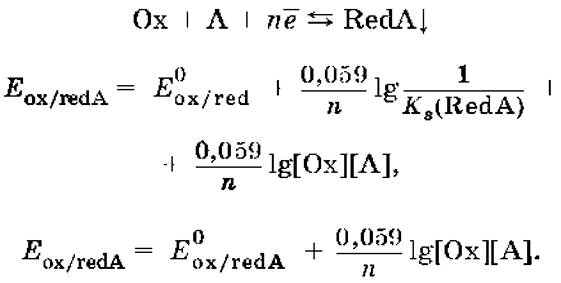
Если в окислительно‑восстановительной полуреакции окисленной формой является комплексное соединение OxLm, характеризующееся константой устойчивости β(OxLm), то равновесный окислительно‑восстановительный потенциал вычисляется по уравнению:
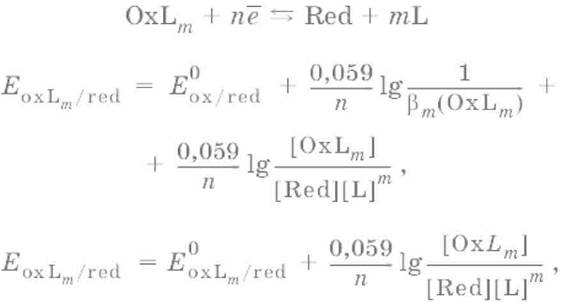
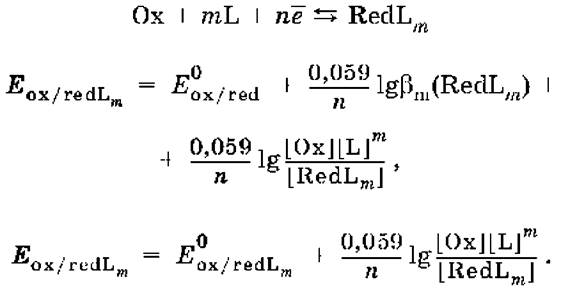
Направление и глубина протекания окислительно‑восстановительных реакций. Обратимая окислительно‑восстановительная реакция
аОх1 + bRed1 ↔ аОх2 + bRed2протекает в прямом направлении, если ΔЕ0= Е0Ox1/Red2 – Е0Ox2/Red1 > 0, И В обратном направлении, если ΔЕ0<0.
Глубина протекания реакции, т. е. степень превращения исходных веществ в продукты реакции, определяется константой равновесия.
Для окислительно‑восстановительной реакции константа равновесия с потенциала‑
ми участвующих в реакции редокс‑пар связана уравнением:
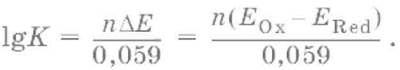
Количественный анализ
