Тема 1. Химическая термодинамика
ХИМИЯ
Курс лекций для студентов ЗиДО и МИППС специальностей 141108, 271101 и направлений 131000, 140100, 140400, 141200, 151000, 151900, 190600, 220400, 220700, 270800, 280700
Часть I.
Краснодар
Составители: д-р хим. наук, проф. Л.А. Бадовская;
д-р хим. наук, проф. В.В. Посконин;
канд. хим. наук, доц. Л.В. Поварова;
канд. хим. наук, доц. Л.А. Солоненко;
канд. хим. наук, доц. Л.Н. Сороцкая;
канд. хим. наук, доц. М.А. Тлехусеж;
канд. хим. наук, доц. З.И. Тюхтенева
УДК 669:54(07)
Химия: Курс лекций для студентов ЗиДОи МИППСспециальностей 141108, 271101 и направлений 131000, 140100, 140400, 141200, 151000, 151900, 190600, 220400, 220700, 270800, 280700. Часть I. / Сост. Л.А. Бадовская, В.В. Посконин, Л.В. Поварова, Л.А. Солоненко, Л.Н. Сороцкая, М.А. Тлехусеж, З.И. Тюхтенева: Кубан. гос. технол. ун-т. Кафедра общей химии. – Краснодар, 2013. – 42 с.
Составлено в соответствии с государственным стандартом высшего профессионального образования 3-го поколения.
© 

 КубГТУ, 2013
КубГТУ, 2013
Содержание
Тема 1. Химическая термодинамика………………………………………..4
Тема 2. Скорость химических реакций и методы ее регулирования…......8
Тема 3. Химическое равновесие…………………………………………..11
Тема 4. Гетерогенные химические системы и поверхностные явления
в них (спецраздел)……………………...………….……...……………….13
Тема 5. Растворы. Кислотно-основные свойства веществ.Реакции
обменного разложения в растворах электролитов и их использование
в химическом анализе ……...……………………………………………..16
Тема 6. Жесткость воды и реакции солей жесткости в водных раство-
рах………………………………………………………………………….. 25
Тема 7. Соединения кальция и вяжущие вещества на их основе (спец-
раздел)…………………………...………………………………………….27
Тема 8. Окислительно-восстановительные реакции и их использова-
ние в химическом анализе…….……………………… ………………..29
Тема 9. Электрохимические системы и процессы..………………………35
Приложение…………………….……………………………………………37
Тема 2. Скорость химических реакций и методы ее регулирования
Рекомендуемая литература:[1], гл. 6, 6.2; [2], гл. 7; [5], гл. V.
Скорость химических реакцийотражает число актов химического взаимодействия, происходящих в единице объема (для гомогенных реакций) или на единице поверхности раздела фаз (для гетерогенных реакций) в единицу времени.
Средняя скорость химического процесса выражается изменением концентрации (ΔС) веществ – реагентов или продуктов реакции в единицу времени.
Полная последовательность всех элементарных стадий в процессе взаимодействия отражает механизм химических реакций.
Число частиц, участвующих в каждом элементарном химическом акте, показывает молекулярность реакции.
Главные факторы, влияющие на скорость реакции:природа реагентов; их агрегатное состояние; концентрация реагентов; давление (для реакций с участием газов), температура, специальные факторы (катализ, инициирование, ингибирование), площадь раздела фаз (для гетерогенных реакций).
Влияние концентрации.Химическое взаимодействие веществ возникает лишь при активном столкновении их молекул, поэтому, чем больше концентрация реагирующих веществ, тем выше вероятность активных столкновений и, следовательно, скорость реакции. Зависимость скорости реакции от концентрации выражается законом действия масс:
Скорость гомогенной химической реакции при данной температуре прямо пропорциональна произведению концентраций реагирующих веществ или парциальных давлений газообразных веществ, взятых в степенях, равных их стехиометрическим коэффициентам.
Для гомогенной реакции общего вида аА + bВ = сС (А и В – реагенты, С – продукт реакции, а, b и с – стехиометрические коэффициенты), протекающей в истинных растворах, выражение ее скорости описывается уравнением:
V = k· [A]а·[B]b или V = k · CaA · CbB, моль/л·с,
где [A], [B] или CA, CB – молярные концентрации веществ А и В, (моль/л); k – коэффициент пропорциональности, называемый константой скорости.
Для этой же реакции, протекающей в газовой фазе, скорость реакции будет выражена уравнением:
V = k · РaA · РbB , моль/л·с,
где РaA и РbB – парциальные давления веществ А и В.
Константа скорости – это скорость реакции при концентрациях реагирующих веществ, равных единице. Константа скорости зависит от химической природы веществ, температуры и специального фактора (присутствия катализатора, инициатора или ингибитора), но не зависит от концентрации реагирующих веществ или создаваемого ими парциального давления (в газовых реакциях).
Скорость гетерогенной реакции не зависит от концентрации твердого вещества, потому что такая реакция проходит только на поверхности раздела фаз. Например, при одинаковой степени измельчения поверхность раздела будет постоянной и уравнение скорости гетеро-генной реакции СО2(Г) + С(К) = 2СО(Г) записывается так:
V = k · [СО2].
Влияние температуры. Экспериментально установлено, что в некотором интервале температур скорость реакции при повышении температуры на каждые 10о увеличивается в число раз, равное температурному коэффициенту γ (правило Вант-Гоффа),т. е.
VT2 = VT1 · γ 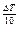 ,
,
где VT2 и VT1 – скорости реакции при температурах Т1 и Т2; ΔT – изменение температуры, равное Т2–Т1; γ – температурный коэффициент реакции, в большинстве случаев имеющий значения от 2 до 4.
Температурный коэффициент γ показывает, во сколько раз изменится скорость реакции при изменении температуры на 10 оС: γ = VT2/VT1 при ΔT = 10.
Влияние температуры на скорость реакции весьма существенно. Химическое взаимодействие происходит при столкновении только тех молекул, энергия которых выше энергии активации (Еакт).
Энергия активации (кДж/моль) – это количество энергии, которое необходимо приложить к 1 молю вещества, чтобы произошло превращение исходных веществ в продукты реакции. Иначе говоря, энергия активации – это разность между наименьшим избыточным запасом энергии, необходимым для взаимодействия молекул, и их среднестатичстическим запасом энергии.
Энергия активации связана с константой скорости реакции уравнением Аррениуса:
K = A · e 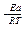 ,
,
где А – предэкспоненциальный множитель, учитывающий строение вещества; R – универсальная газовая постоянная, равная 8,314 Дж/моль.К; Т – абсолютная температура, К; Еакт – энергия активации процесса, Дж/моль; е – основание натурального логарифма.
Влияние катализатора.Катализаторы– это вещества, которые резко изменяют скорость термодинамически возможной химической реакции, участвуют в ней на промежуточных стадиях, но в конце реакции остаются химически неизменными. Катализ – явление изменения скорости реакции при внесении катализатора. По фазовому состоянию реагентов и катализатора различают гомогенный катализ, при котором они находятся в одной и той же фазе, и гетерогенный катализ, при котором катализатор образует самостоятельную фазу.
По действию различают положительные катализаторы, которые увеличивают скорость реакции, и отрицательные катализаторы, уменьшающие ее.
Положительные катализаторы снижают величину энергии активации процесса. Так, в реакции СН3СНО → СН4 + СО без участия катализатора энергия активации составляет 216,7 кДж/моль, тогда как в присутствии паров иода (катализатор) Еакт = 143,0 кДж/моль. Отрицательные катализаторы повышают энергию активации всей реакции.
Изменение одного из условий в равновесной системе (температуры, давления, концентрации) вызывает смещение химического равновесия в направлении того процесса, который противодействует произведенному изменению.
Так, в системе СН4(Г) + СО2(Г) ⇄ 2СО(Г) + 2Н2(Г), ΔΗ>0 равновесие смещается вправо, т.е. в направлении прямой реакции в следующих случаях:
– при повышении температуры, т.к. при этом равновесие должно смещаться в сторону эндотермического процесса;
– при увеличении концентрации метана и (или) оксида углерода (IV) или при уменьшении концентрации оксида углерода (II) и водорода, что вытекает из закона действия масс;
– при понижении давления в системе, поскольку количество газообразных молекул продуктов прямой реакции преобладает над количеством молекул исходных веществ.
В случае реакции, протекающей в растворе, процесс обратим, если хотя бы один реагент и один продукт реакции проявляют свойства слабого электролита. Например, в обратимой реакции гидролиза ацетата калия СН3СООК + Н2О ⇄ СН3СООН + КОН, ΔΗ>0 реагентами – слабыми электролитами являются: в прямой реакции – вода, в обратной реакции нейтрализации – уксусная кислота. При этом равновесие смещено в сторону образования более слабого электролита – воды, т.е. влево. Для смещения равновесия вправо следует увеличить концентрацию воды (разбавить раствор), уменьшить концентрацию КОН (путем добавления кислоты, связывающей образующиеся при гидролизе ионы ОН¯), повысить температуру (поскольку реакция гидролиза эндотермична). Изменением давления невозможно сместить равновесие в данной реакции, т.к. в ней не участвуют газообразные вещества.
Водородный показатель среды
Водородный показатель среды(рН) – это отрицательный десятичный логарифм концентрации ионов водорода: рН = −lg[Н+]. Он служит для характеристики кислотно-основных свойств растворов электролитов. Его значения изменяются в интервале от 0 до 14. В нейтральной среде рН = 7, в кислой рН < 7, в щелочной рН > 7. Значения рН в зависимости от концентрации протонов в растворах приведены в Приложении А, таблица А-19.
Кислотно-основные характеристики среды можно определить с помощью индикаторов. Индикаторы кислотно-основного взаимодействия – это слабые органические кислоты или основания, которые изменяют окраску в зависимости от рН среды. Например, кислотный индикатор диссоциирует по схеме:
ОН−
HInd  H+ + Ind−
H+ + Ind−
окраска I Н+ окраска II
На состояние равновесия влияет концентрация ионов [Н+] и [ОН−] в растворе. При увеличении концентрации протонов равновесие смещается справа налево, что влечет за собой переход окраски II в окраску I. В присутствии оснований ионы гидроксогруппы ОН− связывают ионы Н+ в слабый электролит Н2О, при этом равновесие смещается вправо и происходит переход окраски I в окраску II. В нейтральной среде, как правило, появляется смешанная окраска I и II.
Гидролиз солей
Гидролизомназывается взаимодействие вещества с водой, при котором вещество разлагается под действием воды, и составные части вещества соединяются с составными частями воды с образованием слабого электролита. Гидролизу подвергаются соединения различных классов, но наиболее распространенным случаем гидролиза является гидролиз растворимых солей.
Гидролиз соли – это процесс взаимодействия ионов соли, образовавшихся под действием воды в результате электролитической диссоциации, с составными частями воды, в результате чего образуется слабый электролит.
В большинстве случаев гидролиз – это обратимый процесс, в большинстве случаев он не проходит до конца. Реакцией, обратной гидролизу, является нейтрализация. Гидролиз – эндотермический, а нейтрализация – экзотермический процесс. В результате гидролиза в большинстве случаев изменяется рН раствора соли. Значение рН растворов солей определяется химическим составом гидролизуемой соли.
Гидролизу подвергаются только те соли, в состав которых входит ион от слабого электролита. Это соли, образованные сильным основанием и слабой кислотой (в результате гидролиза рН раствора больше 7), слабым основанием и сильной кислотой (в результате гидролиза рН меньше 7), слабым основанием и слабой кислотой (в результате гидролиза рН примерно равно 7). Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются, так как в их составе нет иона слабого электролита, и не соблюдается главное требование обменных реакций в растворах – необходимость образования слабого электролита. В их растворах рН равно 7.
Если соль образована слабыми электролитами, которые являются нерастворимыми или неустойчивыми и разлагаются с образованием летучих продуктов, то гидролиз протекает необратимо, т.е. приводит к разложению соли.
Количественной характеристикой гидролиза является степень гидролиза (α). Это отношение числа подвергшихся гидролизу молекул (n) к общему числу молекул соли в растворе (N):
α = n/N
Для солей, образованных сильным основанием и слабой кислотой или слабым основанием и сильной кислотой, степень гидролиза < 5 %, т. е. большинство молекул соли находятся в негидролизованном виде. Для солей, образованных слабым основанием и слабой кислотой, степень гидролиза превышает 90 %. Степень гидролиза зависит от температуры и концентрации раствора.
Поскольку гидролиз – эндотермический процесс, то с ростом температуры он усиливается. С разбавлением раствора степень гидролиза повышается, так как увеличивается степень диссоциации соли, а следовательно, концентрация ее ионов, ведущих гидролиз.
Последовательность составления уравнений реакции гидролиза солей:
1. Записывается уравнение электролитической диссоциации соли и определяется, каким по силе основанием и какой по силе кислотой образована данная соль; над ионами указать: от сл. эл. и от с. эл. (см. Приложение А., таблицы А-16 и А-20).
2. Составляется краткое ионно-молекулярное уравнение гидролиза. Для этого следует написать реакцию взаимодействия иона слабого электролита с одной молекулой воды; при этом сразу получится краткое ионно-молекулярное уравнение реакции гидролиза.
3. На основании краткого ионно-молекулярного уравнения пишется молекулярное уравнение, в котором исходные вещества известны (соль и вода), а молекулы конечных продуктов составляются путем связывания ионов, образовавшихся при гидролизе, с теми ионами, которые не участвовали в реакции гидролиза (т.е. ионами от сильных электролитов).
Пример:
ион сильного ион слабого
электролита электролита – ведет гидролиз
1. Na2CO3  2 Na+ + CO32−
2 Na+ + CO32−
↓ ↓
NaOH H2CO3
сильный слабый
электролит электролит
2. CO32− + H−OH  HCO3− + OH− рН > 7
HCO3− + OH− рН > 7
сл. сл.
гидролиз
3 Na2CO3 + H2O  NaHCO3 + NaOH рН > 7
NaHCO3 + NaOH рН > 7
нейтрализация
Данная реакция обратима, так как H2O и HCO3− – слабые электролиты. Аналогичным образом пишутся уравнения реакций гидролиза солей других типов.
Для прохождения нескольких стадий и достижения большей степени гидролиза требуются дополнительные условия – избыток воды, отвод образующихся продуктов, нагревание.
Список рекомендуемой литературы
1. Глинка Н.Л. Общая химия. – М.: Юрайт, 2013; М.: Интеграл-пресс, 2009 и др. годы изд.
2. Коровин Н.В. Общая химия. – М.: Высшая школа, 2013 и др. годы изд.
3. Глинка Н.Л. Задачи и упражнения по общей химии. – Л.: Химия, 2010 и др. годы изд.
4. Денисов В.В., Дрововозова Т.И., Лозановская И.Н. Химия. – М.; Ростов-н/Д: Издат. центр. "Март Т", 2008 и др. годы изд.
5. Гельфман М.И., Юстратов В.П. Химия. – СПБ.: Лань, 2008 и др. годы изд.
6. Рябов В.Д. Химия нефти и газа. – М.: Изд-во "Техника". ТУМА ГРУПП, 2010 и др. годы изд.
Приложение
Классификация электролитов по степени их диссоциации
| Вещество | Сильные электролиты α >30% | Слабые электролиты α <30% |
| Основания | KOH, NaOH, Ba(OH)2, TiOH | NH4OH, все нерастворимые основания и амфотерные гидроксиды |
| Кислоты | HСl, HBr, HI, HNO3, H2SO4, H2MnO4, HСlO3, HClO4 | HF, H2CO3, H2SO3, HNO2, H3PO4, HCN, H2S, H2SiO3, большинство органических кислот (CH3COOH и др.) |
| Соли | все растворимые соли – средние, кислые и гидроксо-нитраты (основные соли, содержащие группу NO3) | все малорастворимые и нерастворимые соли –основные (кроме гидроксонитратов) и средние |
Константы диссоциации водных растворов некоторых кислот при 25оС
| Электролит | Формула | Значение константы диссоциации КД |
| Азотная | HNO3 | 4,36 ∙101 |
| Азотистая | HNO2 | 4 ∙10-1 |
| Борная | H3BO3 | (1)5,8 ∙10-10 (2)1,8 ∙10-10 (3)1,6 ∙10-14 |
| Бромноватистая | HBrO | 2,1 ∙10-9 |
| Бромоводородная | HBr | 1 ∙109 |
| Йодноватистая | HIO | 2,3 ∙10-11 |
| Йодноватая | HIO3 | 1,7 ∙10-1 |
| Йодная | HIO4 | 2,3 ∙10-2 |
| Йодистоводородная | HI | 1 ∙1011 |
| Кремниевая | H2SiO3 | (1)2,2 ∙10-10 (2)1,6 ∙10-12 |
| Малеиновая | HOOCCH=CHCOOH | (1)1,2 10-2 (2)5,9 ∙10-7 |
| Марганцовая | HMnO4 | 2 ∙102 |
Продолжение таблицы
| Электролит | Формула | Значение константы диссоциации КД |
| Муравьиная | HCOOH | 1,77 ∙10-4 |
| Мышьяковистая | HAsO2 | 6 ∙10-10 |
| Мышьяковая | H3AsO4 | (1) 5,89 ∙10-3 (2) 1,05 ∙10-7 (3) 3,89 ∙10-12 |
| Ортофосфорная | H3PO4 | (1)7,52 ∙10-3 (2)6,31 ∙10-8 (3)1,26 ∙10-12 |
| Серная | H2SO4 | (1)1 ∙103 (2)1,2 ∙10-2 |
| Сернистая | H2SO3 | (1)1,58 ∙10-2 (2)6,31∙ 10-8 |
| Сероводородная | H2S | (1)6 ∙10-8 (2)1∙ 10-14 |
| Угольная | H2CO3 | (1)4,45 ∙10-7 (2)4,69 ∙10-11 |
| Уксусная | CH3COOH | 1,754 ∙10-5 |
| Фтороводородная | HF | 6,01 ∙10-4 |
| Хлорноватистая | HClO | 5,01 ∙10-8 |
| Хлороводородная | HCl | 1 ∙107 |
| Хромовая | H2CrO4 | (1)1∙ 101 (2)3,16∙10-7 |
| Циановодородная | HCN | 7,9 ∙10-10 |
| Щавелевая | HOOC-COOH | (1)5,4 ∙10-2 (2)5,4∙10-5 |
| Яблочная | HOOCCH(OH)CH2COOH | (1)3,9 ∙10-4 (2)7,8 ∙10-6 |
| Янтарная | HOOC(CH2)2COOH | (1)6,19 ∙10-5 (2)2,30 ∙10-6 |
Константы диссоциации некоторых неорганических оснований
| Основание | Формула | Значение константы диссоциации КД |
| Гидроксид алюминия | Al(OH)3 | (3) 1,38 ∙10-9 |
| Гидроксид аммония | NH4OH | 6,3 ∙10-5 |
| Гидроксид бария | Ba(OH)2 | 2,3 ∙10-1 |
| Гидроксид ванадия | V(OH)3 | (3) 8,3 ∙10-12 |
| Гидроксид железа (II) | Fe(OH)2 | (2) 1,3 ∙10-4 |
| Гидроксид железа (III) | Fe(OH)3 | (3) 1,35 ∙10-12 |
| Гидроксид кадмия | Cd(OH)2 | 5,0 ∙10-3 |
| Гидроксид кальция | Ca(OH)2 | (2) 4,3 ∙10-2 |
| Гидроксид кобальта | Co(OH)2 | 4 ∙10-5 |
| Гидроксид магния | Mg(OH)2 | (2) 2,5 ∙10-3 |
| Гидроксид марганца | Mn(OH)2 | (2) 5 ∙10-4 |
| Гидроксид меди | Cu(OH)2 | (2)3,4 ∙10-7 |
| Гидроксид натрия | NaOH | 5,9 ∙1 |
| Гидроксид никеля | Ni(OH)2 | (2) 2,5 ∙10-5 |
| Гидроксид хрома | Cr(OH)3 | (3) 1,02 ∙10-10 |
| Гидроксид цинка | Zn(OH)2 | (2) 4 ∙10-5 |
Взаимосвязь концентраций ионов Н+, величины водородного показателя (рН) и окраски индикаторов
| Концентрация ионов Н+ | 10-1 | 10-2 | 10-3 | 10-4 | 10-5 | 10-6 | 10-7 | 10-8 | 10-9 | 10-10 | 10-11 | 10-12 | 10-13 | 10-14 |
| Величина водородного показателя | ||||||||||||||
| Индикаторы | Окраска индикаторов | |||||||||||||
| Лакмус | ярко- крас ный | ярко- крас ный | ярко- крас ный | крас ный | крас ный | слабо- крас ный | фиоле товый | слабо- синий | синий | синий | ярко- синий | ярко- синий | ярко- синий | ярко- синий |
| Фенолфталеин | мали новый | мали новый | мали новый | мали новый | мали новый | мали новый | ||||||||
| Метилоранж | ярко- крас ный | ярко- крас ный | ярко- крас ный | крас ный | крас ный | светло- оран жевый | оран жевый | светло- оран жевый | жёлтый | жёлтый | жёлтый | жёлтый | ярко- жёлтый | ярко- жёлтый |
Растворимость кислот, оснований и солей в воде
| Анионы | Катионы | ||||||||||||||||||||||
| H+ | Li+ | K+, Na+ | NH4+ | Sr2+ | Ba2+ | Ca2+ | Mg2+ | Al3+ | Cr3+ | Fe2+ | Fe3+ | Ni2+ | Co2+ | Mn2+ | Zn2+ | Ag+ | Hg2+ | Pb2+ | Be2+ | Cd2+ | Sn2+ | Cu2+ | |
| OH- | Р | Р | Р | Р | Р | Р | Н | Н | Н | Н | Н | Н | Н | Н | Н | – | – | H | H | H | H | H | |
| F- | Р | Н | Р | Р | Н | М | Н | М | М | М | М | Н | Р | Р | Р | М | Р | – | М | Р | Р | Р | Р |
| Cl- | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р | Р | Р |
| Br- | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р | Р | Р |
| I- | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | – | Р | Р | Р | Р | Н | Н | Н | Р | Р | М | – |
| S2- | Р | Р | Р | Р | Р | Р | Р | Р | – | – | Н | – | Н | Н | Н | Н | Н | Н | Н | – | Н | Н | Н |
| SO32- | Р | Р | Р | Р | Н | Н | Н | Н | – | – | Н | – | Н | Н | Н | Н | Н | – | Н | Н | Р | – | – |
| SO42- | Р | Р | Р | Р | Н | Н | М | Р | Р | Р | Р | Р | Р | Р | Р | Р | М | Р | Н | Р | Р | Р | Р |
| CrO42- | Р | Р | Р | Р | М | Н | М | Р | – | – | – | – | – | – | Н | Н | Н | Н | Н | (?) | (?) | – | Н |
| PO43- | Р | Н | Р | Р | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO32- | Р | Р | Р | Р | Н | Н | Н | Н | – | – | Н | – | – | – | Н | – | Н | – | – | – | – | – | – |
| SiO32- | Н | Р | Р | Н | Н | Н | Н | Н | Н | – | Н | Н | – | – | Н | Н | – | – | Н | (?) | (?) | – | Н |
| NO3- | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | – | Р |
| CH3COO- | Р | Р | Р | Р | Р | Р | Р | Р | М | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | + | Р | Р | Р |
ХИМИЯ
Курс лекций для студентов ЗиДО и МИППС специальностей 141108, 271101 и направлений 131000, 140100, 140400, 141200, 151000, 151900, 190600, 220400, 220700, 270800, 280700
Часть I.
Краснодар
Составители: д-р хим. наук, проф. Л.А. Бадовская;
д-р хим. наук, проф. В.В. Посконин;
канд. хим. наук, доц. Л.В. Поварова;
канд. хим. наук, доц. Л.А. Солоненко;
канд. хим. наук, доц. Л.Н. Сороцкая;
канд. хим. наук, доц. М.А. Тлехусеж;
канд. хим. наук, доц. З.И. Тюхтенева
УДК 669:54(07)
Химия: Курс лекций для студентов ЗиДОи МИППСспециальностей 141108, 271101 и направлений 131000, 140100, 140400, 141200, 151000, 151900, 190600, 220400, 220700, 270800, 280700. Часть I. / Сост. Л.А. Бадовская, В.В. Посконин, Л.В. Поварова, Л.А. Солоненко, Л.Н. Сороцкая, М.А. Тлехусеж, З.И. Тюхтенева: Кубан. гос. технол. ун-т. Кафедра общей химии. – Краснодар, 2013. – 42 с.
Составлено в соответствии с государственным стандартом высшего профессионального образования 3-го поколения.
© 

 КубГТУ, 2013
КубГТУ, 2013
Содержание
Тема 1. Химическая термодинамика………………………………………..4
Тема 2. Скорость химических реакций и методы ее регулирования…......8
Тема 3. Химическое равновесие…………………………………………..11
Тема 4. Гетерогенные химические системы и поверхностные явления
в них (спецраздел)……………………...………….……...……………….13
Тема 5. Растворы. Кислотно-основные свойства веществ.Реакции
обменного разложения в растворах электролитов и их использование
в химическом анализе ……...……………………………………………..16
Тема 6. Жесткость воды и реакции солей жесткости в водных раство-
рах………………………………………………………………………….. 25
Тема 7. Соединения кальция и вяжущие вещества на их основе (спец-
раздел)…………………………...………………………………………….27
Тема 8. Окислительно-восстановительные реакции и их использова-
ние в химическом анализе…….……………………… ………………..29
Тема 9. Электрохимические системы и процессы..………………………35
Приложение…………………….……………………………………………37
Тема 1. Химическая термодинамика
Рекомендуемая литература:[1], гл. 6, 6.1; [2], гл. 5; [5], гл. V.
Химическая термодинамика рассматривает законы термодинамики применительно к химическим и физико-химическим процессам. Химическая термодинамика изучает превращения энергии в химических и физико-химических процессах и способность химических систем совершать полезную работу. Зная термодинамические закономерности, можно подобрать оптимальные условия протекания реакции, установить возможность взаимодействия между конкретными веществами и направление самопроизвольно протекающих процессов, рассчитать тепловой эффект химической реакции.
Величины, которые характеризуют физическое состояние системы и могут быть непосредственно измерены, называются термодинамическими параметрами состояния. Для удобства и расчетов приняты следующие основные стандартные параметры состояния: температура 298 К, давление 1,01325.105 Па, концентрации растворов 1 моль/кг растворителя. В зависимости от условий протекания процесса выделяют: изохорный процесс – протекающий при постоянном объеме системы (V=const); изо-барный процесс – протекает при постоянном давлении системы (Р=const); изотермический процесс – протекает при постоянной температуре системы (Т=const) и др. Химические и физико-химические процессы могут быть термодинамически обратимыми или термодинамически необратимыми.
Кроме параметров состояния в термодинамике используются вели-чины, которые называют термодинамическими функциями – переменные величины, которые не могут быть непосредственно измерены и зависят только от параметров состояния. Выделяют два вида термодинамических функций: функции состояния и функции процесса.
Любая физическая величина, значение которой в данный момент времени определяется термодинамическими свойствами и параметрами состояния системы, называется функцией состояния. Важнейшими функциями состояния являются внутренняя энергия U, энтальпия H, энтропия S и энергия Гиббса G(таблица 1.1).Функции состояния – аддитивные функции, так как их значения можно складывать и вычитать, как обычные числа, их изменения определяются лишь конечным и начальным состояниями системы, т.е. не зависят от пути процесса.
