Краткие теоретические сведения. Свойства жидких топлив Топливо Элементный (средний) состав 1 кг топлива
Свойства жидких топлив
| Топливо | Элементный (средний) состав 1 кг топлива | Молекулярная масса μТ, кг/кмоль | QH, кДж/кмоль | ||
| С | О | N | |||
| Автомобильный бензин | 0,855 | 0,145 | - | 110 – 120 | |
| Дизельное | 0,870 | 0,126 | 0,004 | 180 – 200 | |
| Дизельное моторное | 0,870 | 0,125 | 0,005 | 220 – 280 |
Сгорание топлива представляет собой химическое соединение составных элементов топлива с кислородом:
С + О2 = СО2, 2Н2 + О2 =2Н2О, (3.1)
при неполном сгорании углерода:
2С + О2 = 2СО. (3.2)
Для полного сгорания 1 кг топлива (состав С+Н+О = 1) требуется количество кислорода:
в киломолях
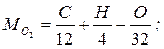 (3.3)
(3.3)
в килограммах
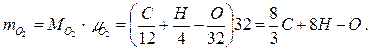 (3.4)
(3.4)
В окружающем воздухе кислорода по массе содержится примерно 23 %, а по объему 21 %. Поэтому количество воздуха, которое теоретически необходимо для сгорания топлива массой 1 кг и состава С + Н + О = 1, выражают стехиометрическим соотношением, кмоль,

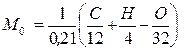 (3.5)
(3.5)
или, кг

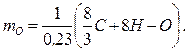 (3.6)
(3.6)
Кажущаяся молекулярная масса воздуха μВ = 29 кг/кмоль, следовательно,
m0= μВМ0 = 29М0.(3.7)
Отношение количества воздуха m, действительно поступающего в цилиндр двигателя, к теоретически необходимому количеству m0 называется коэффициентом избытка воздуха α:
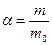 , или
, или 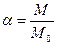 . (3.8)
. (3.8)
Если α < 1 (недостаток кислорода), смесь называют богатой, при α > 1 (избыток кислорода) смесь называют бедной.
При полном сгорании 1 кг топлива в двигателях с искровым зажиганием общее количество горючей смеси, кмоль, состоящей из паров топлива и воздуха,
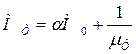 , (3.9)
, (3.9)
где μТ- молекулярная масса топлива (см. табл.1).
В дизелях из-за малого объема, занимаемого жидким топливом, величиной 1/μТможно пренебречь, поэтому
МТ = α М0. (3.10)
При полном сгорании жидкого топлива (α > 1) продукты сгорания состоят из образовавшихся в результате реакции СО2, Н2О, избыточного кислорода и азота. Количество отдельных составляющих продуктов сгорания, кмоль, определяется по следующим формулам:
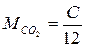 ; (3.11)
; (3.11)
 ; (3.12)
; (3.12)
 , (3.13)
, (3.13)
где 0,21α М0 - количество поступившего кислорода, кмоль; 0,21 М0 – количество кислорода, принявшего участие в реакции, кмоль.
MN2 = 0,79 α М0.
Общее количество продуктов сгорания МПС, кмоль, отнесенное к 1 кг топлива:
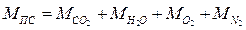 .
.
Подставляя в это выражение значения, 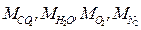 , получим:
, получим:
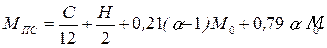
Для стехиометрического состава смеси (α = 1):
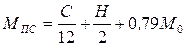 . (3.14)
. (3.14)
Для значения α > 1 количество, кмоль, продуктов сгорания с учетом избыточного азота ΔΜN2 = 0,79(α – 1)M0 и избыточного кислорода ΔΜО2 = 0,21(α – 1)M0 в продуктах сгорания определится:
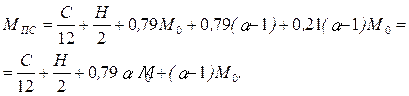 (3.15)
(3.15)
Масса продуктов сгорания GПС, кг, при сгорании 1 кг жидкого топлива
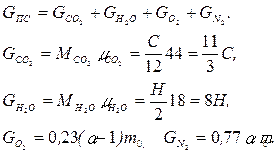
Тогда
 (3.16)
(3.16)
При неполном сгорании жидкого топлива (α < 1) из-за недостатка
кислорода часть углерода топлива сгорает в окись углерода, а часть водорода не реагирует с кислородом.
Эксперименты показывают, что отношение числа молей водорода к окиси углерода примерно постоянно для данного топлива и не зависит от величины α. Обозначим это отношение через К.
 (3.17)
(3.17)
Согласно опытным данным для бензинов, у которых Н/С = 0,17 – 0,19, К= 0,45 – 0,50, а при Н/С = 0,13, К= 0,30.
Вследствие неполноты сгорания топлива выделившееся количество теплоты уменьшается на доли не выделившейся теплоты находящихся в продуктах сгорания окиси углерода водорода (ΔQН)CO и (ΔQН)Н2. Суммарную долю не выделившейся теплоты (ΔQН)хим = (ΔQН)CO + (ΔQН)Н2 можно подсчитать по уравнению, Дж/кг
(ΔQН)хим = А(1 – α)М0, (3.18)
где А =114· 106 при К = 0,5 – 0,45 и А = 116·106 при К = 0,3.
Опуская промежуточные выкладки, запишем выражение для компонентов, входящих в состав продуктов сгорания в случае α < 1. Количество каждого компонента, кмоль, определяется по следующим формулам:
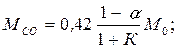 (3.19)
(3.19)
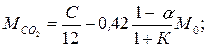 (3.20)
(3.20)
 (3.21)
(3.21)
 (3.22)
(3.22)
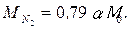 (3.23)
(3.23)
В то время как массы, кг, продуктов сгорания и горючей смеси до сгорания одинаковы (GПС = GT), количество молей продуктов сгорания и количество молей горючей смеси до сгорания неравны. Изменение количества молей смеси (ΔМ) при сгорании происходит вследствие изменения числа молекул газообразных продуктов сгорания по сравнению с числом молекул горючей смеси до сгорания, т.е. ΔМ = МПС – МТ.
Изменение количества молей принято выражать относительной величиной - теоретическим коэффициентом молекулярного изменения
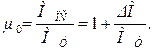 (3.24)
(3.24)
Для бензиновых двигателей с искровым зажиганием
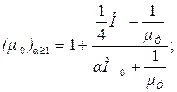 (3.25)
(3.25)
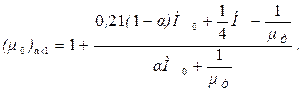 (3.26)
(3.26)
Для дизелей (α > 1)
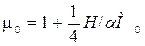 . (3.27)
. (3.27)
Примеры и задачи
Пример 1. Определить количество воздуха, участвующего в сгорании 1 кг бензина А-92 (С = 0,855; Н = 0,145) при коэффициенте избытка воздуха a = 0,9 в кмолях и килограммах.
Решение:
Количество воздуха, участвующего в сгорании 1 кг бензина
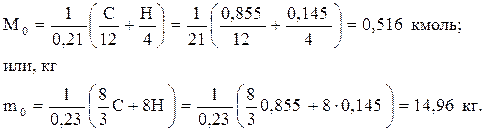
Пример 2. Определить суммарное количество продуктов сгорания 1 кг бензина А-92 (С = 0,855; Н = 0,145) при коэффициенте избытка воздуха a = 0,9 в кмолях, а также теоретический коэффициент молекулярного изменения. Отношение количества молей не прореагировавшего водорода к числу молей окиси углерода К= 0,5:
Решение:
Суммарное количество продуктов сгорания, которое получается при сгорании горючей смеси:
МПС = МСО + МСО2 + МН2 + МН2О + МN2
Количество отдельных составляющих продуктов сгорания:
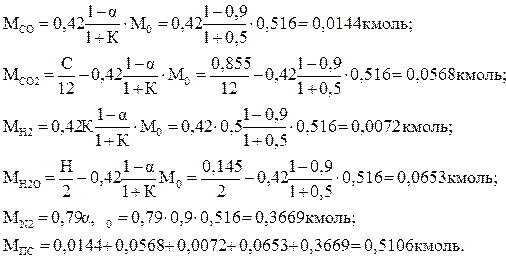
Изменение количества молей смеси
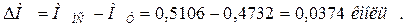
Теоретический коэффициент молекулярного изменения μ0:
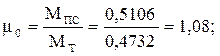
Задачи для самостоятельного решения:
1. Рассчитать теоретически необходимое количество воздуха для сгорания 1 кг дизельного топлива (С = 0,870; Н = 0,126; О = 0,004) в кмолях и килограммах.Определить действительное количество воздуха, участвующего в горении, если коэффициент избытка воздуха a = 1,4
Ответ: Необходимое количество воздуха М0 = 0,495 кмоль/кг; m0 = 14,452 кг/кг. Действительное количество воздуха, участвующего в горении 0,693 кмоль/кг и 20,233 кг/кг.
2. Определить количество молей газа, участвующего в горении дизельного топлива с составом, приведенным в задаче 1, общее количество молей продуктов сгорания и теоретический коэффициент молекулярного изменения. Объем, занимаемый каплями дизельного топлива пренебречь.
Ответ: Количество молей газа, участвующего в горении дизельного топлива 0,693 кмоль/кг; общее количество молей продуктов сгорания 0,960 кмоль/кг; теоретический коэффициент молекулярного изменения 1,385.
3.3. Контрольные вопросы:
1. От чего зависит скорость распространения пламени в процессе сгорания?
2. В чем отличие нормального и турбулентного пламени?
3. Что такое детонационное горение?
4. Что характеризует октановое число? Как оно определяется?
5. Что такое «самовоспламенение» топлива? Что такое цетановое число и как оно определяется?
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
Основная литература
1.Луканин В.Н. Двигатели внутреннего сгорания : учебник для вузов [Гриф Минобрнауки РФ] : в 3-х кн.Кн.1 : Теория рабочих процессов / В.Н.Луканин, К.А.Морозов, А.С.Хачиян [и др.] ; под ред. В.Н. Луканина, М.Г. Шатрова.- 4-е изд., перераб. и доп. - М. : Высшая школа, 2012. - 479 с.
2. Луканин В.Н. Теплотехника : учебник для вузов [Гриф Минобрнауки РФ] / В.Н. Луканин, М.Г., М.Г.Шатров [и др.] ; под ред. В.Н.Луканина. - 5-е изд., перераб. и доп. - М. : Академия, 2009. - 671 с.
3. Шатров М.Г. Автомобильные двигатели : учебник для вузов [Гриф Минобрнауки РФ] / М.Г.Шатров, К.А.Морозов [и др.] ; под. ред. М.Г.Шатрова. – М.: Издательский центр «Академия», 2010. – 464 с.
4. Скачкова С.С. Термодинамика и рабочие процессы двигателей внутреннего сгорания : учебное пособие для вузов [Гриф УМО] : в 2 ч. Ч. 1: Основы термодинамики и теплообмена / С.С. Скачкова, Т.Г. Михайлова. - Екатеринбург: Изд-во ФГАУ ВПО «Рос. Гос. проф.-пед. ун-т», 2010. - 158 с.
Дополнительная литература
1.Железко Б.Е. Термодинамика, теплопередача и двигатели внутреннего сгорания : учебник для вузов [Гриф Минобрнауки РФ] / Б.Е. Железко, В.М. Адамов [и др.] . - Мн. : Высшая школа., 1985. - 271 с.
2. Колчин А.И.Расчет автомобильных и тракторных двигателей: учебник для вузов учебник для вузов [Гриф Минобрнауки РФ] / А.И. Колчин,
В.П. Демидов. – М. : Высшая школа, 2002. - 496 с.
3. Кудинов В.А. Техническая термодинамика : учебное пособие для вузов [Гриф УМО] / Кудинов В.А., Карташов Э.М. – М : Высшая школа, 2007. - 261 с.
Задания и методические указания
к выполнению практических работ по дисциплине
«Транспортная энергетика»
Подписано в печать Формат 60х84/16. Бумага для множ. аппаратов.
Печать плоская. Усл.печ.л. Уч.-изд.л. Тираж экз. Заказ
ФГАОУ ВПО «Российский государственный профессионально-педагогический университет». Екатеринбург, ул. Машиностроителей, 11.
Ризограф ФГАОУ ВПО РГППУ. Екатеринбург, ул. Машиностроителей, 11.
