Энергетические уровни в атоме
В правой части формулы (12) все величины кроме n постоянны, следовательно, радиусы возможных орбит относятся между собой как квадрат чисел натурального ряда rn1 : rn2 = n12 : n22 Из формулы (13) видно, что энергия атома возрастает с увеличением главного квантового числа n или, что одно и то же, с увеличением радиуса орбиты электрона. При этом надо учитывать, что энергия E отрицательна, поэтому уменьшение ее абсолютной величины соответствует возрастанию энергии.
Минимумом энергии атом обладает при движении электрона по ближайшей к орбите, n =1, а максимумом энергии при n=¥ т.е. при ионизации атома. Так как энергия такой системы, как атом водорода, не зависит от эксцентриситета эллипса, то этой же формулой можно пользоваться и при эллиптических орбитах с большой полуосью а = r
Из формулы (13) следует, что энергетические состояния атома водорода образуют последовательность энергетических уровней, изменяющихся в зависимости от главного квантового числа n. Величина полной энергии электрона, находящегося на возможной орбите, называется у р о в н е м энергии атома или энергетическим уровнем. На рис.3 схематично изображены уровни энергии водородного атома. Слева указаны порядковые номера уровней, справа соответствующие им энергии в электронвольтах. Уровень энергии, соответствующий n = 1, т.е. минимуму энергии, называется о с н о в н ы м уровнем, не возбужденным; все остальные уровни являются возбужденными.
В силу закона сохранения и превращения энергии самопроизвольный переход электрона на более далекую от ядра орбиту, т.е. переход атома на более высокий энергетический уровень невозможен. Для осуществления такого перехода необходимо сообщить атому определенное количество энергии, квант. Таким образом, атом может излучать и поглощать волны только вполне определенных длин (частот), чем и обусловлен линейчатый характер спектра.
Вывод расчетной формулы
Из формулы (14), зная длину волны l, можно найти постоянную Планка h, если известны термы спектральных линий. Так как термы спектральных линий водорода известны, то, найдя длину волны линий водорода, можно вычислить постоянную Планка.
Из формулу (14):
h3 = 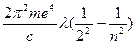 | (16) |
/16/
Формула получена в системе СГСЭ. Чтобы перейти к единицам системы СИ вместо е2 нужно поставить 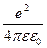 , где e0 –электрическая постоянная;
, где e0 –электрическая постоянная;
e0 = 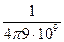 Ф/м;
Ф/м;
e – относительная диэлектрическая проницаемость, для вакуума и воздуха e = 1. В системе СИ расчетная формула примет вид:
h3 = 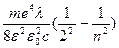 | (16/) |
Эта формула и будет расчетной в работе.
