Теоретические сведения. Существует однозначная связь между спектром испускания и химической
Существует однозначная связь между спектром испускания и химической индивидуальностью атомов. На этом основан спектральный анализ, т.е. определение качественного и количественного состава излучающей смеси паров по ее спектру.
Основной частью спектрального прибора (рис. 16), используемого в данной работе, является призма, осуществляющая дисперсию пучка света по длинам волн.
Дисперсия света заключается в том. Что если в вакууме световые волны различных частот и, следовательно, различных длин распространяются с одинаковой скоростью, то в веществе скорость света различна для волн различной длины. Это приводит к тому, что показатель преломления вещества, который, как известно, измеряется отношением скорости света в вакууме к скорости света в данном веществе, оказывается зависящим от частоты. Лучи света с различной частотой (длиной волны) преломляется по-разному и, таким образом, могут быть разделены. Чем большей дисперсией обладает данное вещество, тем больше оно может разделить близко расположенные спектральные линии.
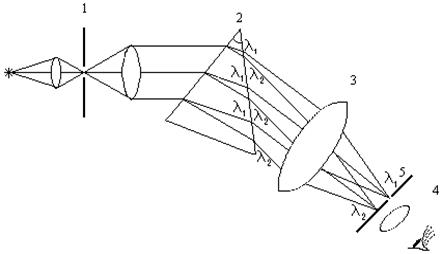 |
Рис.16
Так как угол отклонения луча призмой (2 ) зависит не только от длины волны, но и от угла падения на призму, важно, чтобы все падающие на призму лучи были параллельны. Это достигается с помощью коллиматора. Коллиматор имеет узкую щель (1 ), которая помещается в области коллиматорной линзы. Рассматривается спектр через зрительную трубу, соcтоящую из объектива (3 ) и окуляра ( 4 ). Объектив в своей фокальной плоскости дает много изображений щели, образованных каждым из монохроматических пучков окрашенных в соответствующий цвет.
Эти изображения рассматриваются через окуляр. В монохроматоре, служащем для выделения монохроматического света, в фокальной плоскости окуляра помещена вторая щель (5 ), выделяющая строго монохроматическую волну.
Исследуя спектр поглощения водного раствора двухромовокислого калия, можно определить постоянную Планка. Двухромовокислый калий в воде диссоциирует на ионы K+ и Cr2O7- - .
K2 Cr2O7 Û 2K+ + Cr2O7- - .
Ионы калия в видимой части спектра на поглощают, а ионы Cr2O7- - поглощают все лучи сине-фиолетовой части спектра.
Установлено, что кванты света с длиной волны, соответствующей началу поглощения, производят отщепление молекул CrO3 от иона Cr2O7 по уравнению:
Cr2O7 + hn = Cr2O4 + Cr2O3 .
С другой стороны, известно, что для отщепления CrO3 от иона Cr2O7 необходимо затратить энергию 3,672 × 10-19 Дж. Эта энергия и равна энергии поглощения кванта hn, где n - частота, соответствующая началу поглощения.
 Измерение и обработка результатов
Измерение и обработка результатов
I. Градуировка монохроматора.
1. Включите ртутную лампу. Отрегулируйте ширину входной щели так, чтобы спектр был четким и контрастным.
2. Отградуируйте монохроматор, т. е. определите, какому делению шкалы барабана соответствует определенная длина волны света. Данные занесите в таблицу 1.
Таблица 1.
| № измерения | l, нм | Номер деления барабана (угловое расстояние между спектральными линиями) |
| Красная 690,7 | ||
| Красная 671,6 | ||
| Оранжевая 623,4 | ||
| Оранжевая 612,3 | ||
| Оранжевая 607,3 | ||
| Желтая 579,1 | ||
| Желтая 577 | ||
| Зеленая 546,1 | ||
| Голубая 491,6 | ||
| Фиолетовая 435,8 | ||
| Фиолетовая 434,8 | ||
| Фиолетовая 433,9 | ||
| Фиолетовая 407,8 | ||
| Фиолетовая 404,7 |
Наиболее характерными для спектра ртути являются две весьма близко расположенные желтые линии (l = 579,1 нм и l =577,0 нм). Справа от нее расположена зеленая очень яркая линия (l = 546,1 нм), далее средней яркости голубая линия (l = 491,6 нм), далее три фиолетовых линии: самая яркая (l = 435,8 нм) и две отдельные фиолетовые умеренной яркости (l = 434,8 нм и 433,9 нм). Далее четко видны две отдельные фиолетовые линии умеренной яркости (l = 407,8 нм и l = 404,7 нм). Слева от желтого дублета видна оранжевые линии и красные линии. При наиболее внимательном рассмотрении могут быть замечены еще несколько бледных линий, которые для градуировки существенного значения не имеют.
3. Постройте градуировочный график N = f (l), откладывая по оси абсцисс l (нм), а по оси ординат - деления шкалы барабана.
II. Качественный спектральный анализ (определение газа в источнике света).
1. Поставьте перед входной щелью монохроматора исследуемый источник света и включите его.
2. Снимите спектр исследуемого вещества, записывая деления шкалы барабана монохроматора наиболее ярки(l=х спектральный линий. По градуировочному графику определите длины волн спектральных линий. Данные занесите в таблицу 2.
Таблица 2.
| № п/п | Номер деления шкалы барабана монохроматора | l, нм |
| 1. | Краcная | |
| 2. | Голубая | |
| 3. | Сине-фиолетовая | |
| 4. | Фиолетовая |
III. Определение постоянной Планка.
1. Зажгите лампу накаливания и пронаблюдайте сплошной спектр.
2. Поместите перед входной щелью монохроматора на пути светового пучка кювету с водным раствором двухромовокислого калия. Сплошной спектр лампы оказывается обрезанным с фиолетового конца. Определите наибольшую длину волны, поглощенную раствором.
Зная длину волны поглощения, вычислите частоту по формуле:
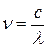
где c - скорость света.
Подсчитайте постоянную Планка по формуле

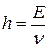 ,
,
где Е =3,672 × 10-19 Дж.
Контрольные вопросы
1. Какое физическое явление лежит в основе спектрального анализа?
2. Что называется дисперсией света?
3. Чем отличается эмиссионный спектр вещества от абсорбционного?
4. Какой свет называется монохроматическим?
Литература
1. Кортнев А.В. и др. Практикум по физике. М.: Высшая школа, 1965, раб. 83.
2. Майсова Н.М. Практикум по курсу общей физики. М.: Высш.школа,1970, раб.77, 78.
3. Савельев И.В. Курс общей физики: В 3-х т. М.: Наука, 1982, т.3.
