Изотермический процесс
Изотермический процесс протекает в условиях постоянной температуры, т.е. при 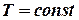 или
или 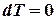 .
.
Таблица 5.3 – Исследование изотермического процесса
| Метод исследования | Формулы |
1. Уравнение кривой процесса в 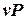 - диаграмме - диаграмме | 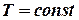 ; ; 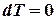 . . |
2. График процесса в 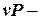 и и 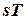 - координатах - координатах | |
В 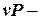 диаграмме изотермический процесс представляет собой равнобокую (равностороннюю) гиперболу. Чем выше температура диаграмме изотермический процесс представляет собой равнобокую (равностороннюю) гиперболу. Чем выше температура 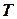 , тем выше в , тем выше в 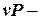 диаграмме располагается изотерма. диаграмме располагается изотерма. |  |
Pис. 5.7. - Изотермический процесс в 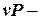 координатах координатах | |
В 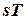 -диаграмме изотермический процесс изображается прямой линией, параллельной оси абсцисс. -диаграмме изотермический процесс изображается прямой линией, параллельной оси абсцисс. | 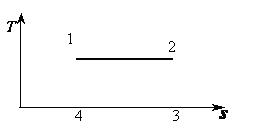 |
Pис. 5.8. - Изотермический процесс в 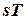 - координатах - координатах |
Продолжение таблицы 5.4.
| Метод исследования | Формулы |
| 3. Изотермический процесс описывается уравнением состояния в виде: | 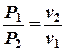 |
4. Изменение внутренней энергии равно нулю, т.е. 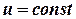 | 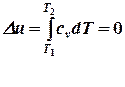 |
| 5. Удельная работа в изотермическом процессе: |   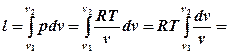 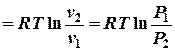 |
| 6. Удельная располагаемая работа Следовательно, в изотермическом процессе для идеального газа располагаемая работа l0 равна работе процесса l. | 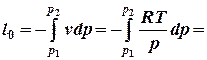 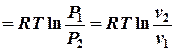 |
| 7. Уравнение первого закона термодинамики для изотермического процесса имеет вид: | 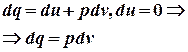 или или 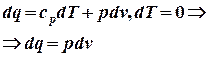 |
| 8. При T = const dT = 0: | 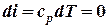 ,т.е. ,т.е.  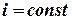 |
| 8. Изменение удельной энтропии: | 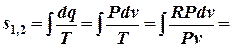 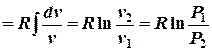 |
| 9. Доля теплоты, расходуемая на изменение внутренней энергии в изотермическом процессе: | 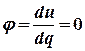 |
| 10. Доля теплоты, расходуемая на совершение работы | 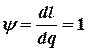 |
На рис. 5.9. показано распределение теплоты в изотермическом процессе
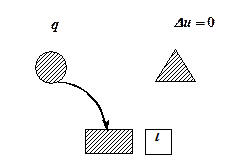 a a | 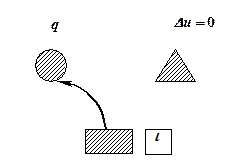 б б |
Рис. 5.9. Схема распределения теплоты в изотермическом процессе:
а- при расширении газа; б – при сжатии газа
Адиабатный процесс
Адиабатный процесс- это процесс без теплообмена с внешней средой. При адиабатном процессе энергообмен рабочего тела с окружающей средой происходит только в форме работы, энергообмена в форме теплоты нет. Эти условия выражаются соотношением: 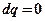 . Тогда уравнение первого закона термодинамики для адиабатного процесса имеет вид:
. Тогда уравнение первого закона термодинамики для адиабатного процесса имеет вид:
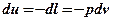 . (5.4)
. (5.4)
Из этого уравнения видно, что работа адиабатного процесса расширения совершается вследствие уменьшения внутренней энергии газа и, следовательно, температура газа уменьшается. Работа адиабатного сжатия полностью идет на увеличение внутренней энергии газа, то есть на повышение его температуры. Таким образом, изменение внутренней энергии и работа в адиабатном процессе эквивалентны по величине и противоположны по знаку.
Выведем уравнение адиабаты для идеального газа. Воспользуемся уравнением первого закона термодинамики:
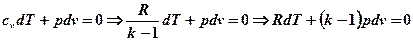
т.к. 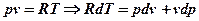 , то
, то
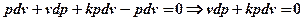 (5.5)
(5.5)
Разделив переменные, получим:
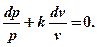 (5.6)
(5.6)
Интегрируя (5.6) при k = const, получим 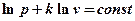 , откуда
, откуда
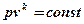 (5.7)
(5.7)
Уравнение (5.7) является уравнением адиабаты.
На рис. 5.10 приведен адиабатный процесс расширения газа в 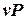 -диаграмме.
-диаграмме.
Из уравнения (5.7) следует:
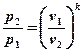 , (5.8)
, (5.8)
то есть при адиабатном расширении давление падает, а при сжатии возрастает.
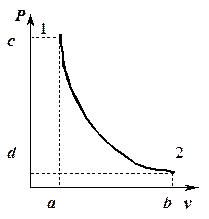
Рис. 5.10. Адиабата идеального газа
Учитывая, что в адиабатном процессе изменяются все три параметра состояния, необходимо выявить зависимости между v и T, p и T.
Зависимость между температурой T и объемом v можно получить из уравнения (5.8) и уравнений состояния, записанных для точек процесса 1 и 2: Р1v1 = RT1 и Р2v2=RT2, откуда
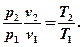 (5.9)
(5.9)
Из уравнений (5.8) и (5.9) следует: 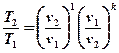
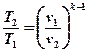 (5.10)
(5.10)
Далее из уравнений (5.8) и (5.10) следует: 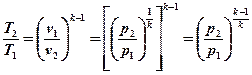
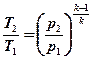 (5.11)
(5.11)
При k = const для вычисления работы адиабатного процесса можно записать несколько формул. Из уравнения 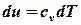 при cv = const имеем:
при cv = const имеем:
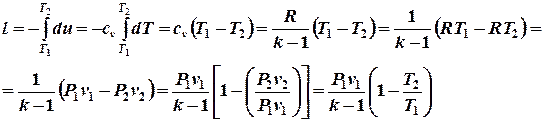 (5.12)
(5.12)
Учитывая соотношения (5.10) и (5.11), уравнение (5.12) запишем в виде:
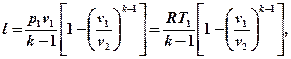
(5.13)
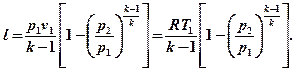
Располагаемая работа в адиабатном процессе определим из соотношения
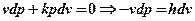 , то есть
, то есть
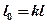 (5.14)
(5.14)
Для обратимого адиабатного процесса 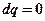 , поэтому
, поэтому
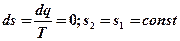 , то есть обратимый адиабатный процесс будет изоэнтропным и в
, то есть обратимый адиабатный процесс будет изоэнтропным и в 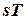 -диаграмме изображается прямой линией, параллельной оси
-диаграмме изображается прямой линией, параллельной оси 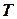 (рис. 5.11). Процесс адиабатного расширения изображается вертикальной прямой 2-1, идущей вниз, а процесс адиабатного сжатия 1-2 – вертикальной прямой, идущей вверх.
(рис. 5.11). Процесс адиабатного расширения изображается вертикальной прямой 2-1, идущей вниз, а процесс адиабатного сжатия 1-2 – вертикальной прямой, идущей вверх.
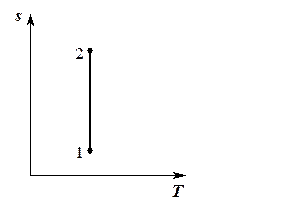
Рис. 5.11. Адиабатный процесс в 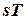 -диаграмме
-диаграмме
Теплоемкость в адиабатном процессе равна нулю: 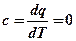 .
.
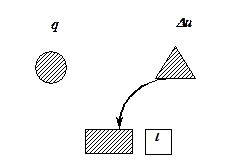 a a | 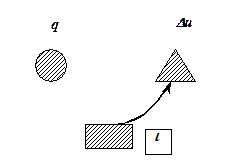 a a |
Рис. 5.12. Схема распределения энергии в адиабатном процессе:
а- при расширении газа; б – при сжатии газа
Политропный процесс
Политропный процесс – любой произвольный процесс изменения состояния рабочего тела, протекающий при постоянной теплоемкости сx, то есть c = cx = const. Линия процесса называется политропой.
Из определения политропного процесса следует, что основные термодинамические процессы (изохорный, изобарный, изотермический, адиабатный, если они протекают при постоянной удельной теплоемкости, являются частными случаями политропного процесса.
Другими словами, политропный процесс характеризуется одной и той же долей количества подводимой теплоты, расходуемой на изменение внутренней энергии системы.
Уравнение политропного процесса можно получить из уравнений первого закона термодинамики для идеального газа:
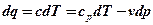
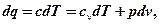
далее имеем:
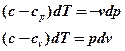
Разделим первое уравнение на второе
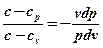
и обозначим
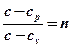 ,
,
тогда
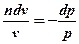
Интегрируя полученное соотношение в пределах от начала до конца процесса, находим:
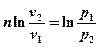 ,
,
или после потенцирования
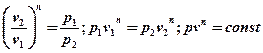
получаем уравнение политропного процесса 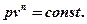
Поскольку уравнение политропы отличается от уравнения адиабаты только значением показателя n, то все соотношения между основными параметрами могут быть представлены формулами, аналогичными формулам для адиабатного процесса:
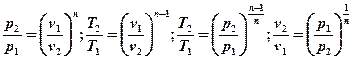
Удельная теплоемкость политропного процесса может быть определена из выражения для показателя политропы
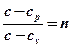 , откуда
, откуда 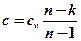 ,
,
где k – показатель адиабаты.
Последнее уравнение позволяет определить удельную теплоемкость политропного процесса для любого значения n. Если в это уравнение подставить значения для частных случаев, то можно получить:
| Изохорный процесс: | n = ±¥; | c = cv; | v = const. | |
| Изобарный процесс: | n = 0; | c = kcv = cp; | p = const. | |
| Изотермический процесс: | n = 1; | c = ±¥; | T = const. | |
| Адиабатный процесс: | n = k; | c = 0; | pvk = const. | |
Характер зависимости 
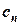 от показателя политропы n графически показан на рис. 5.13.
от показателя политропы n графически показан на рис. 5.13.
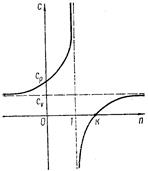
Рис.5.13. Зависимость теплоемкости от показателя политропы.
Уравнение удельной работы изменения объема, совершаемой телом при политропном процессе, имеет аналогичный вид с уравнением удельной работы в адиабатном процессе
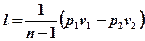
или
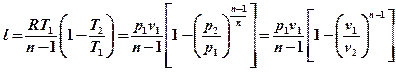 .
.
Располагаемая работа равна: 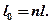
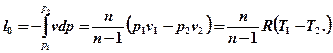
Изменение удельной внутренней энергии газа и теплота в политропном процессе определяются из уравнений:
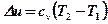
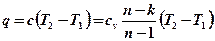 .
.
Изменение удельной энтальпии определяется по формуле, справедливой для всех процессов идеального газа, включая политропный процесс:
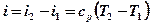 .
.
Изменение удельной энтропии газа в политропном процессе равно:
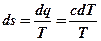
или для конечного изменения состояния
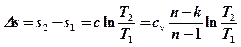 .
.
Значение показателя политропы в любом политропном процессе может быть определено по координатам любых двух точек графика:
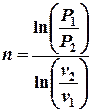 ;
; 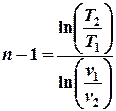 ;
; 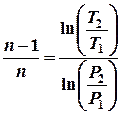 .
.
Если в vP- и sT – координатах выбрать некоторую произвольную точку и провести из нее все рассмотренные термодинамические процессы, то все поле построенной таким образом диаграммы делится на восемь областей, характеризующихся определенными признаками (рис. 5.14).
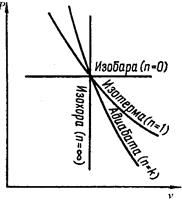
Рис. 5.14. Взаимное расположение политроп в зависимости от величины показателя n
6. второй закон термодинамики
6.1 Термодинамические циклы тепловых машин. Прямые и обратные циклы, обратимые и необратимые
В термодинамическом процессе работу можно получить в двух случаях: вследствие подведенной теплоты или вследствие изменения внутренней энергии рабочего тела. При любом процессе расширения газа в цилиндре наступает момент, когда температура и давление рабочего тела станут равными температуре и давлению окружающей среды, и на этом прекратится получение работы. Следовательно, для повторного получения работы необходимо возвратить рабочее тело в первоначальное состояние в процессе сжатия. Если рабочее тело расширяется, по кривой 1-3-2 (рис.6.1), то оно производит работу, изображенную на vP-диаграмме площадью 1-3-2-4-5-1.
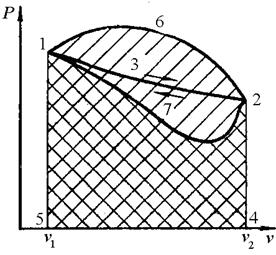
Рис. 6.1. К выбору кругового процесса
При достижении точки 2 тело должно быть возвращено в начальное состояние - точку 1 - для того, чтобы снова начало совершать работу. Процесс возвращения тела в начальное состояние может быть осуществлен тремя путями:
1. Кривая сжатия 2-3 совпадает с кривой расширения 1-3-2. В этом случае вся полученная работа при расширении (пл. 1-3-2-4-5) равна работе сжатия (пл. 2-3-1-5-4) и положительная работа равна 0.
2. Кривая сжатия 2-6-1 располагается под линией расширения. При этом на сжатие затрачивается большее количество работы, чем ее будет получено при расширении (пл.2-6-1-5-4 больше пл. 1-3-2-4-5).
3. Кривая сжатия 2-7-1 располагается над линией расширения 1-3-2. В этом процессе работа расширения будет больше работы сжатия, т.к. пл. 1-3-2-4-5 больше пл. 2-7-1-5-4. В результате будет совершена положительная работа, равная пл. 1-3-2-7-1, внутри замкнутой линии кругового процесса или цикла.
Повторяя цикл неограниченное число раз, можно за счет подводимой теплоты получить любое количество работы.
Цикл, в результате которого получается положительная работа, называется прямым циклом, или циклом теплового двигателя; в нем работа расширения больше работы сжатия.
Цикл, в результате которого расходуется работа, называется обратным циклом; в нем работа сжатия больше работы расширения. По обратным циклам работают холодильные установки.
Цикл, состоящий из равновесных обратимых процессов, будет обратимым. Рабочее тело в таком цикле не должно подвергаться химическим изменениям.
Если хоть один из процессов, входящих в состав цикла, является необратимым, то и весь цикл будет необратимым.
Результаты исследований идеальных циклов могут быть перенесены на действительные, необратимые процессы тепловых машин путем введения опытных поправочных коэффициентов.
