Рацемические смеси и принципы их разделения на энантиомеры
Равные количества энантиомеров образуют рацемическую смесь или иначе рацемат. Взаимная компенсация оптических свойств зеркальных антиподов приводит к отсутствию оптической активности для рацемата. Обычно рацемическая смесь образует отдельную форму кристаллов и по этой причине имеет индивидуальную температуру плавления и растворимость. Например, рацемическая винная кислота (иначе ее называют виноградной кислотой) оптически не деятельна, имеет т. пл. 206 °С и растворимость 20,6 г в 100 г воды по сравнению с 139 г / 100 г воды для D- и L-винных кислот и 125 г / 100 г воды для мезо-винной кислоты.
Большинство соединений с асимметрическим атомом углерода синтезируются в виде рацемической смеси. Кроме того, в определенных условиях индивидуальные энантиомеры могут превращаться в свои антиподы – рацемизироваться. По этим причинам перед исследователями часто стоит проблема разделения рацематов на индивидуальные энантиомеры.
Первым эту задачу решил Л. Пастер[7], который установил, что натрийаммониевая соль винной кислоты образует две формы кристаллов, являющихся зеркальными отображениями друг друга. Данное обстоятельство позволило ему механически с помощью лупы и пинцета выделить чистые энантиомеры. Так как образование разных кристаллических форм энантиомеров встречается очень редко, то данный подход к разделению рацемических смесей скорее является исключением, чем общим способом.
v Разделение рацематов в виде диастереомерных солей. В отличие от энантиомеров диастереомеры отличаются по физико-химическим свойствам и смесь диастереомеров обычно можно разделить, подобрав условия кристаллизации одного из компонентов. Поэтому первым общим методом разделения рацематов является их разделение на антиподы путем превращения в диастереомеры.
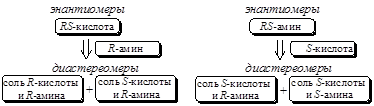
Наиболее просто такой вариант разделения осуществить для аминов и карбоновых кислот, которые легко образуют аммонийные соли. Кроме того, из природных источников было выделено достаточное количество оптически чистых карбоновых кислот (D-(+)-винная, D-(-)-яблочная, D-(-)-миндальная и др.) и аминов (алкалоиды: хинин, стрихнин, бруцин; и полученные синтетически (R)-(+)-ментиламин, (R)- и (S)-1-фенилэтиламины), что позволяет разделять как рацемические амины, так и рацемические кислоты.
Разберем этот способ разделения рацематов на реальном примере. (RS)-2-Фенилизомасляную кислоту нейтрализовали (R)-1-фенилэтиламином. Полученную смесь диастереомерных (R)(S)- и (R)(R)-солей перекристаллизовали из водного этанола и получили кристаллическую (R)(R)-аммонийную соль, которую подкислили и извлекли чистую (R)-2-фенилизомасляную кислоту с выходом 67%.
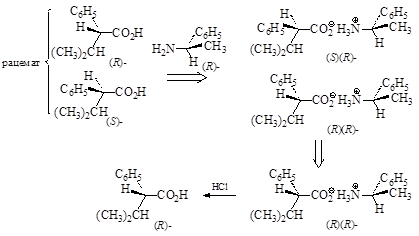
Рис. 6.2. Схема выделения (R)-2-фенилизомасляной кислоты из рацемической смеси
Как в рассмотренном случае, так и во многих других, выделение второго энантиомера из лучше растворимой соли бывает затруднено. Обычно это затруднение решают подбором другого энантиомера. Например, при разделении (RS)-1-фенилэтиламина вначале обработкой (S)-яблочной кислотой выделили менее растворимую (R)(S)-соль и затем сам (R)-1-фенилэтиламин. Из маточного раствора выделяют смесь аминов, обогащенную (S)-энантиомером которую нейтрализуют (RR)-винной кислотой, откристаллизовывают соответствующую соль (S)-амина и после разложения аммонийной соли получают оптически чистый (S)-1-фенилэтиламин.
Данный метод можно расширить и на некоторые другие классы органических соединений. Так, для разделения на энантиомеры октанола-2 его предварительно действием фталевого ангидрида перевели в рацемический моноэфир фталевой кислоты, который затем разделили с помощью оптически активного амина на диастереомеры. Диастереомерные соли разложили соляной кислотой, а фталаты омылили раствором щелочи и получили индивидуальные энантиомерные спирты.
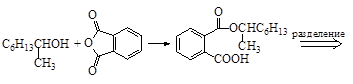
v Ферментативный метод разделения рацематов. Еще Л. Пастер продемонстрировал возможность выделения L-винной кислоты при культивировании Penicillium glaucum в растворе, содержащем рацемическую виноградную кислоту. В процессе развития микроорганизм в основном потреблял D-кислоту. Таким способом можно выделить только один из пары энантиомеров, а второй безвозвратно теряется.
Более эффективно использование ферментов – белковых катализаторов биохимических процессов, специфически воздействующих на субстрат с определенной конфигурацией. Наиболее широко применяют различные липазы (эстеразы), расщепляющие сложноэфирную связь и ацилазы, гидролизующие амидную связь. Например, при действии липазы на диацетат рацемического транс-циклогександиола-1,2 сложноэфирные связи разрушаются только для (R,R)-изомера. После чего разделить два различных химических соединения достаточно просто.
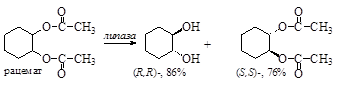
v Кристаллизация под действием энантиомерных затравок. В некоторых случаях при добавлении в насыщенный раствор рацемата затравки чистого энантиомера удается выкристаллизовать один антипод.
Например, при промышленном синтезе антибиотика хлорамфеникола (левомицетина) его синтетический предшественник получается в виде рацемической смеси (R,R)- и (S,S)-трео-2-амино-1-п-нитрофенилпропандиола-1,3. Биологически активный (R,R)-изомер можно выделить добавлением в пересыщенный раствор, частично нейтрализованный соляной кислотой, затравку (R,R)-энантиомера, что вызывает его выкристаллизацию.
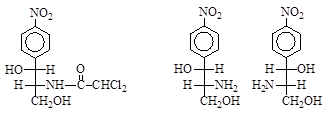
| хлорамфеникол (R,R) | (R,R)- и (S,S)-трео-2-амино-1-п-нитрофенилпропандиол-1,3 |
v Хроматография на хиральных носителях. В настоящее время для разделения рацематов все шире используются хроматографические методы с использованием хиральных носителей. В первых экспериментах в качестве оптически активных сорбентов в основном использовали белки и углеводы, но такие фазы были малоэффективны и неудобны в работе. Долгое время в качестве оптически активной неподвижной фазы используют модифицированную целлюлозу, с чьей помощью осуществлено большое количество разделений рацемических смесей.
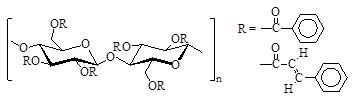
хиральные сорбенты на основе целлюлозы
Современные исследователи предпочитают выполнять задачу выделения индивидуальных энантиомеров из рацематов с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) при использовании в качестве сорбентов модифицированных силикагелей. Обычно в качестве хиральных модификаторов используют производные a-аминокислот.
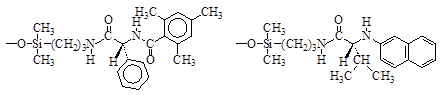
хиральные сорбенты на основе силикагеля для ВЭЖХ
