Метод молекулярных орбиталей
Как уже отмечалось, метод МО рассматривает молекулу как единое образование, в котором каждый электрон принадлежит частице и движется по молекулярным орбиталям в поле всех ядер и остальных электронов молекулы. Молекулярная орбиталь - это область пространства в молекуле, вероятность нахождения электрона в которой существенно отличается от нуля. В отличие от атомной орбитали (АО), молекулярная орбиталь (МО) многоцентрова и охватывает несколько ядер. Заполнение молекулярных орбиталей электронами происходит в порядке увеличения их энергии с соблюдением принципа запрета Паули и правила Гунда. Волновая функция МО (y) конструируется как линейная комбинация волновых функций АО (ji):
y = S сij. (5).
Коэффициенты сi определяются условием нормировки волновой функции, согласно которому вероятность нахождения электрона на заполненной орбитали равна единице:
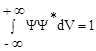 .
.
Атомные орбитали, пригодные для составления МО, должны иметь близкую энергию, одинаковую симметрию и перекрываться в заметной степени. При этом число полученных МО равно числу исходных АО.
Различают три типа молекулярных орбиталей: связывающие, разрыхляющие (антисвязывающие) и несвязывающие. Связывающие МО имеют энергию, меньшую по сравнению с исходными атомными орбиталями. Их заполнение стабилизирует молекулу. Разрыхляющие молекулярные орбитали имеют энергию более высокую по отношению к исходным АО. Заполнение электронами разрыхляющих МО ведет к дестабилизации частицы. Несвязывающие МО локализованы на отдельных атомах и фактически представляют собой атомные орбитали, перенесенные в молекулу без изменения. По симметрии МО разделяют на s (симметричные относительно линии связи) и p (антисимметричные относительно линии связи).
Для иллюстрации принципов метода МО рассмотрим электронное строение молекулы водорода и других двухатомных молекулярных частиц, образованных элементами первого периода. В качестве базисного набора АО будем использовать 1s-орбитали, линейные комбинации волновых функций которых дадут Y-функции двух молекулярных орбиталей:
Y+ = с1j1sA + c2j1sB (6)
Y- = с3j1sA - c4j1sB .
Примем для простоты, что с1 = с2 = с3 = с4 = 1. Тогда,
Y+ = jа + jb (7)
Y- = jа - jb .
На рис. 3.2 приведены кривые волновых функций jа и jb (пунктирная линия) и кривая молекулярной волновой функции Y+ (сплошная линия). Чтобы найти значения последней достаточно сложить значения jа и jb, отвечающие каждой точке. Как следует из рисунка, для областей отрицательных значений координаты z jа и jb практически совпадают с кривой Y+, а в пространстве между ядрами атомов водорода Y+ больше нуля при любых значениях z. Поскольку
Y+2 = jа2 + jb2 + 2jаjb > jа2 + jb2, (8)
вероятность нахождения электронов между ядрами, определяемая значением Y+2, будет больше, если электроны будут располагаться на орбитали Y+, чем, если каждый их них находился бы на одной из атомных орбиталей. Соответственно возрастает плотность отрицательного заряда между ядрами, что приводит к сближению ядер. В результате молекулярные орбитали, являющиеся суммой атомных орбиталей, характеризуются более низкой энергией, чем комбинируемые атомные орбитали. Заселение таких орбиталей электронами стабилизирует образующуюся молекулу.
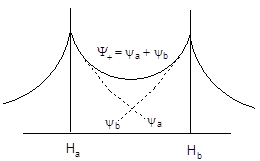 | 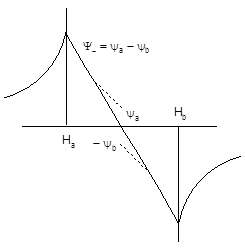 |
| (а) | (б) |
Рис. 3.2. Волновые функции yа, yb и Y+ (а) и yа, yb и Y- (б)
Для молекулярной орбитали Y- значение jb следует брать со знаком минус, в результате чего для точки, равно удаленной от ядер атомов На и Нb, значение Y- становится равным нулю, плотность электронного облака между ядрами понижается, а энергия системы при расположении электронов на Y--орбитали увеличивается, что влечет за собой дестабилизацию частицы.
Форма граничной поверхности полученных МО и энергетическая диаграмма молекулы имеют следующий вид.
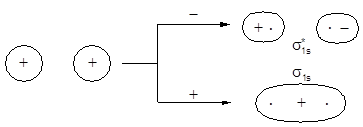 |  |
Рис. 3.3. Молекулярные орбитали и энергетическая диаграмма двухатомной молекулы, образованной элементами первого периода
По аналогии с s-связями в методе ВС, молекулярные орбитали, симметричные относительно линии связи обозначаются символом s. Нижним индексом указывают участвующие в их образовании АО. Справа вверху указывается тип орбитали (sсв., sразр. или sнс.). Часто используют упрощенные обозначения: s º sсв., s* º sразр.. МО, антисимметричные относительно линии связи, обозначают символом p. При переходе через линию связи МО данного типа меняют математический знак на противоположный.
Разместив на МО электроны, получим электронные формулы соответствующих молекулярных частиц. Для качественной характеристики устойчивости молекул в методе МО используется кратность связи (КС), которую рассчитывают как половину разности числа связывающих и разрыхляющих электронов. Кратность связи увеличивается при увеличении устойчивости молекулы. Частицы, для которых КС £ 0, не существуют.
Из полученных данных видно, метод молекулярных орбиталей позволяет описать не только двухэлектронные но и одноэлектронные связи. Кроме этого, метод МО более адекватно отражает физические свойства молекул, в частности он объясняет парамагнетизм молекулы кислорода, в то время как согласно методу ВС молекула кислорода должна быть диамагнитной. Однако метод молекулярных орбиталей несколько проигрывает методу валентных схем в наглядности. Тем не менее метод МО широко используется в современной органической химии, особенно в последние годы, в связи с быстрым прогрессом вычислительной техники.
Таблица 3.2
Кратность связи и магнитное поведение некоторых частиц, соответствующих элементам первого периода
| Частица | Электронная формула | КС | Магнитное поведение |
| H2+ | (s1s)1 | 1/2 | парамагнетик |
| H2 | (s1s)2 | диамагнетик | |
| H2- | (s1s)2(s1s*)1 | 1/2 | парамагнетик |
| He2+ | (s1s)2(s1s*)1 | 1/2 | парамагнетик |
| He2 | (s1s)2(s1s*)2 | частица не устойчива |
Рассмотрим в качестве иллюстрации возможностей метода молекулярных орбиталей результаты расчета несколько относительно простых молекул.
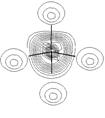
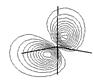
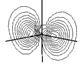
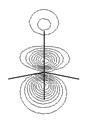
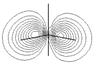
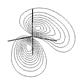
На рис. 3.4 приведена энергетическая диаграмма и контуры МО, полученных при расчете молекулы метана расширенным методом Хюккеля[8] в программном пакете HyperChem 4.5. Близкие по форме МО дают и другие полуэмпирические методы расчета, например mndo, AM1, а также неэмпирический метод расчета (ab inicio). Однако энергии молекулярных орбиталей, полученные разными методами существенно отличаются.
Как видно из рисунка, расчет в рамках метода МО дает несколько неожиданный результат. Дело в том, что вместо ожидаемого для sp3-гибридизации атома углерода набора из четырех эквивалентных связывающих МО получена одна сильно связывающая МО с энергией, равной –24,56 эВ или 2320 кДж/моль (1 эВ на молекулу тождественно 96,452 кДж/моль) и три эквивалентные по энергии (вырожденные) связывающие МО с энергией –15,52 эВ. В то же время, существование в молекуле метана двух отличающихся по энергии уровней, занятых электронами, подтверждается фотоэлектронным спектром, в котором наблюдаются два пика, отвечающие потенциалу ионизации около 13 и 23 эВ. Интересно, что расчеты дают очень близкие величины для энергии связывающих орбиталей молекулы. Таким образом приходится признать, что несмотря на то, что метод ВС дает более четкое и правильное описание формы молекулы, метод МО позволяет более точно определить ее энергетические характеристики.
 | 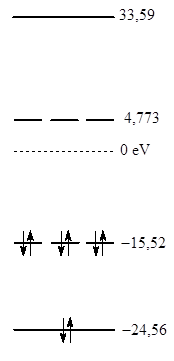 | |
 |  |  |
 |  |  |
 |
Рис. 3.4. Энергетическая диаграмма и проекции контуров МО молекулы метана
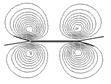
На рис. 3.5 и 3.7 представлены энергетические диаграммы молекул этилена и ацетилена, полученные при расчете по методу АМ-1.
 | 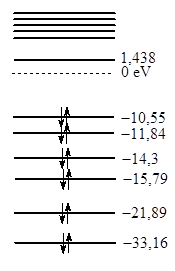 |
| НВМО | |
 | |
| ВЗМО |
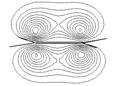
Рис. 3.5. Энергетическая диаграмма и контуры граничных молекулярных орбиталей молекулы этилена
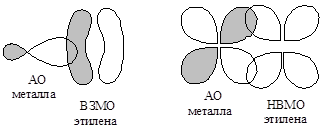
Рис. 3.6. Взаимодействие граничных орбиталей этилена с орбиталями катиона металла при образовании p-комплекса
 Y6,7 Y6,7 | 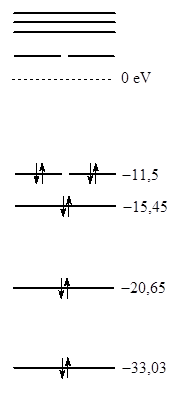 |
 Y4,5 Y4,5 | |
 Y3 Y3 | |
 Y2 Y2 | |
 Y1 Y1 |
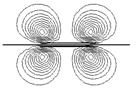
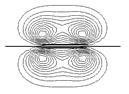
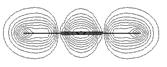
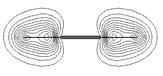
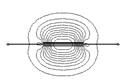
Рис. 3.7. Энергетическая диаграмма и контуры МО молекулы ацетилена (три последние разрыхляющие МО не показаны)
Как видно из рис. 3.5, молекула этилена имеет более сложный энергетических спектр по сравнению с молекулой метана, что вызвано большим числом исходных атомных орбиталей. Но описание особенностей электронного строения данной и других молекул можно сильно упростить, рассматривая не все, а только высшую занятую (ВЗМО) и низшую вакантную МО (НВМО). Эти орбитали часто называют граничными, и именно они в первую очередь определяют реакционную способность молекулярной частицы. Реакции, идущие с присоединением электрона к молекуле этилена или атака на двойную связь нуклеофильного реагента будут направлены на НВМО. В то же время атака электрофильного реагента будет направлена на ВЗМО. Особенно ярко это видно при образование p-комплексов этилена с катионами переходных металлов, в которых этилен, с одной стороны, выступает в качестве донора электронной пары ВЗМО, а с другой стороны, является акцептором пары d-электронов металла за счет НВМО (рис. 3.6).
Метод граничных орбиталей был впервые предложен К. Фукуи[9] в 1952 г. и в настоящее время широко применяется для описания и прогнозирования реакционной способности органических соединений.
ВЗМО молекулы ацетилена имеют более низкую энергию (-11,5 эВ), по сравнению с ВЗМО этилена (-10,55 эВ), поэтому можно ожидать, что к действию электрофильных реагентов тройная связь будет более устойчива, нежели двойная. Экспериментально это подтверждается для большинства электрофильных реагентов, хотя имеются исключения.
Таким образом, очевидно, что метод молекулярных орбиталей не только более точно описывает энергетические свойства молекул, по сравнению с методом валентных связей, но позволяет также прогнозировать реакционную способность молекулярной частицы.
