Силы и потенциальная энергия межмолекулярного взаимодействия
Внутренняя энергия реального газа. Эффект Джоуля - Томсона.
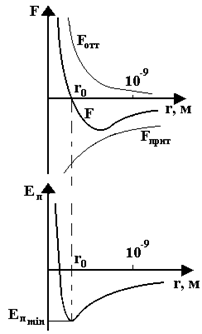 В реальных газах между молекулами действуют силы отталкивания (они считаются положительными) и силы притяжения (они отрицательны). На расстоянии r=r0 результирующая этих сил F=0.(Рис. 7.9, вверху) Это расстояние соответствует равновесному расстоянию между молекулами, на котором они находились бы в отсутствие теплового движения. Этому расстоянию соответствует минимум потенциальной энергии (Рис. 7.9, внизу).
В реальных газах между молекулами действуют силы отталкивания (они считаются положительными) и силы притяжения (они отрицательны). На расстоянии r=r0 результирующая этих сил F=0.(Рис. 7.9, вверху) Это расстояние соответствует равновесному расстоянию между молекулами, на котором они находились бы в отсутствие теплового движения. Этому расстоянию соответствует минимум потенциальной энергии (Рис. 7.9, внизу).
Отметим, что потенциальная энергия реального газа обусловлена только силами притяжения между молекулами (r – достаточно большие).
Рис.7.9.
Пусть дан 1 моль реального газа.
Рассмотрим элементарную работу dA сил межмолекулярного сцепления (притяжения), которые создают внутреннее давление pi и приводят к изменению объема одного моля на dVm. Очевидно:
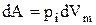 .
.
Работа, которая затрачивается на преодоление сил притяжения идет на увеличение потенциальной энергии системы, т.е.:
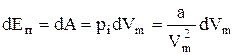 .
.
Здесь учли, что внутреннее давление 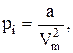 где а - некоторая постоянная.
где а - некоторая постоянная.
Тогда 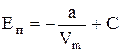 ,
,
где С = 0 т.к. на бесконечно большом расстоянии Еп = 0 ( объем стремится к бесконечности).
Следовательно: 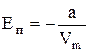 . (7.8.1.)
. (7.8.1.)
Отметим, что знак минус означает, что молекулярные силы, создающие внутреннее давление являются силами притяжения.
Внутренняя энергия реального газа складывается из потенциальной энергии их взаимодействия и их кинетической энергии Ек.
Известно, что средняя кинетическая энергия молекул одного моля газа равна:
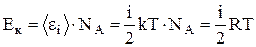 .
.
С учетом того, что 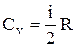 , последнее равенство примет вид:
, последнее равенство примет вид:
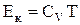 . (7.8.2.)
. (7.8.2.)
Тогда внутренняя энергия 1 моля реального газа, с учетом (7.8.1.) и (7.8.2.), определится так:
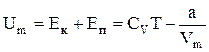 ,
,
т.е. 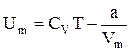 . (7.8.3.)
. (7.8.3.)
Вывод: внутренняя энергия реального газа зависит не только от температуры, но и от объема V.
Практическое применение:Эффект Джоуля - Томсона.
Пусть газ расширяется без теплообмена (адиабатически dQ=0) и без совершения им работы против внешних сил (расширение в пустоту). В этом случае первое начало термодинамики (dQ = dU + pdV) запишется так:
dU = 0,
т.е. U = const.
Но тогда, из (7.8.3.) следует, что при адиабатном изменении объема должна меняться температура. Более того, 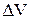 и
и 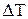 имеют разные знаки. Следовательно, при адиабатном расширении газ должен охлаждаться. Это обнаруженное экспериментально явление.
имеют разные знаки. Следовательно, при адиабатном расширении газ должен охлаждаться. Это обнаруженное экспериментально явление.
Изменения температуры Т реального газа при адиабатическом расширении получило название эффекта Джоуля - Томсона.
Если 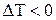 эффект называется положительным, если
эффект называется положительным, если 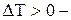 эффект отрицательный.
эффект отрицательный.
Знак 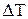 зависит не только от сорта газа, но и от начальных объема и температуры газа. Практическое применение эффекта Джоуля – Томсона позволяет осуществлять сжижение газов.
зависит не только от сорта газа, но и от начальных объема и температуры газа. Практическое применение эффекта Джоуля – Томсона позволяет осуществлять сжижение газов.
