Экспериментальное доказательство основных положений теории
| Существование молекул | 1. Делимость вещества 2. Закон кратных отношений: при образовании из двух элементов различных веществ массы одного из элементов в разных соединениях находятся в кратных отношениях – N2O : N2O2 : N2O3 - 1:2:3. (1803, Дж. Дальтон; 1808, Ж.Л. Гей-Люссак). 3. Наблюдение молекул с помощью ионного проектора, электронного микроскопа, туннельного микроскопа. 4. Явление диффузии. | |
| Наличие промежутков | 1. При смешивании различных жидкостей объем смеси меньше суммы объемов отдельных жидкостей. 2. Явление диффузии. 3. Деформация. | 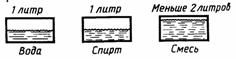 |
| Хаотическое движение молекул |
| 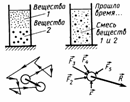 |
| Силы взаимодействия |
|
Диффузия - явление проникновения частиц одного вещества в промежутки между частицами другого. Скорость диффузии зависит от температуры и состояния вещества (быстрее в газах).
Броуновское движение - беспорядочное движение мелких частиц, взвешенных в жидкости или газе, происходящее под влиянием теплового движения молекул. Р. Броун (1827) наблюдал. Движение не прекращается. Роль в природе, технике: питание растений из почвы, в организмах человека и животных всасывание питательных веществ происходит через стенки органов пищеварения, работа органов обоняния, цементация.
22. Масса молекул. Количество вещества.
Массы отдельных молекул и атомов очень малы, поэтому в расчётах удобнее использовать не абсолютные значения масс, а относительные.
Относительная молекулярная масса (или относительная атомная масса) вещества Мr – это отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода. 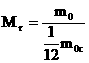 где m0 – масса молекулы (или атома) данного вещества, m0C – масса атома углерода.
где m0 – масса молекулы (или атома) данного вещества, m0C – масса атома углерода.
Относительная молекулярная (или атомная) масса вещества показывает, во сколько раз масса молекулы вещества больше 1/12 массы изотопа углерода С12. Относительная молекулярная (атомная) масса выражается в атомных единицах массы.
Атомная единица массы – это 1/12 массы изотопа углерода С12. Точные измерения показали, что атомная единица массы составляет 1,660*10-27 кг, то есть 1 а.е.м. = 1,660 * 10-27 кг
Относительная молекулярная масса вещества может быть вычислена путём сложения относительных атомных масс элементов, входящих в состав молекулы вещества. Относительная атомная масса химических элементов указана в периодической системе химических элементов Д.И. Менделеева.
Пример:
Для H2 : 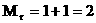
Для О2: 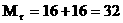
Для Н2О: 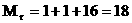
Для воздуха Mr=29
ν - количество вещества; [ν]=моль;
1 моль углерода имеет массу 0,012 кг
NA=6,02.1024 моль-1 - число (постоянная) Авогадро - количество структурных элементов (атомов, молекул) в 1 моле вещества (в 12 г углерода 12С).
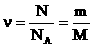 , где М - молярная масса (масса 1 моля);
, где М - молярная масса (масса 1 моля);
