Определить эквивалент и эквивалентную массу хромовой кислоты
5.Найти простейшую формулу соединения, которое содержит 35% азота, 5% водорода, 60% кислорода.
6. Какой заряд ядра и сколько электронов, протонов, нейтронов в атомах брома и кадмия?
7. Напишите электронную и графическую конфигурации атома мышьяка. Определите к какому семейству он относится.
8. Определить валентностьэлементов в соединении и изобразите его графическую формулу: MgO.
9. Выразить концентрацию водного раствора хлорида бария BaCl2 через массовую долю, молярность, моляльность и мольные доли, если его нормальность 2 н, а плотность 1,179 г/мл.
10. Составить уравнения в полной и сокращенной ионной формах (расставить коэффициенты), дать названия всем веществам:
CaCl2 + NaOH = Са(ОН)2 + NaCl
Вопросы
1.Опишите положение в периодической системе и охарактеризуйте свойства элемента с порядковым номером 7.
2. Зонная теория кристаллов.
Вариант 8
Задачи
1.Найдите относительную молекулярную массу аммофоса (NH4)2HPO4.
2.Образец вещества массой 6,6 г содержит 9,03×1022 молекул. Определите молярную массу этого вещества.
3. Относительная плотность газа по воздуху равна 1,517. Рассчитайте количество вещества этого газа, которое заключается в его образце массой 11 г.
4. Найти простейшую формулу оксида хрома, содержащего 68,4 % (масс.) хрома.
5. Сколько граммов карбоната кальция разложилось, если образовалось 11,2 г оксида кальция СаО?
6. Закончить уравнение ядерной реакции: 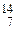 N +
N + 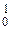 n
n 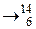 C + …
C + …
7. Напишите электронную и графическую конфигурации атома олова. Определите к какому семейству он относится.
8. Определить валентностьэлементов в соединении и изобразите его графическую формулу: Cr2O3.
9. В 250 г воды растворили 40 г азотной кислоты. Определить массовую долю растворенного вещества.
10. Составить уравнения в полной и сокращенной ионной формах (расставить коэффициенты), дать названия всем веществам:
BaCl2 + K2SO4 = BaSO4 + KCl
Вопросы
1.Опишите положение в периодической системе и охарактеризуйте свойства элемента с порядковым номером 8.
2. Практическое применение электролиза.
Вариант 9
Задачи
1.Определите молярную массу горькой соли MgSO4 × 7 Н2О.
2.Сколько атомов меди содержится в 18,5 г оксида меди (II).
3. Определите число молекул газа, который заполняет сосуд вместимостью 190,4×10–3 м3. Давление газа в сосуде равно 180 кПа, температура 37°С.
4.Вещество содержит (по массе) 26,53 % калия, 35,37% хрома и 38,10 % кислорода. Найти его простейшую формулу.
5. Смесь этилена и ацетилена объемом 16,8 л при н.у. имеет массу 20,5 г. Определить объем каждого газа в смеси.
6.Изотоп некоторого элемента имеет 10 нейтронов в составе ядра атома и атомную массу 19. Определите, что это за элемент.
7. Напишите электронную и графическую конфигурации атома селена. Определите к какому семейству он относится.
8. Определить валентностьэлементов в соединении и изобразите его графическую формулу: CuCl2.
9. Вычислите массу раствора с массовой долей гидроксида натрия в нем 0,23, если для приготовления раствора использовали 4,6 г основания.
10.Выразить концентрацию 1,405 М раствора нитрата серебра через массовую долю, моляльность, нормальность и мольные доли, если его плотность равна 1,194 г/мл.
Вопросы
1.Опишите положение в периодической системе и охарактеризуйте свойства элемента с порядковым номером 9.
2. Нестехиометрические соединения (соединения переменного состава, соединения включения).
Вариант 10
Задачи
1.Чему равна молярная масса хлорной извести CaOCl2.
2.Сколько молекул содержится в 49 г серной кислоты.
3. Во сколько раз оксид углерода (IV) тяжелее метана?
